Причин, способных привести человека к инвалидности, к сожалению, великое множество. Для удобства проведения МСЭ (медико-социальной экспертизы) их классифицируют, объединяя похожие нарушения интеллектуального, психического и физического здоровья в отдельно взятые категории, состоящие из более мелких подгрупп. К одной из них относятся полинейропатии или как их еще называют полирадикулоневропатии.
Это многочисленная группа, неоднородных по своей этиологии и некоторой симптоматике заболеваний, возникших вследствие воздействия негативных экзогенных либо эндогенных факторов.
Патологии объединяет обширное, как правило, дистальное симметричное поражение периферических нервов, приводящее к чувствительным, двигательным, вегетативно-сосудистым и трофическим нарушениям. Все это зачастую существенно снижает качество жизни пациента, тем самым приводя его к утрате трудоспособности в той или иной мере.
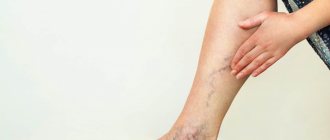
Что такое нейропатия нижних конечностей?
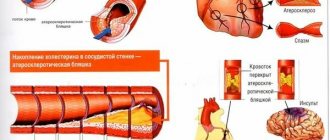
Нейропатия — поражение периферических нервов и питающих их сосудов. Изначально это заболевание не носит воспалительный характер, но впоследствии на него может наслаиваться неврит — воспаление нервных волокон. Нейропатия нижних конечностей включается в группу полинейропатий, основу которых составляют обменные нарушения, ишемия тканей, механические повреждения, аллергические реакции.
По типу течения выделяют нейропатию:
- острую;
- хроническую;
- подострую.
По виду патологического процесса в нервных волокнах нейропатия бывает аксональной (охватывает отростки нейронов — аксоны) и демиелинизирующей (распространяется на оболочки нервных волокон). По симптоматике патология бывает:
- Сенсорной
. Преобладают симптомы нарушения чувствительности и болевой синдром. - Моторной
. Проявляется, преимущественно, двигательными расстройствами. - Вегетативной
. Отмечаются признаки вегетативных и трофических нарушений.
Реклама:
Причины патологии разнообразны. Так, диабетическая форма характерна для метаболических расстройств в нейронах при сахарном диабете. Токсическая, алкогольная вызвана отравлениями, интоксикациями. Прочие возможные причины — опухоли, дефицит витаминов гр.В, гипотиреоз, ВИЧ, травмы, отягощенная наследственность.
При ишиасе у человека возникает защемление нервного ствола в области поясницы. Это приводит к появлению сильного болевого синдрома, поэтому лечение должно быть своевременным, правильным. Подробнее читайте в статье: «медикаментозное лечение ишиаса, основные симптомы».
Лечение
Лечение полинейропатии включает в себя максимально возможное устранение причины, приведшей к её развитию.
- Так, если имеется диабетическая полинейропатия, то необходимо строго и постоянно контролировать сахар крови, находиться под наблюдением врача-эндокринолога, чтобы не допускать декомпенсации основного заболевания.
- Если полинейропатия развилась на почве алкоголизма, надо полностью отказаться от приема алкоголя.Необходимо наладить питание и провести лечение витаминами при развившемся их дефиците.
- Лечение полинейропатий, в основе которых лежат аутоиммунные процессы называют патогенетической терапией. При этом лечение также индивидуализировано и подбирается в зависимости от типа заболевания, с учетом всех нюансов механизма болезни и индивидуальных особенностей пациента. Это лечение высокими дозами глюкокортикоидных гормонов, использование в лечении цитостатиков и препаратов моноклональных антител, проведение высокодозной внутривенной иммунотерапии препаратами иммуноглобулина человеческого класса G и высокообъемного программного плазмафереза.
Чувствительные расстройства — основная группа симптомов
Проявления патологии в области ног могут быть разнообразными, часто они зависят от причины нейропатии. Если болезнь вызвана травмой, симптомы охватывают одну конечность. При сахарном диабете, аутоиммунных заболеваниях признаки распространяются на обе ноги.
Чувствительные нарушения могут быть настолько неприятными, что вызывают у больного депрессивные состояния.
Сенсорные расстройства встречаются во всех случаях нейропатии нижних конечностей. Симптомы обычно наблюдаются постоянно, не зависят от положения тела, режима дня, отдыха, нередко вызывают бессонницу.
- онемение ног;
- чувство ползания мурашков;
- ощущение присутствия инородных предметов под кожей.
Реклама:
Кроме описанных признаков, часто имеются нарушения чувствительности — медленное распознавание холодного, горячего, изменение болевого порога, регулярная потеря равновесия из-за снижения чувствительности стоп. Также часто появляются боли — ноющие или режущие, слабые или буквально нестерпимые, локализуются они в зоне пораженного участка нерва.
[media=
https://youtu.be/svHRBJ9gOgU
]
Причины инвалидности при полинейропатии
Заболевания данной группы, как уже упоминалось, могут развиваться на фоне воздействия различного ряда факторов, поэтому причинами получения инвалидности принято считать следующие:
- Общее заболевание.
- Инвалидность детства.
- Нетрудоспособность, наступившая из-за болезни, полученной во время прохождения военной службы, либо возникшая на протяжении 3-х месяцев после увольнения из ВС.
- Профессиональное заболевание: полинейропатия возникла под влиянием токсичных веществ в условиях производственной деятельности, под воздействием физических факторов (холодовая полинейропатия, вибрационная болезнь, вегетативная полинейропатия перенапряжения рук).
Справка! В ходе присвоения группы инвалидности, наступившей вследствие специфики трудовой деятельности, одновременно устанавливается степень потери профессиональной трудоспособности, выражающаяся в процентах.
Прочие признаки заболевания
По мере развития патологии конечностей повреждаются двигательные нервные волокна, поэтому присоединяются прочие расстройства. К ним относятся спазмы мышц, частые судороги в ногах, особенно, в икрах. Если пациент на данном этапе посещает невролога, врач отмечает снижение рефлексов — коленного, ахиллового. Чем ниже сила рефлекса, тем дальше зашло заболевание. На последних стадиях сухожильные рефлексы могут вовсе отсутствовать.
Главная задача Магнелиса В6 — предупредить недостаток магния в организме. Витамин В6, которых также входит в его состав, помогает организму усваивать магний из синтетического препарата. Подробнее читайте в статье: «магнелис b6 для чего принимают».
Мышечная слабость — важный признак нейропатии ног, но он свойственен поздним стадиям заболевания. Вначале ощущение ослабления мышц транзиторное, потом становится постоянным. На запущенных стадиях это приводит:
- снижению активности конечностей;
- затруднению передвижения без опоры;
- истончению мышц, их атрофии.
Реклама:
Вегетативно-трофические нарушения — еще одна группа симптомов при нейропатии. Когда поражена вегетативная часть периферических нервов, возникают такие признаки:
- на ногах выпадают волосы;
- кожа становится тонкой, бледной, сухой;
- появляются зоны излишней пигментации;
- меняется работа потовых, сальных желез.
У больных с нейропатией плохо заживают порезы, ссадины на ногах, они почти всегда гноятся. Так, при диабетической нейропатии изменения трофики настолько тяжелы, что появляются язвы, порой процесс осложняется гангреной.
О.С. Левин
Кафедра неврологии РМАПО, Москва
Полиневропатия – заболевание периферической нервной системы, характеризующееся диффузным, относительно симметричным поражением нервных волокон и проявляющееся моторными, сенсорными и вегетативными симптомами. Боль, наряду с парезами, амиотрофиями, выпадением сухожильных рефлексов, изменением чувствительности, дисфункцией кардиоваскулярной системы, трофическими расстройствами, относится к наиболее частым проявлениям полиневропатий [1]. Зачастую именно боль бывает основной жалобой пациентов с полиневропатиями и решающим фактором, снижающим качество их жизни. Боль при полиневропатиях является классическим примером невропатической боли, которая, в отличие от наиболее частой – ноцицептивной боли – связана не с раздражением болевых рецепторов, передающимся в ЦНС, а с изменением свойств соматосенсорных нервных волокон [2]. Высокая интенсивность и стойкость невропатической боли, её особый, часто мучительный характер, резистентность к традиционным методам обезболивания придают этой проблеме исключительную актуальность [2, 6, 7].
Особенности болевого синдрома при полиневропатиях По характеру боль при полиневропатиях бывает различной, но наиболее характерна постоянная жгучая, зудящая, мозжащая или холодящая, реже отмечается более острая пронизывающая, простреливающая, режущая, рвущая, колющая [1, 3, 6]. Боль обычно сопровождается изменением чувствительности и, как правило, локализуется в той же зоне. В большинстве случаев боль начинается с наиболее дистальных отделов – подошвенной поверхности стоп, что объясняется опережающим поражением наиболее длинных нервных волокон, а затем, как и другие симптомы полиневропатии, может распространяться в проксимальном направлении (т. е. имеет полиневропатический тип распределения) [6]. Боль может быть спонтанной или вызванной. К вызванной боли относится гипералгезия и аллодиния. Гипералгезия характеризуется усилением болевой чувствительности, в результате чего относительно интенсивная боль может индуцироваться сравнительно слабым болевым раздражением. Аллодиния характеризуется возникновением болевого ощущения при неболевом раздражении – прикосновении, лёгком давлении, штриховом раздражении или разминании (механическая аллодиния), воздействии слабого термического раздражителя, который в норме не вызывает ощущения боли (холодовая или тепловая аллодиния), движении. Вследствие гипералгезии и аллодинии кожа становится крайне болезненной. В типичных случаях больной не может выносить даже прикосновения шерстяного одеяла, а затем иногда и обычного постельного белья. По мере прогрессирования и углубления гипестезии боль может замещаться онемением, а болезненный участок может смещаться в проксимальном направлении. Часто боль отмечается в покое и усиливается в ночное время, нарушая сон. Постоянная, мучительная, плохо поддающаяся лечению, боль нередко приводит и к эмоциональной угнетённости, что, в свою очередь, усиливает болевые ощущения [16]. При хронических полиневропатиях в значительном числе случаев боль имеет тенденцию к спонтанному улучшению в течение нескольких месяцев, но иногда она неуклонно нарастает вместе с другими проявлениями полиневропатии. Регресс боли может свидетельствовать не только о восстановлении функций, но и о дальнейшем прогрессировании патологического процесса (в последнем случае боль уменьшается на фоне расширения зоны снижения поверхностной чувствительности). Характер боли при полиневропатии зависит от остроты процесса, типа и калибра поражённых волокон. Выраженные болевые ощущения чаще возникают при аксональных невропатиях, протекающих с преимущественным поражением тонких волокон [1, 2, 6]. В связи с этим болевой синдром часто сопутствует нарушениям болевой и температурной чувствительности, а также вегетативно-трофическим нарушениям. Возможные причины полиневропатии с выраженным болевым синдромом представлены в табл. 1. В клинической практике самой частой причиной болезненной полиневропатии является сахарный диабет (диабетическая полиневропатия) [7, 16].
Патогенез боли при полиневропатии Непосредственной причиной боли и таких сопровождающих её явлений, как гипералгезия, аллодиния или дизестезия, чаще всего является повреждение Aδ- и C-волокон [2, 16]. Феномены выпадения и раздражения при этом бывают причудливо переплетены. Детали этого процесса остаются неясными, но, по-видимому, некоторую роль играют сенситизация ноцицепторов и связанных с ними С-волокон, которая сопряжена с явлениями нейрогенного воспаления, эктопическая спонтанная активность частично повреждённых участков нервных волокон и регенерирующих аксональных отростков, эфаптическая (без участия медиатора) передача импульсов от одних аксонов к другим (например, между соматосенсорными и болевыми волокнами) при их контакте. Важное значение, по-видимому, также принадлежит вторичной функциональной реорганизации центральных нейронов под действием усиленной периферической афферентации, в частности, центральная сенситизация на уровне задних рогов спинного мозга. Одним из универсальных механизмов невропатической боли служит повышение возбудимости мембран нервных волокон, связанное с повышением экспрессии потенциал-зависимых натриевых каналов [9].
Принципы лечения боли при полиневропатиях Лечение боли при полиневропатиях предполагает воздействие прежде всего на этиологические и патогенетические процессы (табл. 2), а также на все возможные факторы, способствующие развитию или усилению боли. Например, при диабетической полиневропатии – самой распространённой форме болезненной полиневропатии – важное место в патогенезе боли принадлежит гипергликемии, которая может снижать болевой порог и уменьшать эффект анальгетиков, поэтому нормализация содержания глюкозы в крови может привести к существенному уменьшению боли [1, 16]. Невропатическая боль, в отличие от ноцицептивной боли, плохо поддаётся лечению обычными анальгетиками и НПВС, однако её можно контролировать с помощью нескольких групп нейротропных средств, воздействующих на те или иные механизмы невропатической боли. К ним относятся антидепрессанты, антиконвульсанты, местные анестетики, трамадол, опиоидные анальгетики и некоторые другие средства [9, 12, 13]. Механизм действия препаратов для лечения невропатической боли представлен в табл. 3. Антидепрессанты оказывают умеренный эффект при хронической боли любого происхождения, но особенно важное место занимают в лечении невропатической боли. Терапевтическая эффективность антидепрессантов, назначаемых для облегчения невропатической боли, была убедительно продемонстрирована при мета-анализе ряда плацебо-контролируемых исследований. Противоболевой эффект антидепрессантов не связан непосредственно с их антидепрессивным действием, о чём свидетельствует тот факт, что он часто проявляется в значительно более низких дозах и наступает быстрее. Предполагают, что противоболевой эффект связан с усилением активности норадренергических и серотонинергических систем, оказывающих тормозящее влияние на проведение болевых импульсов по ноцицептивным путям в ЦНС [6]. Трициклические антидепрессанты обладают наиболее высокой противоболевой активностью и считаются препаратами выбора при невропатической боли. Дополнительными механизмами их действия являются блокада натриевых каналов и антагонизм по отношению к NMDA-глутаматным рецепторам, которые опосредуют гипералгезию и аллодинию [3, 8, 9]. Наиболее широко применяют амитриптилин. Начальная доза препарата составляет 10-12,5 мг на ночь, затем дозу постепенно увеличивают на 10-25 мг каждые 7 дней до достижения эффекта (максимально до 150 мг/сут). Суточную дозу принимают однократно на ночь или дробят на 2-3 приёма. У некоторых пациентов противоболевой эффект достигается при назначении малых или средних доз, у других – лишь при применении в высоких дозах. При сопутствующей депрессии обычно требуется назначение более высоких доз препарата. При непереносимости амитриптилина возможно назначение других трициклических антидепрессантов, например имипрамина или кломипрамина. Пробное лечение антидепрессантами должно продолжаться, как минимум, 6-8 недель, при этом максимально переносимую дозу пациент должен принимать не менее одной-двух недель. Хотя амитриптилин эффективен примерно у 70 % больных с невропатической болью, излишний седативный эффект, выраженное антихолинергическое действие (сухость во рту, запоры, задержка мочи и т. д.), неблагоприятное влияние на сердечно-сосудистую систему ограничивают его применение. Следует отметить, что у больных с поражением вегетативных волокон (вегетативной невропатией) и развивающейся в силу этого клинически явной или скрытой вегетативной недостаточности чувствительность к побочному действию трициклических антидепрессантов (на сердечно-сосудистую систему, систему мочеиспускания и т. д.) особенно высока. Перед назначением любого трициклического антидепрессанта обязательно предварительное проведение ЭКГ, особенно у лиц старше 40 лет. Следует ограничить применение трициклических антидепрессантов у пациентов с задержкой мочи, закрытоугольной глаукомой, когнитивными нарушениями, нарушениями равновесия и ходьбы. При плохой переносимости трициклических антидепрессантов возможно применение тетрациклических антидепрессантов (например, мапротилина, 25-100 мг/сут) или ингибиторов обратного захвата серотонина и норадреналина (венлафаксина, 150-225 мг/сут, или дулоксетина, 60 мг/сут) [8]. Селективные ингибиторы обратного захвата серотонина (циталопрам, пароксетин) вызывают меньше побочных действий, но оказывают менее отчётливый противоболевой эффект, что, возможно, объясняется отсутствием прямого влияния на норадренергическую передачу. Они показаны, главным образом, в тех случаях, когда боль связана с депрессией, а больной плохо переносит другие антидепрессанты [6, 8, 13]. Антиконвульсанты, по данным контролируемых исследований, уменьшают интенсивность болевых ощущений не менее чем на половину в среднем более чем у 50 % пациентов с невропатической болью. Эффективность антиконвульсантов, как и антидепрессантов, весьма вариабельна, и заранее прогнозировать, произойдёт ли ослабление боли у данного конкретного больного с помощью того или иного препарата, практически невозможно. На данный момент у больных с болезненными полиневропатиями в контролируемых клинических испытаниях доказана эффективность двух препаратов: габапентина и прегабалина [8]. Габапентин – структурный аналог ГАМК, однако механизм его действия объясняется взаимодействием препарата с альфа2-дельта (α2δ) – субъединицей потенциал-зависимых кальциевых каналов. Это приводит к уменьшению выделения таких медиаторов, как глутамат и субстанция Р, и торможению прохождения ноцицептивной импульсации на уровне спинного мозга. Начальная доза габапентина – 100-300 мг на ночь. Затем суточную дозу постепенно увеличивают каждые 3-5 дней на 100-300 мг, переходя на трёхкратный приём. Средняя эффективная доза составляет 1800 мг/сут (600 мг 3 раза в день), максимальная – 3600 мг/сут. На титрование дозы габапентина может уйти от 2 до 8 недель. Прежде чем делать вывод о неэффективности препарата, его максимально переносимую дозу следует принимать одну-две недели. Помимо уменьшения болевого синдрома, препарат может способствовать нормализации аффективного состояния пациентов и ночного сна, однако у некоторых пациентов возможно развитие нежелательной сонливости. Чтобы избежать её, большую часть дозы рекомендуется назначать на ночь. Другие побочные эффекты: головокружение, желудочно-кишечные расстройства, периферические отёки, увеличение массы тела – обычно бывают легко выражены и редко требуют отмены препарата. У пожилых лиц, а также при наличии нарушения глубокой чувствительности препарат следует применять с осторожностью, поскольку он может усугубить нарушения равновесия и ходьбы. Дозу габапентина следует ограничить и при почечной недостаточности. В целом, габапентин оказывает умеренный противоболевой эффект при полиневропатиях, однако его относительная безопасность делает его препаратом выбора в тех случаях, когда пациенты не могут принимать трициклические антидепрессанты. Прегабалин, как и габапентин, является лигандом α2δ-субъединицы кальциевых каналов. По показателям эффективности и безопасности он примерно соответствует габапентину, но имеет некоторые фармакокинетические преимущества, благодаря которым устраняется необходимость длительного титрования и создаются условия для более быстрого эффекта. В контролируемых исследованиях показана эффективность прегабалина при болезненной диабетической полиневропатии (в дозе 150-600 мг/сут) [6, 8]. Эффективность антиконвульсантов, блокирующих натриевые каналы, при полиневропатиях изучена хуже. Наиболее заметный представитель этой группы препаратов – карбамазепин – в течение длительного времени применяется в лечении невропатической боли и остаётся препаратом первого выбора при невралгии тройничного нерва. Карбамазепин первоначально назначают в дозе 100 мг два раза в сутки, затем её повышают до 200 мг 3-4 раза в сутки. Максимальная доза составляет 1200 мг/сут. Побочные эффекты (головокружение, атаксия, нарушение зрения, тошнота, сонливость, головная боль) менее вероятны при медленном увеличении дозы. Предпочтительнее использовать препараты карбамазепина с замедленным высвобождением, которые достаточно принимать два раза в день. Они обеспечивают более стабильную концентрацию препарата в течение суток, что снижает вероятность побочного эффекта. При недостаточной эффективности или непереносимости карбамазепина возможно применение окскарбазепина (300-1200 мг/сут). Данные об эффективности фенитоина, топирамата, ламотриджина, вальпроевой кислоты, леветирацетама в лечении боли при полиневропатиях противоречивы, тем не менее их применение может быть оправданно в резистентных случаях [3, 4, 13]. Местные анестетики, такие как лидокаин или его пероральный аналог мексилетин, наряду с антиконвульсантами относятся к препаратам, стабилизирующим клеточные мембраны. Механизм действия препаратов этого класса связан с блокадой натриевых каналов в нервных волокнах и подавлением в них эктопической спонтанной генерации импульсов. Лидокаин назначают в/в капельно в дозе 5 мг/кг в 100-200 мл изотонического раствора в течение 40-60 минут на протяжении от одной до трёх недель. В некоторых случаях короткий курс в/в инфузий лидокаина может приводить к удивительно стойкому ослаблению интенсивной боли, однако риск многочисленных побочных эффектов, прежде всего на сердечно-сосудистую систему, ограничивает практическую ценность данного метода. В последние годы разработана новая лекарственная форма лидокаина – пластины для трансдермального введения препарата (трансдермальная терапевтическая система – ТТС). ТТС с лидокаином (версатис) прикрепляются к зоне максимальной болезненности (например, на область голеней), особенно если в ней выявляются гипералгезия и аллодиния. Главное достоинство этой лекарственной формы заключается в отсутствии побочных эффектов, связанных с системным действием лидокаина [5]. Кроме того, пластина закрывает участок изменённой чувствительности от дополнительного механического раздражения. Благодаря длительному эффекту ТТС с лидокаином часто помогает успешно контролировать боль в ночное время, которая может быть для больного особенно мучительна. В плацебо-контролируемом исследовании у больных с болезненной диабетической полиневропатией применение ТТС с лидокаином привело к стойкому снижению интенсивности боли более чем на треть и существенному улучшению качества жизни за счёт повышения общей активности, настроения, способности к передвижению, трудоспособности, улучшения сна [5]. К концу исследования примерно у четверти больных, у которых отмечался особенно хороший эффект, удалось отменить другие обезболивающие препараты, перейдя на монотерапию, или, по крайней мере, значительно снизить их дозу. Аналогичные результаты получены и у пациентов с идиопатической сенсорной полиневропатией [11]. При применении ТТС с лидокаином одномоментно прикрепляют от одной до трёх пластин не более чем на 12 часов в сутки. Пробное лечение должно продолжаться не менее двух недель. При получении лечебного эффекта пластины с лидокаином могут при необходимости применяться в течение длительного времени без ослабления обезболивающего эффекта. Трамадол (трамал) обладает обезболивающим эффектом, в основе которого лежит двойной механизм. Помимо влияния на мю-опиоидные рецепторы (его сродство к ним примерно в 10 раз слабее, чем у кодеина), он способен также тормозить обратный захват серотонина и норадреналина, что, по-видимому, в значительной степени потенцирует тот умеренный обезболивающий эффект, который достигается сравнительно слабым опиоидным действием. Терапевтический эффект трамадола при болезненной полиневропатии доказан по меньшей мере в двух плацебо-контролируемых исследованиях [10]. Лечение начинают с дозы 50 мг на ночь (или 25 мг 2 раза в день), спустя 5-7 дней дозу увеличивают до 100 мг/сут. При необходимости дозу повышают до 100 мг 2-4 раза в день. Пробное лечение трамадолом должно продолжаться не менее 4 недель [9]. Эффективность может сохраняться при длительном приёме в течение 6 месяцев и более. Риск лекарственной зависимости у трамадола значительно ниже, чем у других опиоидов, и может рассматриваться как минимальный. Более того, по данным E.H. Adams et al. (2006), при применении трамадола в течение года признаки зависимости от препарата или злоупотребления им возникали не чаще, чем при применении НПВС [4]. Тем не менее следует соблюдать осторожность при назначении трамадола лицам, склонным к формированию лекарственной зависимости. Вероятность побочных эффектов (головокружение, тошнота, запоры, сонливость, ортостатическая гипотензия) ниже при медленном титровании дозы. С осторожностью следует назначать трамадол пожилым лицам, у которых доза препарата не должна превышать 300 мг/сут [4, 9]. Комбинация трамадола с парацетамолом (Залдиар) позволяет снизить дозу трамадола и тем самым риск побочного действия, не жертвуя анальгетическим эффектом [14]. При комбинации двух указанных препаратов, обладающих разным механизмом действия (механизм анальгетического эффекта парацетамола может быть связан с ингибирующим эффектом на центральный синтез простагландинов, возможно, за счёт торможения ЦОГ-3), возникает эффект синергизма. Адекватное обезболивание при приёме комплекса препаратов наблюдается в 1,5-3 раза чаще, чем при применении каждого из соединений в соответствующих дозах. Кроме того, для парацетамола и трамадола характерен взаимодополняющий фармакокинетический профиль, благодаря которому препарат быстро начинает действие – уже через 15-20 минут (за счёт парацетамола) и длительное время поддерживает анальгетический эффект (за счёт трамадола) [14, 15]. За счёт того что в состав Залдиара входит низкая доза трамадола (в одной таблетке содержится 37,5 мг трамадола и 325 мг парацетамола), побочные эффекты при его применении (особенно тошнота, рвота и головокружение) возникают реже, чем при применении трамадола в минимальной рекомендуемой разовой дозе (50 мг). Более того, к настоящему времени накоплен опыт длительной терапии Залдиаром, в частности у больных с невропатической болью, болью в спине, остеоартрозами и т. д. Он свидетельствует о длительном сохранении эффекта препарата, отсутствии тенденции к развитию толерантности и лекарственной зависимости. Так, на протяжении 23-месячного открытого исследования у больных с хронической болью в спине не возникало необходимости увеличивать дозу Залдиара, что свидетельствует об отсутствии толерантности. Назначение препарата не требует длительного титрования дозы, лечение может быть начато с дозы одна-две таблетки в день, в последующем доза может быть повышена до 4 таблеток в сутки [15].
Применение других средств при невропатической боли Для усиления анальгетического эффекта могут применяться агонисты альфа2-адренорецепторов (клонидин, тизанидин), ГАМКергические средства (баклофен, клоназепам), блокаторы NMDA-глутаматных рецепторов. При более или менее локализованной боли целесообразно наружное применение препаратов стручкового перца. Содержащийся в них капсаицин, стимулируя капсаициновые рецепторы, способствует истощению запасов в периферических тканях субстанции P и других нейромедиаторов, с выделением которых связывают развитие гиперестезии и жгучей боли. Предпочтительнее применять 0,025-0,075 % капсаициновый крем. Препарат наносят на кожу от 2 до 4 раз в день не более 6 недель [4, 6, 9].
Последовательность применения средств для лечения невропатической боли На сегодняшний день выбор препарата для лечения боли при полиневропатии не может быть основан ни на её характере, ни на её предполагаемом механизме, и должен проводиться эмпирически с учётом эффективности и безопасности отдельных препаратов, индивидуальной чувствительности пациента, экономической доступности, наличия у него сопутствующих заболеваний [6, 8]. Например, при серьёзной сердечно-сосудистой патологии, закрытоугольной глаукоме, выраженных вегетативных нарушениях, в частности при тенденции к ортостатической гипотензии или задержке мочи, назначения трициклических антидепрессантов следует избегать. Ввиду отсутствия прямых сравнительных исследований, в которых бы сопоставлялась действенность различных препаратов для лечения невропатической боли, их эффективность принято соизмерять косвенно – по показателю NNT («числу пациентов, которых необходимо пролечить, чтобы добиться 50 % облегчения боли у одного пациента») [6, 8]. Этот показатель рассчитывается на основе данных конкретных исследований, чем он оказывается ниже (ближе к единице), тем выше средняя эффективность препарата. Этот показатель дополняется другим показателем, оценивающим безопасность препарата, – NNH («число пациентов, которых необходимо пролечить, чтобы получить побочный эффект, вынудивший отменить препарат («нанести вред»)». Чем выше NNH, тем препарат более безопасен. В табл. 4 представлены указанные показатели в отношении основных средств, применяемых в лечении невропатической боли. О практической полезности препарата наиболее точно свидетельствует соотношение NNT/NNH, которое чем ниже, тем благоприятнее. Оптимальное соотношение эффективности и безопасности при болезненных полиневропатиях отмечено у трициклических антидепрессантов, габапентина (прегабалина) и трамадола, которые обычно рассматривают как препараты первого ряда у больных с болезненной полиневропатией [6, 8, 9]. При ограниченной распространённости боли к препаратам первого ряда может быть добавлена ТТС с лидокаином [6]. В любом случае каждому препарату, назначаемому пациенту с невропатической болью, надо давать полноценный шанс «проявить себя», что предполагает его назначение в адекватной дозе (при условии хорошей переносимости) на достаточно длительный период, указанный выше при описании каждого отдельного препарата [7]. Для оценки эффективности лечения болевого синдрома полезно использовать визуальную аналоговую шкалу. Обычно эффект препарата может считаться клинически значимым, если оценка по такой шкале снижается не менее чем на 50 %.
Комбинирование лекарственных средств при лечении невропатической боли Ни один из препаратов не даёт при невропатической боли гарантированного эффекта. Поэтому хотя число одновременно принимаемых пациентом лекарственных средств по общему правилу следует стараться ограничивать, но в большинстве случаев невропатическую боль удаётся адекватно контролировать лишь с помощью комбинации двух и более средств. Нерационально сразу же назначать комбинацию несколько средств: первоначально следует испробовать один препарат, и лишь убедившись, что в переносимых данным пациентом дозах он оказывает лишь частичный эффект, к нему следует присоединить следующее средство, которое, как правило, обладает иным механизмом действия. В клинической практике часто комбинируют антидепрессант с антиконвульсантом, антиконвульсант с трамадолом или Залдиаром. Возможна также комбинация двух антиконвульсантов, действующих на разные ионные каналы, например габапентина и карбамазепина, однако комбинация карбамазепина и ламотриджина нерациональна. К любой из указанных комбинаций может быть добавлена ТТС с лидокаином. Рекомендуется избегать сочетания трамадола (особенно больших доз) с ингибиторами МАО, селективными ингибиторами обратного захвата серотонина или серотонина и норадреналина, так как подобная комбинация может спровоцировать серотониновый синдром. С осторожностью трамадол следует назначать в комбинации с трициклическими антидепрессантами (учитывая риск серотонинового синдрома) [5]. При лечении боли необходимо широко использовать возможности не медикаментозных методов лечения (психотерапии, психофизиологической релаксации, рефлексотерапии, бальнеотерапии, чрескожной электронейростимуляции, магнитотерапии и других физиотерапевтических процедур). Нельзя забывать и о мощном ресурсе психотерапевтического воздействия, а также о том, что многие пациенты с невропатической болью исключительно чувствительны к плацебо, терапевтический потенциал которого также должен использоваться.
Литература 1. Левин О.С. Полиневропатия. М.: МИА, 2006. 496 с. 2. Строков И.А., Баринов А.Н. Клиника, патогенез и лечение болевого синдрома при диабетической полиневропатии // Неврологический журнал. 2001. № 6. С. 47-54. 3. Штульман Д.Р., Левин О.С. Неврология. Справочник практического врача. М.: МЕДпресс-информ, 2005. 944 с. 4. Adams E.H., Brenier S., Cicero T.J. et al. A comparison of the abuse liability of tramadol, NSAIDs and hydrocodone in patients with chronic pain // J. Pain Symptom Manage, 2006. V. 31(5). P. 465-476. 5. Barbano R.L., Herrmann D.N., Hart-Gouleau S., et al. Effectiveness, tolerability, and impact on quality of life of the 5 % lidocaine patch in diabetic polyneuropathy // Arch. Neurol., 2004. V. 61. P. 914-918. 6. Bennet M. (ed). Neuropathic pain. Oxford University Press, 2006. 176 p. 7. Berger A., Dukes E.M., Oster G. Clinical characteristics and economic costs of patients with painful neuropathic disorders // Pain. 2004. V. 5. P. 143-149. 8. Fennerup N.B., Otto M., McQuay N.J. Algorithm of neuropathic pain treatment // Pain. 2005. V. 118. P. 289-305. 9. Dworkin R.H. Advances in neuropathic pain // Arch. Neurol. 2003. V. 60. P. 1524-1534. 10. Harati Y., Gooch C., Swenson M. et al. Double-blind randomized trial of tramadol for the treatment of the pain of diabetic neuropathy // Neurology, 1998. V. 50. P. 250-257. 11. Herrmann D.N., Barbano R.L., Hart-Gouleau S. et al. An Open-Label Study of the Lidocaine Patch 5 % in Painful Idiopathic Sensory Polyneuropathy // Pain Medicine, 2005. V. 6. P. 379. 12. Irving G.A. Contemporary assessment and management of neuropathic pain // Neurology, 2005. V. 64 (S.3). S. 21-27. 13. Leo R.J. Treatment considerations in neuropathic pain // Curr. Treatment in Neurology, 2006. V. 8. P. 389-400. 14. Medve R., Wang J., Karim S. Tramadol and acetaminophen tablets for dental pain // Anesthesia Progress, 2001. V. 23. P. 34-37. 15. Raffa R.B. Pharmacology of oral combination analgetics: rational therapy for pain // J. Clin. Pharmac. Therapeutics, 2001. V. 26. P. 257-264. 16. Vinik A.I., Mehrabyan A. Diabetic neuropathies // Med Clin North Am., 2004. V. 88. P. 947-999.
Порядок диагностики патологии
Опытный невролог без труда поставит предположительный диагноз по описанным симптомам со слов пациента и по имеющимся объективным признакам — изменению кожи, нарушению рефлексов и т.д.
Методы диагностики весьма разнообразны, вот часть их них:
| Методика | Что показывает |
| Электронейромиография | Установление очага поражения нервной системы — корешков, нервных отростков, тел нейронов, оболочек и т.д. |
| Общий, биохимический анализ крови | Воспалительный, инфекционный процесс, наличие аутоиммунных изменений |
| Анализ крови на сахар | Развитие сахарного диабета |
| Рентгенография позвоночника | Патологии позвоночного столба |
| Спинномозговая пункция | Присутствие антител к собственным нервным волокнам в спинном мозге |
Основным методом диагностики проблем с нервными волокнами остается простая методика электронейромиографии — именно она помогает уточнить диагноз.
Как проявляется заболевание?
Алкогольная полинейропатия имеет набор характерных симптомов, которые постепенно становятся все более выраженными:
- мышцы рук и ног становятся слабыми. Сначала легкая слабость ощущается в ладонях, стопах, а затем распространяется и становится более заметной;
- уменьшение чувствительности, ее постепенное снижение вплоть до исчезновения;
- снижение выраженности рефлексов вплоть до их отсутствия;
- болевой синдром. Болезненность может нарастать постепенно или сразу быть сильной. Обычно боли не связаны с какими-то «внешними» причинами (травмами, нагрузками);
- отеки ног, рук;
- появление мурашек, жжения, других ощущений в конечностях;
- тремор, тики, подергивания мышц, дрожание пальцев;
- проблемы с сердечно-сосудистой, дыхательной системой (одышка, нарушения дыхания, частый пульс, аритмия);
- потливость (появляется неожиданно, не связана с нагрузками, температурой тела или жарой);
- нарушения координации движений, головокружение, проблемы с равновесием.
Симптомы могут резко нарастать после сильной алкогольной интоксикации, запоя, часто они остро проявляются после переохлаждения. В других случаях они усиливаются постепенно, на фоне общего ухудшения состояния здоровья на фоне хронической алкогольной зависимости. Чаще заболевание развивается подостро за несколько недель или месяцев: нарушается чувствительность рук или ног, икроножные мышцы становятся болезненными. При сдавливании болезненность усиливается. Без лечения появляется слабость мускулатуры — вплоть до паралича, атрофии.
Заказать лечение алкоголизма
Работаем круглосуточно, опытные врачи, 100% анонимно.
Основы лечения нейропатии
Лечить данное заболевание нужно комплексно, обязательно с коррекцией основной патологии. При аутоиммунных болезнях назначаются гормоны, цитостатики, при диабете — сахароснижающие лекарства или инсулин, при токсическом типе болезни — очищающие методики (гемосорбция, плазмаферез).
Целями терапии нейропатии нижних конечностей являются:
- восстановление нервной ткани;
- возобновление проводимости;
- коррекция нарушений в системе кровообращения;
Реклама: - улучшение самочувствия;
- снижение болевых ощущений и прочих расстройств;
- оптимизация двигательной функции ног;
- повышение скорости обмена веществ.
Существует много методик лечения, основная из них — медикаментозная.
Хирургическое лечение практикуют только при наличии опухолей, грыж, после травм. Всем больным для предотвращения атрофии мышц показаны физические упражнения из специального комплекса ЛФК, в первое время их выполняют под контролем врача-реабилитолога.
При нейропатии следует соблюдать диету с увеличением содержания витаминов гр.В, а также надо исключить алкоголь, продукты с химическими добавками, маринады, жареное, копченое.
Заболевание успешно лечится при помощи физиопроцедур. Отлично зарекомендовали себя массаж, магнитотерапия, лечебные грязи, рефлексотерапия, электростимуляция мышц. Для предупреждения формирования язв следует носить специальную обувь, применять ортезы.
Основные препараты для лечения патологии
В лечении нейропатии препараты играют ведущую роль. Поскольку в основе лежит дегенерация нервной ткани, следует медикаментозным путем восполнять структуру нервных корешков. Это достигается путем применения таких лекарств:
Реклама:
- Нейропротекторы
, ускорители метаболизма в нервных клетках — Пирацетам, Милдронат. Улучшают трофику нервной ткани, помогая улучшить ее структуру. - Антихолинэстеразные препараты
— Ипидакрин, Прозерин. Оптимизируют сенсорную работу нервов, помогают в передаче нервных импульсов. - Антиоксиданты
— Мексидол, Цитофлавин. Способствуют «гашению» действия свободных радикалов, усугубляющих разрушение периферических нервов. - Препараты альфа-липоевой кислоты
. Усиливают метаболизм, усиливают восстановление нейроцитов, особенно показаны при диабетической нейропатии.
В обязательном порядке в курсе терапии применяются витамины группы В, особенно показаны В12, В6, В1. Чаще всего назначаются комбинированные средства — Нейромультивит, Мильгамма в таблетках, уколах. После их приема устраняются расстройства чувствительности, все симптомы уменьшают выраженность.
Чем еще лечат нейропатию?
Реклама:
Очень полезны для организма при любой форме нейропатии нижних конечностей витамины, являющиеся мощными антиоксидантами — аскорбиновая кислота, витамины Е, А. Их обязательно применяют в комплексной терапии заболевания для уменьшения разрушительного влияния свободных радикалов.
При сильных мышечных спазмах больному помогут миорелаксанты — Сирдалуд, Баклофен, которые применяют только с назначения врача — при злоупотреблении они способны увеличить слабость мышц.
Есть и другие лекарства против данной патологии. Они подбираются индивидуально. Таковыми являются:
- гормональные средства для подавления боли, воспалительного процесса — Преднизолон, Дексаметазон
; - сосудистые лекарства для улучшения кровообращения в тканях — Пентоксифиллин, Трентал
; - антидепрессанты, седативные средства, препараты против излишней тревожности — Амитриптиллин, Дулоксетин
; - анальгетики, в том числе наркотические при сильных болях — Трамадол, Анальгин, а также НПВН — Кетопрофен, Кетонал Дуо
.
Местно рекомендуется применять мази с новокаином, лидокаином, нестероидными противовоспалительными средствами, а также согревающие мази с красным перцем, ядами животных. При бактериальном поражении кожи стоп, ног накладывают повязки с антибиотиками (мази Тетрациклиновая, Оксациллин).
Народное лечение нейропатии
Лечение народными средствами используют с осторожностью, особенно, при диабете. Рецепты могут быть такими:
- Соединить желток сырого яйца и 2 ложки оливкового масла. Добавить 100 мл сока моркови, столовую ложку меда. Пить по 50 мл трижды в день после еды. Курс — 14 дней.
- Влить в ведро теплой воды 2/3 стакана уксуса 9%, насыпать стакан соли. Подержать ноги в воде 15 минут. Курс — раз в день месяц.
- Смешать 3 столовые ложки семян пажитника, столовую ложку лаврового листа, все измельчить. Заварить в термосе литром кипятка на час, потом пить по малым порциям в течение дня. Курс — 10 дней.
- Развести голубую глину водой до кашицы, нанести на ноги. Дать высохнуть, потом смыть. Повторять каждый день 2 недели.
При своевременной терапии болезнь имеет хороший прогноз. Даже если причина нейропатии очень тяжелая, ее можно замедлить или остановить прогрессирование, а также повысить качество жизни человека.
Причины
Ряд факторов может привести к развитию невропатии, в том числе:
- Алкоголизм. Скудная диета может привести к дефициту витаминов.
- Аутоиммунные заболевания. Они включают такие заболевания как синдром Шегрена, системная красная волчанка, ревматоидный артрит, синдром Гийена-Барре, хроническая воспалительная демиелинизирующая полинейропатия и некротический васкулит.
- Диабет. Более чем у половины пациентов с диабетом развиваются некоторые типы нейропатии.
- Воздействие ядов. Токсичные вещества включают в себя тяжелые металлы или химикаты.
- Лекарства. Некоторые лекарства, особенно те, что используются для лечения рака (химиотерапия), могут привести к развитию периферической невропатии.
- Инфекции. К ним относятся некоторые вирусные или бактериальные инфекции, в том числе болезнь Лайма, опоясывающий лишай, вирус Эпштейна-Барр, гепатит С, проказа, дифтерия и ВИЧ.
- Наследственные заболевания. Например такое заболевание как болезнь Шарко-Мари-является наследственным типом нейропатии.
- Травма или компрессия на нерв. Травмы, такие как дорожно-транспортные происшествия, падения или спортивные травмы, могут повредить или даже привести к разрыву периферических нервов. Компрессия нерва может возникать при постоянном воздействии на периферические нервы.
- Опухоли. Злокачественные и доброкачественные опухоли могут повреждать нервы или оказывать давление на них.
- Дефицит витаминов. Витамины группы В, в том числе B-1, B-6 и B-12, витамин Е и ниацин имеют большое значение для нервов.
- Заболевания костного мозга. Они включают в себя наличие аномального белка в крови (моноклональные гаммопатии), миеломная болезнь, лимфома и амилоидоз.
- Другие заболевания. К ним относятся заболевания почек, заболевания печени, заболевания соединительной ткани и щитовидной железы (гипотиреоз).
Осложнения полинейропатии могут включать
- Ожоги и травмы кожи. Если есть онемение частей тела пациент не может чувствовать изменения температуры или боль.
- Инфекции. Ноги и другие области тела со сниженной чувствительностью могут незаметно повреждаться. Необходимо следить за целостностью кожных покровов, особенно если есть сахарный диабет так как даже незначительные повреждения кожи могут приводить к инфицированию тканей.