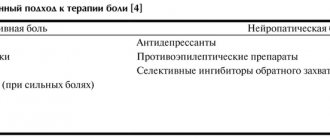
Медиатор ацетилхолин: зачем он нужен человеку и другим живым существам? Как связаны между собой ацетилхолин и никотин? Где вырабатывается ацетилхолин и как он работает?
Ацетилхолин — это один из основных медиаторов в нервной системе. Но информации про медиатор ацетилхолин, написанной понятным языком, очень мало. Википедия и другие источники рассказывают про нейромедиаторы с множеством сложных терминов, которые с первого раза тяжело понять. В этой статье мы попытаемся рассказать про ацетилхолин простым и понятным языком.
Что такое вообще нейромедиаторы? Нейромедиаторы — это такие химические вещества, которые переносят информацию в нервной системе человека. То есть информация между нервными структурами, в этом случае, передается не с помощью электрического импульса, а именно благодаря особенным молекулам, которые плавают в межклеточной жидкости. Эти молекулы и называются медиаторами.
Нужно сразу рассказать и про самые важные для человека свойства ацетилхолина. Он напрямую влияет на память и успеваемость. Чем выше уровень ацетилхолина — тем они выше. И вторая важная функция медиатора — процесс засыпания. Мы засыпаем, когда ацетилхолина у нас совсем мало. Если вы не можете уснуть, вероятно, у вас высокий уровень ацетилхолина. Это может быть связано с тем, что вы много двигались или вообще работали. Почему мы расскажем ниже.
Молекула ацетилхолина
Открытие медиатора ацетилхолина
Ацетилхолин стал первым медиатором, который открыли ученые. И сделал это немецкий фармаколог Отто Леви. В его удивительном эксперименте ацетилхолин останавливал сердце лягушки.
- Эксперимент с медиатором ацетилхолином и сердцами лягушек
Ученый взял два лягушачьих сердца и погрузил их в физиологический раствор. А особенность сердца лягушки такова, что они могут очень долго биться в особенном физиологическом растворе. Потом он начал раздражать блуждающий нерв, который выходил из одного из сердец, электрическим током. Сердце замедляло свой ритм (так и должно происходить).
После этого ученый набрал возле сердца немного жидкости в шприц, и вылил эту жидкость в сосуд, где билось второе сердце. Второе сердце тоже замедлило свой ритм.
Эксперимент Отто Леви
За открытие ацетилхолина, и вместе с ним вообще нейромедиаторов, Леви наградили Нобелевской премией. Говорят, что опыт с лягушками приснился ему ночью. Причем сон повторялся два раза, с первого раза ученый не понял, что это такое ему привиделось.
Причины недостатка
Уровень этого нейротрансмиттера имеет тенденцию снижаться с возрастом. Потеря памяти, которую мы считаем частью возрастного когнитивного снижения, часто вызывается этим падением. Также низкий уровень может быть по нескольким другим причинам:
- Антитела против рецепторов ацетилхолина, в случае миастении [];
- Инсулинорезистентность и диабет мешают синтезу ацетилхолина [];
- Диеты с низким содержанием жиров;
- Лекарства (антихолинергические препараты).
Ацетилхолин и никотин
Нейромедиатор ацетилхолин важен в том плане, что именно его молекулу копирует никотин. Вообще, почти все наркотики похожи по строению молекул на разные нейромедиаторы.
- Никотин подменяет ацетилхолин.
- Опиум и героин копируют другой медиатор — дофамин, который еще называют «гормоном счастья».
- Экстази заменяет собой серотонин — один из гормонов удовольствия.
- Алкоголь не заменяет своей молекулой никакой медиатор, но воздействие его на обменные процессы в мозге очень сильное. Из-за алкоголя повышается уровень дофамина, хотя и не так сильно, как из-за опиума. А еще алкоголь усложняет работу ГАМК — нейромедиатора, который отвечает за спокойствие, сосредоточенность и обучение. То есть алкоголь «отключает мозг» и воздействует сразу на две системы медиаторов.
Существует препарат, которое блокирует тягу к никотину — это Табекс с активным веществом цитизином. Есть и более современный препарат Чемпикс с действующим веществом варениклин. Молекулы этих веществ соединяются с ацетилхолиновыми рецепторами в тех местах, куда крепятся ацетилхолин у здоровых людей или никотин у курильщиков. В итоге, тяга к никотину исчезает. Впрочем, лекарства тем, кто хочет бросить курить не обязательны, в человеческом организме есть все, чтобы справиться самостоятельно с этой проблемой.
Кроме курительного есть еще жевательный, нюхательный и даже сосательный табак. Никотин может впитываться через кожу. На этом основано действие никотиновых пластырей. Бывает еще никотиновый спрей и жвачки.
Молекулу ацетилхолина копирует не только никотин из табака. К примеру, вещества агонисты или «заменители» ацетилхолина есть еще в белладонне и дурмане. Действие этих растений на человеческий организм еще разрушительнее, чем у табака.
Дурман может вызвать галлюцинации, тахикардию, светобоязнь.
Но любой яд в маленьких дозировках становится лекарством, и препараты из дурмана и белладонны используют для снятия боли, спазмов, для проверки зрения и в некоторых других целях. К примеру, основное назначение препарата Белластезин — обезболивание при язве желудка. Но с такими лекарствами все-таки следует быть предельно осторожными и стараться их избегать. Кроме множества побочных эффектов они вызывают стойкую зависимость.
Препарат, который дублирует ацетилхолин
А вообще никотин и похожие на него вещества в растениях — это токсины. Растения используют их как нервно-паралитический яд от жуков и других вредителей, которые хотят ими полакомиться. На насекомых никотин действует, как смертельный яд, они меньше и уязвимей, чем люди. В небольшом количестве никотин есть даже в спелых помидорах, чуть больше его в листьях томатов и листьях картофеля. А чтобы насекомые не покушались на огородные растения можно использовать перетертый в порошок табак. Его применяют и как удобрение.
О.А. Громова1,2, К.В. Рудаков1,2, И.Ю. Торшин1,2
1Российский сателлитный центр института микроэлементов ЮНЕСКО, Москва
2Лаборатория вычислительной и системной биологии ВЦ им. А.А. Дородницына, РАН, Москва
Ключевые слова: холин, клеточная биохимия, физиологические эффекты.
Холин является одним из витаминоподобных веществ. Биологические эффекты холина наиболее важны в нервно-мышечной системе, где холин является предшественником ацетилхолина, важнейшего нейромедиатора. Также холин необходим для регулировки механических свойств клеточных мембран и является донором метильных групп для синтеза S-аденозилметионина. Вышеупомянутые клеточные и биохимические эффекты холина соответствуют спектру физиологических эффектов данного вещества. Следует отметить, что до сих пор достоверный спектр физиологических эффектов холина не был систематически проанализирован на основе объективных данных. Последнее приводит к необоснованным спекуляциям с целью продвижения холиновых препаратов и чрезвычайному преувеличению терапевтической значимости холинергических препаратов. В данной работе, мы ставим своей целью определить спектр физиологических эффектов холина на основе данных фундаментальной медицины. Знание достоверного спектра холина позволяет объективно оценить реальную применимость холиновых препаратов в различных областях медицины, в т. ч. неврологии. Результаты анализа сопоставляются с имеющимися данными по доказательной медицине с целью указания на реальные возможности холиновых препаратов при их использовании в рамках персонализированной медицины. Введение Создание и правильное применение высокоэффективных нейропротективных препаратов искусственного и естественного происхождения – важнейшая задача в современной медицине. Только в России заболеваемость инсультом составляет около полумиллиона случаев в год, что делает необходимым разработку эффективных терапевтических протоколов на основе отдельных препаратов. Адекватное воплощение протоколов должно проводится в рамках персонализированной медицины, т. е. принимать во внимание индивидуальные особенности каждого из пациентов. Известные нейропротективные препараты отличаются спектром своего физиологического воздействия на организм. Существуют препараты с чрезвычайно широким спектром воздействия (например, церебролизин, оказывающий положительное влияния на десятки физиологических механизмов [1]). Есть также препараты с крайне узким спектром воздействия (например, тромболитики, которые воздействуют исключительно на гемостаз). Другие препараты воздействуют на несколько специфических физиологических подсистем организма. Интенсивность и разносторонность этих воздействий и определяют, в конечном счете, степень терапевтической эффективности препаратов. Холин, фосфатидилхолин, ЦДФ-холин и другие производные холина – хорошо известные БАДы, повсеместно использующиеся в школах здорового питания (см., например, [2]). Предметом данной статьи является анализ спектра всех возможных физиологических воздействий препаратов на основе холина. Очевидно, что установление этого спектра на основе данных фундаментальной медицины, клинических исследований и постгеномной биологии позволит установить реальную область терапевтической применимости данной группы препаратов. Анализ в данной работе проводился с использованием поиска общественных баз данных (включая базы данных по геному человека на сайтах www.genome.gov, ncbi.nlm.nih.gov) и имеющейся литературе по фундаментальной медицине и клиническим исследованиям. Последовательно рассматриваются потребность в холине, его доступность в продуктах питания, фундаментальные физиологические механизмы холина и его производных и данные клинических исследований.
Холин: его источники и диетический дефицит холина Холин (витамин B4, рис. 1) входит в состав лецитина, играет роль в синтезе и обмене фосфолипидов в печени, является предшественником нейротрансмиттера ацетилхолина. Холин широко распространён в повсеместно используемых пищевых продуктах в виде свободного холина; в животных источниках и в сое в виде составной части молекулы лецитина. Основные пищевые источники холина: яйца, печень, постное мясо, рыба, соевые бобы, овсянка, цветная капуста, шпинат, капуста белокочанная, арахис. Он является составной частью лецитина. Содержание холина в различных пищевых продуктах указано в таблице 1. В обычном рационе содержится 500-900 мг холина. По рекомендациям, принятым в России, потребность взрослого человека в холине составляет 500-1500 мг/сутки. Верхний допустимый уровень потребления: 1000-2000 мг/сутки – для детей до 14 лет, 3000-3500 мг/сутки – для детей старше 14 лет и взрослых [3]. Недостаточность холина может наблюдаться только в экстремальных ситуациях (хронический алкоголизм, генетические дефекты), поскольку холин присутствует в большом количестве продуктов. Более того, организм человека может синтезировать холин из других пищевых компонентов при отсутствии холина в рационе. Дефицит холина (в отличие, например, от дефицита магния или пиридоксина) не является нозологией по МКБ вследствие достаточно низкой специфичности симптоматики. При доказанной недостаточности холина развиваются следующие нарушения: непереносимость жира (диарея и метеоризм при съедании жира), гипертония, ухудшение роста, язвы желудка, изменения сердечного ритма, недостаточность печёночной и почечной функций. Для холина установлен верхний допустимый уровень потребления (3000-3500 мг/сут в России, Методические рекомендации МЗ РФ [3]). Большие дозы холина (граммы) приводят к повышенному потоотделению, тошноте, появлению резкого рыбного запаха кожи. В группе пациентов с инсультом, принимавших 2000 мг/сут, чаще отмечались случаи головной боли и головокружения [4]. Производителями холиновых препаратов неврологической направленности (цитиколин) указываются побочные действия в форме аллергических реакций (сыпь, зуд кожи и т. п.), возможно развитие шока. Противопоказаниями к назначению холиновых препаратов являются ваготония (преобладание тонуса парасимпатической части вегетативной нервной системы) и повышенная чувствительность к препарату. Опять же в соответствии с рекомендациями производителей, не рекомендуется применение у детей до 18 лет (в связи с отсутствием данных), а в период беременности лекарственный препарат назначают только, если ожидаемая польза превосходит потенциальный риск.
Фундаментальные механизмы воздействия холина на физиологию С точки зрения фундаментальной медицины, холин и его метаболиты необходимы для трёх физиологических процессов (рис. 2): поддержание структурной стабильности мембран, холинергическая нейротрансмиссия (через синтез ацетилхолина) и участие в метилировании ДНК через производное холина триметилглицин (бетаин). На основе бетаина синтезируется источник метильных групп, молекула S-аденозилметионина. Фосфатидилхолин (основной компонент лецитина) – один из фосфолипидов, образующих клеточную мембрану. Фосфолипиды, помимо образования клеточной мембраны, также служат промежуточным продуктом в системах сигнализации клетки. Высвобождаясь из клеточной мембраны посредством фосфолипаз, фосфолипиды участвуют в каскаде арахидоновой кислоты, опосредующем провоспалительные реакции. Фосфолипаза D катализирует гидролиз фосфатидилхолина с образованием фосфатидной кислоты и, опять, холина, который секретируется в цитозоль. Передача сигнала через фосфатидилхолин – интегральная часть многих молекулярных механизмов клетки, (например, передача сигнала от белка «фактор стимуляции колоний клеток», приводящего, в конечном итоге, к росту популяции лейкоцитов [5, 6]. Именно с сигнализацией через фосфатидилхолиновые каскады и связано, вероятно, увеличение апоптоза клеток (например, лимфоцитов [5]). Ацетилхолин – нейротрансмиттер как периферической, так и центральной нервной системы. В периферической нервной системе ацетилхолин активирует мышечные клетки. В ЦНС ацетилхолин образует холинергическую систему, включающую многочисленные типы рецепторов ацетилхолина и ферментов катаболизирующих этот нейротрансмиттер. Активация холинергической системы, в целом, оказывает скорее возбуждающее, чем тормозящее действие на нервно-мышечную систему [7, 8]. Когда ацетилхолин взаимодействует с АХ-рецепторами мышц скелета, открываются ионные натриевые каналы, натрий поступает в клетку и стимулирует сокращение. В случае миокарда, ацетилхолин обладает противоположным действием – уменьшает сократимость кардиомиоцитов. В ЦНС ацетилхолин служит нейромодулятором функции синапсов, и глубокий дефицит ацетилхолина связан с ухудшением работы памяти при болезни Альцгеймера [7]. Физиологические эффекты ацетилхолина значительно зависят от локализации рецепторов в определённых тканях и органах (табл. 2) и могут быть весьма важны при анализе пациента в контексте персонализированной медицины (см. далее). Существует два основных класса ацетилхолиновых рецепторов: никотиновые и мускариновые. Названия рецепторов связаны с лигандами, активирующими эти рецепторы. Никотиновые рецепторы расположены на мышечных клетках, в ЦНС и меняют проницаемость мембраны для ионов натрия, калия и хлорида. Мускариновые рецепторы находятся в ЦНС и периферии, также в миокарде, лёгких, верхнем отделе ЖКТ и потовых железах. Мускариновые рецепторы ацетилхолина не меняют ионной проводимости мембран, но инициируют внутриклеточную передачу сигнала через G-белки [9]. Ацетилхолин и холин увеличивают уровни окиси азота в плазме и нитритов в эритроцитах. Возможный механизм – активация М1 мускариновых рецепторов ацетилхолина [10, 11]. Увеличенная концентрация NO приводит к вазодилатации. Окись азота также является наиболее вероятным механизмом дезагрегантного действия холина [12], и уменьшения агрегации эрироцитов также способствуют понижению свёртываемости крови [11]. На основе одного из производных холина, бетаина, синтезируется молекула S-аденозилметионина, компонента клеточной биохимии, важного для поддержания структуры генома. S-аденозилметионин – промежуточный продукт трансформации аминокислоты метионина, поступающей с избытком белковой пищи (мясо, творог, яйца). Цикл трансформаций метионина включает гомоцистеин, метионин, S-аденозилметионин и S-аденозилгомоцистеин (рис. 3). Гомоцистеин, независимый фактор атеросклероза и инсульта, существенно отягчает реабилитацию пациентов. Наряду с фолатами, витаминами В12 и В6, S-аденозилметионин участвует в обезвреживании гомоцистеина (рис. 4). Однако, в отличии от обезвреживания гомоцистеина в каскаде фолатов, трансформация гомоцистеина и метионина через S-аденозилметионин может приводить к:
1) усиленному метилированию ДНК вследствие более высоких уровней S-аденозилметионина и 2) повышению уровня катехоламинов.
Избыток холина, следовательно, может отрицательно сказываться на структуре генома вследствие усиления его метилирования. Следует также отметить, что раковые клетки содержат повышенные уровни холина что, по всей видимости, связано именно с характерными для онкологии нарушениями метаболизма фосфолипидов [13]. Повышенное содержание холина соответствует увеличенному метилированию ДНК (вследствие увеличенных уровней S-аденозилметионина) и, следовательно, усугублению онкологически обусловленных хромосомных нарушений. Одним из интересных физиологических эффектов холина на клеточную биохимию является также влияние на уровни катехоламинов. Эксперименты на клетках в культуре показали, что холин стимулирует секрецию катехоламинов (адреналина, в частности) [14, 15]. Катехоламины также зависят от уровней S-аденозилметионина [16] и являются одним из основных регуляторов вазоконстрикции. ЦДФ-холин (цитидилдифосфохолин, основа таких препаратов как цитиколин и др.) приводит к увеличению катехоламинов в плазме [17]. Более высокие уровни катехоламинов связаны с повышенным артериальным давлением и, таким образом, далеко не всегда полезны при инсульте и других заболеваниях. Внутрибрюшинное введение ЦДФ-холина и в самом деле приводит к увеличению артериального давления в эксперименте [17]. Вышеупомянутые механизмы воздействия холина подтверждаются и с пост-геномной точки зрения, включающей данные обо всех известных генах через анализ функциональной связи [16]. В целом, с холином в человеческом организме взаимодействуют более 40 белков, кодируемых приблизительно таким же количеством генов. Три разобранных выше пути физиологического воздействия холина (фосфатидилхолин, ацетилхолин, S-аденозилметионин) отображены в таблице 3. Биологические функции этих белков уточняют диапазон влияния ацетилхолина на физиологию человека. В частности, данные полногеномного анализа позволили выделить основные белки, участвующие в метаболизме, транспорте холина и в функционировании системы холинергических рецепторов. Многочисленные генетические дефекты (т. н. «редкие мутации») каждого из этих генов будут приводить к определённым биохимическим и соответствующим клиническим проявлениям. Например, мутации, приводящие к потере функций белков метаболизма холина, приводят к понижению потребности в холине у конкретного пациента. И наоборот, мутации этих генов, приводящие к усилению функции соответствующих белков приводят к повышению потребности в холине.
Клинические исследования холиновых препаратов Анализ данных клеточной биологии и фундаментальной медицины указывает на то, что один из основных эффектов холиновых препаратов – влияние на холинергическую нейротрансмиссию, что приводит к оптимизации нервной и нервно-мышечной проводимости. Побочным эффектом этого является замедление процессов апоптоза в ткани головного мозга. Оба эти эффекта холина могут быть важны при пост-инсультном восстановлении нервной ткани. Соответственно, клинические исследования холиновых препаратов, таких как цитиколин и др., ориентированы именно на восстановление после инсульта. Мета-анализ исследований по пероральному приёму, например цитидил-дифосфохолина, показал некоторый положительный и кратковременный эффект приёма препарата на функционирование памяти пациентов [18]. Мета-анализ 10 исследований по цитиколину (2 279 пациентов) указал на снижение частоты смертности и осложнений в группе принимавших препарат [19]. Мета-анализ исследований 1 372 пациентов показал небольшое, но статистически значимое различие в скорости восстановления пациентов (по шкалам mRS, BI, и NIHSS), принимавших цитидилдифосфохолин перорально в течение 3 месяцев (отношение шансов 1,33; 95 % достоверный интервал 1,1-1,6; p = 0,003) [20] при использовании доз препарата не менее 2000 мг/сут. Индивидуальные рандомизированные исследования воздействия препаратов холина отличаются по своему качеству и степени достоверности результатов. Изучение влияния цитиколина на объём инфаркта мозга на 100 пациентах в остром периоде ишемического инсульта на основе магнитно-резонансной томографии показало достоверное уменьшение прироста ишемического очага в группе больных, получавших 500 мг/сут цитиколина в течение 6 недель [21]. В мультицентровом двойном слепом плацебо-контролируемом исследовании цитиколина у 272 пациентов с инсультом средней и тяжёлой степени 133 пациента ежедневно на протяжении 14 дней получали цитиколин в/в по 1000 мг/сут [22]. К 14-у дню – достоверное улучшение в группе цитиколина только в случае когнитивных функций. Результат предполагает, что в/в введение цитиколина в остром периоде инсульта, возможно, способствует восстановлению функций при обратимых поражениях тканей. В то же время, сравнительно большое мультицентровое исследование 899 пациентов с острым инсультом в бассейне средней церебральной артерии показало крайне противоречивые результаты [4]. Так, приём цитиколина в дозе 2000 мг/сут на протяжении 6 недель способствовал двукратному изменению индекса Barthel по сравнению с группой пациентов, принимавших плацебо. То же самое наблюдалось при приёме дозы в 500 мг/сут. Парадоксально, однако, что результаты у пациентов, принимавших цитиколин по 1000 мг/сут, были сравнимы с группой пациентов, принимавших плацебо (рис. 5). Более того, несмотря на то, что в группе приёма цитиколина отмечена достоверно более высокая пропорция пациентов, показавших улучшение после 6 недель терапии, улучшение отсутствовало при сравнении на 12-й неделе исследования. Подобного рода противоречия в одном из самых больших рандомизированных исследований холиновых препаратов при инсульте, наряду с результатами мета-анализов, показывают, что применение цитиколина обладает достаточно малым эффектом по улучшению исходов у пациентов с острым ишемическим инсультом – основной областью применения холиновых препаратов/БАДов. Противоречия необязательно указывают на низкое качество проведения исследований а, скорее, являются следствием пренебрежения стратификацией пациентов по уровням холина в крови и состояния холинового депо. Пренебрежение стратификационным анализом данных – одно из самых грубейших и наиболее часто встречающихся нарушений анализа результатов биомедицинских исследований [23]. Сравнительно малая величина наблюдаемого терапевтического эффекта, наряду с достаточно узким окном физиологического воздействия (ацетилхолин-зависимая нейротрансмиссия) и отсутствием стратификации данных, указывает на возможность того, что положительный эффект наблюдается только у незначительного числа пациентов исследованных выборок. Например, в мета-анализе 1 372 пациентов отношение шансов всего лишь 1,33 [20] при p = 0,003, что соответствует не более чем 33 % шансу улучшения по сравнению с группой плацебо. Проведённый нами анализ распределения c2 при p = 0,003 и других статистических параметров исследований, указанных в работе [20], подтверждает это предположение. Анализ данных проводился на основе делеционной методологии анализа медицинских данных [16]. Так, получение отношения шансов в 1,33 при p = 0,003 становится возможным уже при разнице в числе респондентов в 50 человек между группами контроля и пациентов, принимавших препарат. Принимая во внимание большой размер обеих групп (порядка 500-700 человек), становится очевидным, что позитивные эффекты холиновых препаратов наблюдаются не более чем у 10 % пациентов, принимавших препарат.
Препараты холина и персонализированная медицина Персонализированная медицина требует максимального принятия во внимание индивидуальных особенностей метаболизма конкретного пациента и, прежде всего, индивидуальную фармакокинетику и фармакогенетику конкретных фармпрепаратов. Персонализированный подход позволяет оценить баланс между эффективностью и побочными эффектами применения фармпрепаратов в каждом индивидуальном случае. Приведённый выше анализ биологических эффектов холина указывает на определённые ограничения связанные с применением холиновых препаратов у конкретных пациентов. Эффективность. Вышеупомянутый анализ испытаний холиновых препаратов показал, что эффекты холиновых препаратов наблюдаются не более чем у 10 % пациентов, принимавших препарат. Можно предположить, что это пациенты с глубоким дефицитом холина. Следовательно, препараты холина не будут эффективны у пациентов с нормальными уровнями холина (каковых большинство, включая, прежде всего, молодых гипертоников), даже при использовании высоких доз препаратов. Влияние холина на вазодилатацию неоднозначно. С одной стороны, исследования на культурах клеток человека показали увеличение окиси азота при обработке холином и ацетилхолином [10, 11]. Увеличенная концентрация NO соответствует вазодилатации. В то же время, в эксперименте были установлены вазоконстрикторный и гипертонический эффекты холиновых препаратов при внутрибрюшинном введении [17]. Антитромботический эффект холиновых препаратов наблюдается при очень высоких дозах (250 мг/кг в эксперименте) [12], что соответствует приёму 10-15 г/сут в случае взрослых пациентов. Подобного рода высокие дозы (превышают максимально допустимые в 4-5 раз), наряду с возможным гипертоническим эффектом, поднимают вопрос о безопасности применения холиновых препаратов (рис. 6). Холин необходим для синтеза ацетилхолина [24] и введение препаратов холина, особенно в гипердозах, может увеличивать системные уровни ацетилхолина. При назначении препаратов холина врач должен учитывать особенности индивидуальной фармакологии ацетилхолина. Классическая фармакология указывает на различные эффекты ацетилхолина на различные органы (см. табл. 2). Как иллюстрируют нижеследующие примеры, эти фармакологические данные могут эффективно использоваться в персонализированной медицине.
• Например, у пожилого пациента с брадикардией и достаточным потреблением холина дополнительное введение препаратов холина может вызвать дальнейшее замедление ритма. • У пациента с бронхиальной астмой и достаточным потреблением холина приём препаратов холина повышает риск бронхоспазма. • У пациента с каким-либо генетическим дефектом типа «медленный метаболизатор» в генах, обслуживающих метаболизм холина (см. табл. 3), избыточное введение препаратов холина будет приводить к повышенной нагрузке на элиминационную систему и появлению запаха разлагающейся рыбы у пациента. • У пациента с желчекаменной болезнью и наличием кальцифицированных желчных камней применение препаратов холина стимулирует тонус стенки желчного пузыря, желчевыводящих путей и может вызвать опасное движение желчных камней и непроходимость (обтурацию) желчных протоков.
Безопасность. По данным производителей, противопоказаниями к назначению холиновых препаратов являются ваготония, повышенная чувствительность к препарату, не рекомендуется применение у детей до 18 лет и в период беременности без оценки баланса риск-польза. При высоких дозах холина (такие как 2 000 мг/сут) чаще отмечались случаи головной боли [4]. Следует учитывать антиагрегатный эффект препаратов холина [12]. В частности, уменьшение агрегации эрироцитов, наблюдаемое при приёме холина, способствует понижению свёртываемости крови [11]. Поэтому, нельзя рекомендовать применение холиновых препаратов при геморрагическом инсульте (и в ранний период ишемического инсульта), когда тромболитики и дезагреганты могут принести больше вреда, чем пользы. Прогрессивные фирмы производители холиновых препаратов (Сомазина, производство Ferrer Internacional, Испания, https://www.ferrergrupo.com) указывают, что при персистирующем внутричерепном кровотечении рекомендуется вводить препарат в виде очень медленной в/в инфузии (30 капель/мин) и не превышать суточную дозу в 1000 мг. Избыток холина может приводить к «синдрому рыбного запаха» вследствие деградации холина в триметиламин. Рыбный запах триметиламина – признак интоксикации холином и неспособности элиминационных систем (печени, прежде всего) справится с избыточным поступлением холина. Интоксикация будет значительно усугубляться у пациентов с заболеваниями почек вследствие удлинения периода полувыведения, что следует принимать во внимание при персонализированном подходе к медицине. Как показывают и клинические, и фундаментальные исследования, препараты холина наиболее эффективны в достаточно высоких дозах (граммы). Одна из самых часто используемых форм холина, ЦДФ-холин (цитиколин и т. д.) является также значительным источником фосфора. Принимая во внимание избыток фосфора в питании россиян [25] вследствие избыточного потребления переработанных мясных продуктов (сосиски, колбасы и др.), большие дозы ЦДФ-холина будут только способствовать гиперфосфатемии и создавать дополнительную нагрузку на выводящие системы. Гиперфосфатемия способствует нарушению баланса макро- и микроэлементов (прежде всего, кальция и магния), длительная гиперфосфатемия способствует развитию онкологий. Высокие уровни фосфора также могут значительно ускорять образование камней в почках [26] и, возможно, в желчном пузыре [27].
Заключение Холин – основа для синтеза нейротрансмиттера ацетилхолина и одна из самых популярных биологически активных пищевых добавок. Препараты на основе производных холина продвигаются для лечения инсульта, в реанимации и акушерстве. Однако как доказательная, так и фундаментальная база по использованию холина и его производных не дают достаточного обоснования для настойчивого повсеместного навязывания в применения холиновых препаратов всем пациентам. В настоящей работе, мы рассмотрели спектр физиологических проявлений эффектов холина. С нейрохимической точки зрения, холин и препараты на его основе характеризуются однонаправленным воздействием (ацетилхолин-зависимая нейротрансмиссия). В общем случае, при инсульте происходит нарушение многочисленных путей нейротрансмиссии (ГАМК, глутамат, катехоламины, NO, нейропептиды, эндоканнабиноиды, эйкозаноиды и т. д.), не говоря уже о специфических нейротрофических факторах и интерлейкинах. Эффекты других нейротрансмиттеров проявляются в значительной степени независимо от ацетилхолина. Анализ данных по доказательной медицине указывает на высокую вероятность того, что препараты на основе холина имеют значительный эффект только у сравнительно небольшой пропорции пациентов (менее 10 % всех пациентов). Этими пациентами могут являться, например, имеющие генетические дефекты холинового метаболизма, характеризующиеся глубоким дефицитом холина, либо вследствие алкоголизма или неадекватного питания. Таким образом, назначение препаратов холина требует оценки врачом целесообразности применения препаратов этой группы у данного пациента и обоснованной оценки баланса «эффективность-безопасность». Фармакологическая нейропротекция – лишь часть комплексной программы восстановления пациента после инсульта. Наибольшая эффективность лекарственных препаратов проявляется именно в контексте комплексных программ, включающих двигательную реабилитацию, лечебную физкультуру, занятия с логопедом, плавание, массаж, программируемую электромиостимуляцию, коррекцию стереотипа ходьбы и т. д. Очень важна профилактика повторного инсульта, которая должна обязательно включать корректоры липидного профиля и коагуляции (аспирин, омега-3 ПНЖК, селен-содержащие, магний-содержащие препараты и антиатерогенную диету).
Литература 1. Громова О.А.,Гупало Е.М.,Торшин И.Ю. Церебролизин: анализ фундаментальных и клинических исследований. Методическое письмо для врачей. М.: 2008; РСЦ Института Микроэлементов ЮНЕСКО, 142. 2. Аткинс Р. Биодобавки доктора Аткинса, РИПОЛ Классик. М.: 1999; 81. М.: 2008; 33. 3. Методические рекомендации НИИ питания РАМН. Рекомендуемые нормы потребления пищевых и биологически активных веществ. Проект. 2008; МР 2.3.1.1915-04, 39. 4. Clark W.M., Warach S.J., Pettigrew L.C., Gammans R.E. et al. A randomized dose-response trial of citicoline in acute ischemic stroke patients. Citicoline Stroke Study Group // Neurology. 1997 Sep; 49: 3: 671-8. 5. da Costa K.A., Niculescu M.D., Craciunescu C.N., Fischer L.M., Zeisel S.H. Choline deficiency increases lymphocyte apoptosis and DNA damage in humans // Am J Clin Nutr. 2006 Jul; 84: 1: 88-94. 6. Jackowski S., Xu X.X., Rock C.O. Phosphatidylcholine signaling in response to CSF-1 // Mol Reprod Dev. 1997 Jan; 46: 1: 24-30. 7. Katzung, B.G. (2003). Basic and Clinical Pharmacology (9th ed.). McGraw-Hill Medical. ISBN 0-07-141092-9. 8. Харкевич Д.А. Фармакология. ГэотарМед, 2008; 113. 9. Hasselmo M.E. Neuromodulation and cortical function: modeling the physiological basis of behavior // Behav Brain Res. 1995; 67: 1: 1-27. 10. Carvalho F.A, Mesquita R., Martins-Silva J., Saldanha C. Acetylcholine and choline effects on erythrocyte nitrite and nitrate levels // J Appl Toxicol. 2004; 24: 6: 419-427. 11. Santos T., Mesquita R., Martins E. Silva J., Saldanha C. Effects of choline on hemorheological properties and NO metabolism of human erythrocytes // Clin Hemorheol Microcirc. 2003; 29: 1: 41-51. 12. Masi I., Giani E., Galli C. Effects of CDP-choline on platelet aggregation and the antiaggregatory activity of arterial wall in the rat // Pharmacol Res Commun. 1986; 18: 3: 273-281. 13. Ackerstaff E., Pflug B.R., Nelson J.B., Bhujwalla Z.M. Detection of increased choline compounds with proton nuclear magnetic resonance spectroscopy subsequent to malignant transformation of human prostatic epithelial cells // Cancer Res. 2001; 61: 9: 3599-3603. 14. Wurtman R.J. Stimulation of catecholamine secretion by choline // Science. 1983; 222: 4620: 188. 15. Holz R.W., Senter R.A. Choline stimulates nicotinic receptors on adrenal medullary chromaffin cells to induce catecholamine secretion // Science. 1981; 214: 4519: 466-468. 16. Torshin I.Yu. Bioinformatics in the post-genomic era: sensing the change from molecular genetics to personalized medicine. Nova Biomedical Books, NY, USA, 2009, In «Bioinformatics in the Post-Genomic Era» series, ISBN: 978-1-60692-217-0. 17. Cansev M., Yilmaz M.S., Ilcol Y.O., Hamurtekin E., Ulus I.H. Cardiovascular effects of CDP-choline and its metabolites: involvement of peripheral autonomic nervous system // Eur J Pharmacol. 2007; 577: 1-3: 129-42 Epub 2007 Au. 18. Fioravanti M., Yanagi M. Cytidinediphosphocholine (CDP-choline) for cognitive and behavioural disturbances associated with chronic cerebral disorders in the elderly // Cochrane Database Syst Rev. 2005; 2: CD000269. 19. Saver J.L. Citicoline: update on a promising and widely available agent for neuroprotection and neurorepair // Rev Neurol Dis. 2008; 5: 4: 167-177. 20. Davalos A., Castillo J., Alvarez-Sabin J., Secades J.J. et al. Oral citicoline in acute ischemic stroke: an individual patient data pooling analysis of clinical trials // Stroke. 2002; 33: 12: 2850-2857. 21. Warach S., Pettigrew L.C., Dashe J.F., Pullicino P. et al. Effect of citicoline on ischemic lesions as measured by diffusion-weighted magnetic resonance imaging // Citicoline 010 Investigators. Ann Neurol. 2000;48(5):713-722. 22. Tazaki Y., Sakai F., Otomo E., Kutsuzawa T. et al. Treatment of acute cerebral infarction with a choline precursor in a multicenter double-blind placebo-controlled study // Stroke. 1988; 19: 2: 211-216. 23. Torshin I.Yu. Bioinformatics in the post-genomic era: physiology and medicine. Nova Biomedical Books, NY, USA (2007), ISBN: 1600217524, 35-67. 24. Freeman J.J., Jenden D.J. The source of choline for acetylcholine synthesis in brain // Life Sci. 1976; 19: 7: 949-961. 25. Тутельян В.А., Спиричев В.Б., Суханов Б.П., Кудашева В.А. Микронутриенты в питании здорового и больного человека. М.: Колос, 2002; 423. 26. Guan X., Wang L., Dosen A., Tang R. et al. An understanding of renal stone development in a mixed oxalate-phosphate system // Langmuir. 2008; 24: 14: 7058-60. 27. Wolf P., Mannino F., Hofmann A.F., Nickoloff B., Edwards D.K. Calcium oxalate-phosphate gallstones, a unique chemical type of gallstone // Clin Chem. 1982; 28: 8: 1804-1805.
Где вырабатывается ацетилхолин?
Ацетилхолин вырабатывается в нервно-мышечных синапсах возле позвоночника. И вырабатывается он в ответ на движение, в ответ на стресс, и вообще практически постоянно. То есть если вы решили пошевелить пальцем, то по вашим нервным волокнам прошли сигналы. К примеру, сигнал прошел, от пальца до позвоночника (аксоны или отростки нервных клеток действительно иногда такие длинные). В ответ на это нервный синапс возле позвоночника выработал медиатор ацетилхолин, который заставил согнуться ваш палец.
Выводов из этого простого описания можно сделать много:
- Самый простой вывод — активные движения и работа повышают уровень ацетилхолина и мешают заснуть.
- Еще один вывод — ацетилхолин мобилизует организм. Поэтому если вам нужно выполнить важную работу, даже умственную, то вам помогут физические нагрузки.
- Интересно, что ацетилхолин вырабатывается не только тогда, когда вы сознательно решили подвигаться, но и у нервных и беспокойных особ. Чем тревожнее человек, тем выше у него уровень ацетилхолина.
- Если вы решили бросить курить, то занятия спортом сделают ваш процесс отвыкания быстрее, но ощутимее. То чем мы не пользуемся — атрофируется. И у курильщика ацетилхолина вырабатывается мало. Если вы будете много двигаться, то дадите большую нагрузку на эту систему.
Создание и разрушение ацетилхолина
Как повысить уровень ацетилхолина
Хотя ацетилхолин играет ключевую роль во многих аспектах вашего здоровья, нет никаких пищевых добавок, которые могли бы непосредственно повысить его уровень.
Тем не менее вы можете есть продукты или принимать пищевые добавки, которые косвенно увеличивают высвобождение ацетилхолина или препятствуют его расщеплению.
Один из самых простых способов поднять уровень ацетилхолина − это употреблять продукты или принимать пищевые добавки с высоким содержанием холина, важнейшего питательного вещества, которое можно преобразовать в ацетилхолин ().
Холин присутствует во многих продуктах, включая ():
- Говяжья печень: 85 грамм содержат 65% от рекомендованной суточной нормы потребления (РСНП).
- Яйца: 1 большое яйцо вкрутую содержит 27% от РСНП.
- Говядина: 85 грамм содержат 21% от РСНП.
- Соевые бобы, жареные: 85 грамм содержат 19% от РСНП.
- Жареная куриная грудка: 85 грамм содержат 13% от РСНП.
- Рыба, треска: 85 грамм содержат 13% от РСНП.
- Грибы шиитаке, приготовленные: 75 грамм содержат 11% от РСНП.
- Консервированная фасоль: 130 грамм содержат 8% от РСНП.
- Киноа, приготовленная: 185 грамм содержат 8% от РСНП.
- Молоко, 1%: 1 стакан (240 мл) содержит 8% от РСНП.
- Ванильный йогурт, обезжиренный: 1 чашка (245 грамм) содержит 7% от РСНП.
- Вареная брокколи: 80 грамм содержат 6% от РСНП.
- Брюссельская капуста, вареная: 80 грамм содержат 6% от РСНП.
К биологически активным добавкам, которые могут повышать уровень холина, относятся Alpha-GPC (L-альфа-глицерилфосфорилхолин), цитиколин (ЦДФ-холин) и битартрат холина.
Однако Alpha-GPC и цитиколин обычно содержат больше холина на единицу веса и легче усваиваются, чем другие формы (, ).
Еще одним способом косвенного повышения уровня ацетилхолина является прием добавок, которые ингибируют ферменты, расщепляющие ацетилхолин.
Вот некоторые добавки, которые могут ингибировать расщепление ацетилхолина (, , ):
- Гинкго билоба (гинкго)
- Бакопа Монье
- Гуперзин А
Однако неясно, насколько эффективны добавки, которые ингибируют расщепление ацетилхолина, в повышении уровня ацетилхолина по сравнению с добавками холина.
Резюме:
Ацетилхолин недоступен в качестве диетической добавки, но его уровни могут быть косвенно повышены за счет потребления холина, предшественника ацетилхолина, а также добавок, которые ингибируют расщепление ацетилхолина.
Жизненный цикл ацетилхолина
Объясним некоторые термины на предыдущей схеме:
Холинацетилаза — это фермент, который катализирует, то есть ускоряет и усиливает реакцию возникновения ацетилхолина. Создается он из двух веществ уксусной кислоты и холина. Выделить холинацетилазу в чистом виде ученым пока не удалось. О ее количестве можно судить по косвенным признакам: количеству ацетилхолина и скорости его накопления.
В выработке холиацетилазы очень важную роль играет витамин B1, который еще называют тиамином. Тиамин, как лекарственное средство, показано применять при его дефиците, иногда при беременности, при сердечной недостаточности, тяжелых болезнях печени и других нарушениях. Тиамин поддерживает процессы, связанные с работой инсулина и стимулирует выработку медиатора ацетилхолина.
Тиамин выпускается в форме раствора для инъекций и в форме таблеток в комбинации с другими витаминами группы B. Эти витамины показаны при неврологических нарушениях, физических повреждениях нервных тканей, алкоголизме, химических отравлениях и некоторых других состояниях.
Препарат с тиамином
M и N холинорецепторы. Рецепторы — это структуры которые ловят определенное вещество, в нашем случае медиатор ацетилхолин. Так часто бывает, что медиатор один, а рецепторов, на которые он воздействует, сразу несколько. Ацетилхолин воздействует на никотиновые и мускариновые рецепторы.
- Никотиновые рецепторы есть в скелетных мышцах и в вегетативных ганглиях. Агонист, то есть вещество, заменяющее в них ацетилхолин — это никотин. Полностью блокируются эти рецепторы смертельно опасным змеиным ядом курарином.
- Мускариновые рецепторы в большом количестве можно найти в гладких мышцах и в мозге. Подменить собой ацетилхолин в них может мускарин — яд мухоморов, белены и других пасленовых растений. А блокирует эти рецепторы ядовитый атропин.
Холинергический синапс[править | править код]
Источник:
«Наглядная фармакология»
.
Автор
: X. Люльман. Пер. с нем.
Изд.
: М.: Мир, 2008 г.
Ацетилхолин — Вячеслав Дубынин (д.б.н. МГУ им М.В. Ломоносова)
Ацетилхолин
(АХ) — медиатор в постганглионарных синапсах — накапливается в высокой концентрации в везикулах аксоплазмы нервного окончания. АХ образуется из холина и активированной уксусной кислоты (ацетилкофермент А) под действием фермента ацетилхолинтрансферазы. Высокополярный холин активно захватывается аксоплазмой. На мембране холинергического аксона и нервных окончаний имеется специальная транспортная система. Механизм высвобождения медиатора до конца не раскрыт. Везикулы закреплены в цитоскелете при помощи белка синапсина таким образом, что их концентрация около пресинаптической мембраны высокая, однако контакт с мембраной отсутствует. При возникновении возбуждения повышается концентрация Са2+ в аксоплазме, активируются протеинкиназы, и происходит фосфорилирование синапсина, приводящее к отсоединению везикул и связыванию их с пресинаптической мембраной. Затем содержимое везикул выбрасывается в синаптическую щель. Ацетилхолин мгновенно проходит сквозь синаптическую щель (молекула АХ имеет длину около 0,5 нм, а ширина щели составляет 30-40 нм). На постсинаптической мембране, т. е. мембране целевого органа, АХ взаимодействует с рецепторами. Эти рецепторы возбуждаются также алкалоидом мускарином и поэтому называются мускариновыми ацетилхолиновыми рецепторами (М-холинорецепторы). Никотин имитирует действие ацетилхолина на рецепторы ганглионарных синапсов и концевой пластинки. Никотин возбуждает холинорецепторы ганглионарных синапсов и концевой пластинки мотонейрона, поэтому этот тип рецепторов назван никотиновыми ацетилхолиновыми рецепторами (N-холинорецепторы).
В синаптической щели ацетилхолин быстро инактивируется специфической ацетилхолинэстеразой, находящейся в щели, а также менее специфической сывороточной холинэстеразой (бутирилхолинэстеразой), находящейся в сыворотке крови и интерстициальной жидкости.
По своему строению, способу передачи сигнала и сродству к различным лигандам М-холинорецепторы подразделяются на несколько типов. Рассмотрим M1, М2- и М3-рецепторы. M1-Рецепторы находятся на нервных клетках, например ганглиях, и их активация способствует переходу возбуждения с первого на второй нейрон. М2-Рецепторы расположены в сердце: открытие калиевых каналов приводит к замедлению диастолической деполяризации и уменьшению частоты сердечных сокращений. М3-Рецепторы играют роль в поддержании тонуса гладких мышц, например, кишечника и бронхов. Возбуждение этих рецепторов приводит к активации фосфолипазы С, деполяризации мембраны и повышению тонуса мышц. М3-Рецепторы расположены также в клетках желез, которые активируются посредством фосфолипазы С. В головном мозге имеются разные типы М-холинорецепторов, играющие роль во многих функциях: передаче возбуждения, памяти, обучаемости, болевой чувствительности, контроле активности ствола мозга. Активация М3-рецепторов в эндотелии сосудов может приводить к высвобождению оксида азота N0 и таким образом расширять сосуды.
Ацетилхолин и равновесие эмоций
Курильщики знают, что сигарета им нужна, чтобы успокоиться, чтобы взбодриться утром. Никотин помогает им думать над сложными задачами и наоборот начать активную физическую работу, при которой не нужно много думать. Такую же роль в организме человека выполняет и медиатор ацетилхолин.
Интересно, что помимо химических веществ, на выработку ацетилхолина влияют и гены. Кому то достались ферменты и синапсы, которые обеспечивают их большим количеством ацетилхолина. А у кого-то этого нейромедиатора относительно мало. Перекос и в ту, и в другую сторону — это не очень хорошо.
- При избытке ацетилхолина у человека отличная память и живой ум. Но при этом он не может быстро успокоиться, его мучит бессонница.
- При недостатке ацетилхолина человек спокойней и сдержанней. Но может показаться, что ему не хватает живости ума и быстроты реакции.
Уровень ацетилхолина зависит не только от генов. Свою роль играет образ жизни. Особенно физическая активность. Психологические установки, особенно тревожность и сильные стрессы, тоже играют свою важную роль.
Ацетилхолин выполняет такую же роль, как моторное масло в двигателе
Первый среди равных
Рисунок 1. Классический опыт Отто Лёви по выявлению химических посредников передачи нервных импульсов (1921 год). Объекты — изолированные и погруженные в солевой раствор сердцá двух лягушек (донора и реципиента). Описание приведено в тексте. .
Рисунок 2. Структурная формула ацетилхолина. .
Речь пойдет об ацетилхолине, и это будет символично, учитывая, что он был первым открытым нейромедиатором. В начале XX века между учеными велся спор, каким способом передается сигнал от одной нервной клетки на другую. Одни считали, что электрический заряд, пробежав по одному нервному волокну, передается на другое по каким-то более тонким «проводам». Их оппоненты утверждали, что существуют вещества, которые переносят сигнал от одной нервной клетки к другой. В принципе, обе стороны оказались правы: существуют химические и электрические синапсы. Однако сторонники второй гипотезы оказались «правее» — химические синапсы преобладают в организме человека.
* — О том, как сокращается наше сердце — об автоматизме, дирижирующих пейсмейкерах и даже смешных каналах, — читайте в обзоре «Метроном: как руководить разрядами?» . — Ред.
Рисунок 3. Ацетилхолиновая система мозга. Мы видим, что в глубоких отделах головного мозга находятся скопления нервных клеток (в переднем мозге и стволе), которые посылают свои отростки в различные отделы коры и подкорковых областей. В конечных пунктах из нейронных окончаний выделяется ацетилхолин. Местные эффекты нейромедиатора различаются в зависимости от типа рецептора и его расположения. MS — медиальное ядро перегородки, DB — диагональная связка Брока, nBM — базальное магноцеллюлярное ядро (ядро Мейтнера); PPT — педункулопонтийное тегментальное ядро, LDT — латеральное дорсальное тегментальное ядро (оба ядра — в ретикулярной формации ствола мозга). Рисунок из , адаптирован.
Рецепторы ацетилхолина делятся на две группы — и . Стимуляция мускариновых рецепторов приводит к изменению метаболизма в клетке через систему G-белков* (метаботропные рецепторы), а воздействие на никотиновые — к изменению мембранного потенциала (ионотропные рецепторы). Это происходит благодаря тому, что никотиновые рецепторы связаны с натриевыми каналами на поверхности клеток. Экспрессия рецепторов различается в разных участках нервной системы (рис. 4).
* — О пространственных структурах нескольких представителей громадного семейства GPCR-рецепторов — мембранных рецепторов, действующих через активацию G-белка, — доступно рассказано в статьях: «Рецепторы в активной форме» (об активной форме родопсина) , «Структуры рецепторов GPCR „в копилку“» (о дофаминовом и хемокиновом рецепторах) , «Рецептор медиатора настроения» (о двух серотониновых рецепторах) . — Ред.
Рисунок 4. Распределение мускариновых и никотиновых рецепторов в головном мозге человека. .
Ацетилхолин дофамин и болезнь Паркинсона
Медиатор ацетилхолин сложно рассматривать без его связей с другими медиаторами. Пример неправильного взаимодействия ацетилхолина и дофамина — симптомы болезни Паркинсона.
Болезнь Паркинсона — это неизлечимое в данный момент заболевание, которое проявляется преимущественно в пожилом возрасте. Хотя бывает и ранний паркинсонизм уже с 30 лет. Характерная черта таких больных — постоянное дрожание конечностей, сложности в координации движений. Даже сесть на стул или подняться по ступенькам для таких людей проблема.
Причина болезни Паркинсона истощение и отмирание клеток в мозге, которые вырабатывают медиатор дофамин. В результате возникают большие сложности с тем, чтобы отправить мышцам осознанный импульс, ослабляется контроль над телом. А вот активность медиатора ацетилхолина остается прежней. В результате возникает характерная для болезни Паркинсона дрожь.
Это состояние пытаются сгладить различными методами: блокируя синтез ацетилхолина или искусственно повышая уровень дофамина. Но все эти препараты серьезные и имеют много побочных эффектов. К примеру, активность ацетилхолина снижает циклодол, а дофамин повышает левадопа.
При болезни Альцгеймера, которая тоже бывает у стариков, ацетилхолина наоборот недостаточно. И для них используются повышающие ацетилхолин лекарственные средства. Эти препараты помогают бороться с деменцией и провалами в памяти у стариков.
Болезнь Паркинсона
Потенциальные полезные свойства ацетилхолина
Повышение уровня ацетилхолина было связано с несколькими потенциальными полезными эффектами в отношение здоровья.
Может помочь памяти и функции мозга
Исследования на животных и людях показывают, что более высокое потребление холина − предшественника ацетилхолина − может улучшить память у людей с проблемами с памятью.
В исследованиях на мышах пероральное введение холина в течение их жизни значительно улучшило память и уменьшило образование бета-амилоидных бляшек − соединения, связанного с развитием болезни Альцгеймера (, ).
Исследование, проведенное среди 2195 участников в возрасте 70–74 лет, показало, что у людей с более высоким уровнем холина в крови показатели памяти и обучения значительно выше, чем у людей с низким уровнем ().
Кроме того, добавки, которые ингибируют расщепление ацетилхолина, такие как бакопа монье, гинкго билоба и гуперзин A, были связаны с улучшением памяти и функции мозга (, , ).
Тем не менее исследование воздействия этих добавок на умственную деятельность является довольно новым. Прежде чем рекомендовать их для этой цели необходимы дополнительные исследования.
Может поддерживать психическое здоровье
Некоторые исследования показывают, что добавки-предшественники ацетилхолина могут помочь в лечении некоторых психических состояний.
Наблюдательное исследование с участием более 5900 участников показало, что низкие уровни холина в крови были связаны с более высоким риском возникновения тревоги. Тем не менее оно не нашло связи между уровнем холина в крови и депрессией ().
Другое исследование с участием 50 человек, страдающих депрессией, показало, что у людей, которые ежедневно в течение 6 недель принимали 200 мг цитиколина вместе с циталопрамом (лекарство от депрессии), имели менее тяжелые симптомы депрессии, чем те, кто принимал только лекарства от депрессии ().
Есть также некоторые свидетельства того, что бакопа монье и гинкго билоба могут помочь уменьшить симптомы тревоги, но необходимы дополнительные исследования на людях (, ).
Кроме того, добавки холина иногда используются для лечения симптомов у людей с биполярным расстройством. Однако исследования в этой области ограничены, и, прежде чем можно будет рекомендовать их для этой цели необходимы дополнительные исследования (, , , ).
Может поддержать здоровую беременность
Приблизительно 90–95% беременных женщин потребляют меньше холина, чем рекомендуемые суточные дозы ().
Существуют некоторые свидетельства того, что прием холина во время беременности может способствовать здоровому росту плода и улучшению его развития.
Одно исследование показало, что прием либо 480 мг, либо 930 мг холина в день в течение третьего триместра беременности значительно улучшил умственную функцию и память ребенка в 4, 7, 10 и 13 месяцев ().
Другое исследование, проведенное с участием 69 беременных женщин, которые употребляли много алкоголя, показало, что ежедневный прием 2 граммов холина с середины беременности до рождения значительно снижает воздействие алкоголя на психическую функцию ребенка ().
Несколько других исследований отметили, что более высокий уровень потребления холина во время беременности связан с более низким риском возникновения проблем с нервной трубкой у детей (, ).
Тем не менее другие исследования не обнаружили никакой связи между приемом холина матерью и развитием мозга плода или проблемами с нервной трубкой, поэтому необходимы дополнительные исследования (, ).
Другая потенциальная польза
Прием добавок холина, которые могут повысить уровень ацетилхолина, может принести также другую пользу при различных заболеваниях.
Однако связь между приемом холина и этими заболеваниями не совсем ясна, поэтому необходимы дополнительные исследования:
- Болезнь печени. Дефицит холина может вызвать заболевание печени, а более высокое потребление холина может быть связано с более низким риском заболеваний печени и рака печени (, , ).
- Болезнь сердца. Есть некоторые свидетельства того, что холин может снизить риск развития сердечно-сосудистых заболеваний и инсульта. Однако связь неясна, и другие исследования показывают смешанные результаты ().
Медиатор ацетилхолин и ВСД
Болезни, про которые мы писали выше, паркинсонизм и болезнь Альцгеймера малоизучены, и требуют дальнейших исследований. Еще одна загадочная болезнь, которая по нашему мнению связана с медиатором ацетилхолином — это ВСД или вегето-сосудистая дистония.
Диагноз ВСД терапевты ставят очень часто. По разным данным этим нарушением страдает от 25 до 70 процентов людей. Особенно часто ВСД возникает при гормональных перестройках у подростков или у женщин во время климакса.
Есть мнение, что ВСД — это болезнь, которая возникает из-за того, что у человека не совпадает «нужно» и «хочется». К примеру, вы едете в троллейбусе и сильно устали. Вы расслабляетесь на сиденье и почти засыпаете, но в следующую секунду вспоминаете, что на вас смотрят люди и заставляете себя встрепенуться. Так повторяется несколько раз. Баланс нейромедиаторов и тонус сосудов меняется. Это утомляет. В результате может возникнуть гипертония или наоборот упасть давление.
Ацетилхолин — важное звено вегетативной системы. По результатам недавних российских исследований стресс (который как считается основная причина ВСД) вызывает выброс большого количества ацетилхолина. Ацетилхолин считается нейромедиатором покоя, но после сильного возбуждения или стресса, его выбрасывается намного больше, чем обычно. Если компенсаторные системы не справляются и получается какой-то дисбаланс в вегетативной системе, то это приводит к известным симптомам ВСД. Впрочем, по поводу медиатора ацетилхолина и связей между вегетативной и нервной системой сейчас больше вопросов, чем ответов.
Возможно, вас заинтересуют другие статьи на нашем сайте о гормонах и нейромедиаторах:
- Что такое дофамин?
- 5 гормонов радости, счастья и удовольствия.
- Высокий и низкий эстроген у женщин.
- Окситоцин гормон привязанности и беременности.
- Адреналин медиатор и медицинский препарат.
Риски и побочные эффекты
Что случится, если у ацетилхолина будет слишком много? Обычно с едой сложно получить слишком большое количество холина (из которого потом выработается ацетилхолин), но вы можете получить передозировку из добавок холина.
Максимально допустимой безопасной суточной дозировкой холина считается 3500 мг. Поэтому во избежание побочных эффектов держитесь ниже этого уровня.
Прием высоких доз холина может привести к выработке слишком большого количества ацетилхолина. В больших количествах добавки могут вызвать пониженное кровяное давление, потливость, рыбий запах тела и повышенное слюноотделение.
Заключение
Что такое ацетилхолин? Это нейротрансмиттер, который передает сигналы между клетками мозга и важен для памяти и других функций мозга.
Другие функции ацетилхолина включают в себя поддержку движения мышц, внимания, обучения, возбуждения, мотивации и быстрого сна.
Дисфункции ацетилхолина и его дефицит был связан с когнитивным спадом, ухудшением памяти и некоторыми расстройствами мозга, такими как болезнь Альцгеймера.
Для поддержания адекватного уровня ацетилхолина в организме рекомендуется включить в свой рацион продукты, богатые холином – яйца, бобовые, индейку. Также для повышения когнитивных функций с помощью ацетилхолина вы можете принимать добавки холина в кратковременном режиме, не превышая рекомендуемую дозировку.