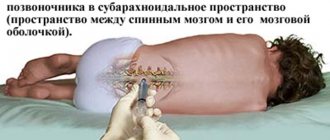
Современная мировая неврология достигла значительного прогресса в лечении рассеянного склероза. Если еще 10 — 15 лет назад прогноз этого хронического заболевания часто бывал неутешительным, и дело заканчивалось инвалидностью и смертью, то сегодня этого сценария все чаще удается избежать.
Наш эксперт в этой сфере:
Лащ Наталия Юрьевна
Врач-невролог высшей категории, к.м.н., доцент. Лауреат Премии города Москвы в области медицины.
Позвонить врачу Отзывы о докторе
Это не значит вылечить рассеянный склероз полностью. Но это значит сохранить человеку способность к полноценной жизни, избежать потери трудоспособности. Это значит достичь устойчивой, длительной ремиссии, предотвратить обострения или сделать их редкими, минимизировать симптомы и остаточные явления.
Рассеянный склероз имеет три основные формы: ремитирующую, вторично прогрессирующую и первично прогрессирующую.
Ремитирующая форма означает появление первичных симптомов, которые относительно быстро проходят, после чего наступает ремиссия. При этом происходит полное восстановление, остаточные явления отсутствуют. Такое благополучное состояние может продлиться несколько лет. После этого происходит рецидив, и отныне обострения становятся регулярными. Они происходят все чаще и их форма становится все более тяжелой. Это значит, что заболевание приняло вторично прогрессирующую форму.
После каждого обострения сохраняются остаточные явления — мышечная слабость, онемение, паралич, снижение умственной работоспособности, ухудшение когнитивных способностей, памяти.
Человек постепенно утрачивает способность самостоятельно передвигаться. Сначала он вынужден опираться при ходьбе на трость, затем перемещается в инвалидную коляску. Такое развитие заболевания является наиболее типичным.
Первично прогрессирующая форма означает отсутствие обострений и ремиссий. Заболевание развивается непрерывно, неврологические симптомы все более нарастают. Каждый из вновь появившихся симптомов уже не исчезает, а остается навсегда и только усугубляется со временем.
Новейшие методики лечения рассеянного склероза, которые мы используем, дают хорошие результаты при всех трех формах заболевания. При ремитирующей форме они помогают максимально продлить ремиссию, предотвратить наступление вторично прогрессирующей стадии или сделать ее менее опасной. Это значит избежать инвалидизации.
В случае первично прогрессирующей формы заболевания наши методики помогают замедлить развитие заболевания и также избежать инвалидности.
Наши методики
Что же это за новые методики, которые мы предлагаем сегодня в нашем медицинском центре?
Во-первых, это новейшие препараты, изменяющие течение рассеянного склероза (ПИТРС). За последние десятилетия появились лекарственные средства, значительно превосходящие по эффективности все то, что применялось прежде. Каждый год проходят клинические исследования и внедряются в практику все новые ПИТРС. Мы внимательно отслеживаем этот процесс и используем все лучшие разработки, доказавшие свои преимущества.
Во-вторых, это методика предварительного очищения крови, которая значительно повышает результаты медикаментозной терапии.
В-третьих, это метод диагностики, который показывает наступление рецидива до появления его симптомов. Это позволяет принять превентивные меры и избежать обострения или максимально облегчить его с тем, чтобы избежать осложнений, остаточных явлений и их накопления, а в конечном итоге инвалидности, и сохранить нашему пациенту полноценную физическую и умственную активность.
Традиционные способы лечения рассеянного склероза
К сожалению, до недавнего времени рассеянный склероз относился к числу неизлечимых заболеваний. Традиционные методики были направлены на облегчение симптомов болезни, они могли замедлить ее развитие и отдалить по времени наступление нового рецидива. Лекарственные препараты – например, интерферон, копаксон или иммуносупрессоры – подавляли иммунный ответ, тормозили процесс демиелинизации, но не восстанавливали уже имеющееся повреждение нервных волокон. Иными словами, они были бессильны вернуть пациенту утраченные функции.
Пульс-терапия
Для купирования острых симптомов рассеянного склероза в международной клинике Медика24 применяется пульс-терапия — медленное внутривенное введение гормонального препарата — 6-метилпреднизолона.
Этот глюкокортикоидный препарат оказывает мощное и быстрое противовоспалительное, мембраностабилизирующее, противоотечное действие и помогает существенно улучшить состояние больного в течение 3 — 7 дней.
Перед назначением курса пульс-терапии в нашей клинике проводится обследование, чтобы исключить противопоказания.
В частности, выполняется гастродуоденоскопия, чтобы исключить язву желудка и 12-перстной кишки. Должны быть исключены и другие противопоказания — инфекционные заболевания, декомпенсированный сахарный диабет, туберкулез.
Главное преимущество пульс-терапии состоит в ее исключительной эффективности. Ее результаты существенно превосходят возможности перорального применения гормональных или иных препаратов.
Уже за 3 — 7 дней достигается значительное улучшение состояния — проходят онемение и слабость в руках и ногах, улучшается зрение, проходят головокружения, нарушения координации, шаткость при ходьбе и другие симптомы, связанные с поражением спинного мозга, мозжечка, ствола головного мозга.
Острые симптомы исчезают, развитие заболевания замедляется, наступает улучшение состояния (регрессия симптомов).
Введение препарата 6-метилпреднизолона выполняется внутривенно посредством капельницы. Протоколы лечения соответствуют наиболее эффективным схемам, результаты которых были объективно подтверждены клиническими исследованиями и сегодня считаются «золотым стандартом» пульс-терапии при рассеянном склерозе. При этом учитываются индивидуальные особенности пациента.
Пульс-терапия в международной клинике Медика24 назначается на основе данных МРТ с контрастированием (для выявления активных очагов демиелинизации), а также оценки состояния больного при появлении новых или обострении прежних симптомов.
Врачи нашей клиники имеют большой опыт проведения этого вида лечения и своевременной коррекции побочных эффектов.
Лечебный курс рекомендуется проводить в условиях стационара. Это гарантирует максимальную безопасность и лучшую эффективность пульс-терапии.
Внутривенное введение гормонального препарата оказывает мощное терапевтическое действие, но наряду с этим возникают побочные эффекты.
Одни из них относительно незначительны — головокружение, эйфория, икота, тошнота, бессонница, тревожность.
Другие могут быть более серьезны — скачки артериального давления, кровотечение, гипергликемия, сердечная аритмия.
Чтобы своевременно купировать эти побочные эффекты, скорректировать лечебный курс, пациенту лучше находиться в стационаре, под врачебным наблюдением.
Закажите обратный звонок. Мы работаем круглосуточно
Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Этапы лечения с помощью трансплантации стволовых клеток
Шаг первый – Подготовка стволовых клеток. В первую очередь, донор предоставляет врачам полную историю своей болезни. Кроме того, у пациента берут анализы, такие как химия крови, серология для инфекций, определяется группа крови, резус-фактор, делается кардиограмма, визуализация и спирография. Также обязательна поясничная пункция и МРТ с контрастом и без него. Затем из периферической крови извлекают гемопоэтические стволовые клетки посредством подкожных инъекций. Этого может быть достаточно для трансплантации стволовых клеток больному рассеянным склерозом.
Если же этот метод оказывается не эффективным, в этом случае стволовые клетки собирают из костного мозга тазовой кости (подвздошный гребень). Это не сложная операция, которую делают под местной анестезией, реже — общим наркозом.
Шаг второй – Трансплантация стволовых клеток при рассеянном склерозе. Перед тем, как пересадить здоровые клетки, больной рассеянным склерозом проходит так называемую процедуру кондиционирования, которая подавляет иммунную систему, чтобы она не отторгла новые стволовые клетки. По сути, это химиотерапия. Безусловно, это риск, поскольку иммунитет фактически разрушается, человек становится очень чувствительным к любым инфекциям, даже легкая простуда может привести к летальному исходу. Поэтому пациент находится в стационаре, в специальной стерильной палате. Но период при лечении рассеянного склероза недолгий – всего неделя.
После чего, происходит непосредственно трансплантация. Здоровые клетки, посредством инъекций вводятся больному. Дальше самое сложное – ожидание. Состояние рецепиента ежедневно контролируется: регулярно берут кровь для анализов, проверяют как растут новые стволовые клетки и восстанавливается иммунитет. Чаще всего, на то, чтобы результаты анализов пришли в норму, уходит от 10 до 14 дней. Когда это происходит – пациента выписывают.
Шаг третий – Лечение рассеянного склероза и укрепление иммунитета. После выписки, пациент обязательно проходит курс лечения, направленный на укрепление иммунитета, а также на профилактику воспалительных процессов. Один раз в три-четыре дня необходимо посещать врача и сдавать анализ крови, для контроля за общим состоянием больного. Средняя длительность такого лечения – до двух месяцев. По прошествии этого времени и в зависимости от результатов анализов, врач назначает даты контрольных исследований по поводу рассеянного склероза.
Сделайте заявку на лечение
Нажимая эту кнопку, вы получаете быстрый отклик и индивидуальное решение от врача
Особенности диагностики
Рассеянный склероз — это заболевание, при котором активные клетки иммунной системы атакуют и разрушают миелиновую оболочку нервов. В развитии этого аутоиммунного заболевания может сыграть свою роль наследственный фактор, интоксикации, образ жизни, нервные стрессы, перенесенные острые вирусные или бактериальные инфекции. По той или иной причине иммунная система начинает вести себя агрессивно по отношению к собственным клеткам организма.
Рассеянный склероз поражает белое вещество мозга. В отличие от серого вещества, образуемого нейронами, оно состоит из аксонов. Эти отростки служат проводниками нервных сигналов. Самые короткие из них всего несколько миллиметров длиной, самые длинные — до полутора и более метров. Подобно проводам, по которым течет электрический ток, аксоны имеют внешнюю изоляцию.
Такую же внешнюю изоляцию имеют пучки нервных волокон, двигательные и чувствительные. Первые отвечают за мышечные сокращения, вторые — за восприятие зрительных, слуховых, обонятельных, вкусовых, тактильных ощущений. Изоляционная оболочка аксонов и нервов состоит из миелина — сложного белково-липидного вещества.
При развитии аутоиммунного процесса агрессивные клетки иммунной системы атакуют миелин и разрушают его. Возникают области оголения аксонов и нервов, на месте которых образуются бляшки. Из-за этого резко (в 5 — 10 раз) снижается скорость передачи нервных сигналов. Одновременно развивается воспалительный процесс и интоксикация, что приводит к гибели нервных тканей. Из-за этого развиваются необратимые изменения, которые в итоге приводят к инвалидности и смерти.
Процесс образования уплотнений, бляшек называется склерозированием. Эти бляшки образуются в большом множестве и рассеяны по центральной нервной системе — в головном и спинном мозге. Отсюда название заболевания — рассеянный склероз.
Замедление прохождения нервных сигналов и разрушение нервной ткани проявляется симптомами, которые обычно начинаются с ног. Организм, пораженный заболеванием, можно образно сравнить с деревом, у которого начинает умирать листва, отмирать ветви. В то время, когда нижние уже погибли, верхние выглядят вполне здоровыми. Но это вопрос времени. Если заболевание начало свое развитие, оно будет распространяться все выше и выше.
Сначала человек ощущает слабость и онемение в ступнях, затем в голенях, в бедрах. Возможны ощущения покалывания, жжения, ползания мурашек. Все это признаки нарушения иннервации, которые легко можно принять за проявление заболевания позвоночника, например, протрузии или грыжи.
Дело осложняется тем, что в последние десятилетия дегенеративно-дистрофические заболевания позвоночника стали широко распространены. Врач назначает МРТ, которая действительно показывает наличие проблемы, например, в поясничном отделе. Это вполне очевидное и простое объяснение симптомов, на основе которого врач назначает лечение. Это может быть операция по удалению диска, которая не дает никакого эффекта. Симптомы сохраняются, потому что их причина — рассеянный склероз. Хорошо если заболевание будет диагностировано хотя бы после первой безуспешной операции.
Слабость в ногах нарастает, но теперь уже в процесс вовлекается мочеполовая, выделительная системы. Нарушаются нормальные процессы дефекации, мочеиспускания, они происходят неконтролируемо. Слабость и онемение распространяется на руки, становится трудно удерживать предметы, совершать обычные движения, обслуживать себя в быту. Продвигаясь вверх, болезнь может привести к параличу дыхательной системы, сердца. Человек оказывается в отделении реанимации, под аппаратом ИВЛ.
Бывают случаи, когда врачи, не сумев обнаружить рассеянный склероз, вместо этого рекомендуют лечить, например, синдром хронической усталости. Ведь центральная нервная система — это не только сокращения мышц, но и психическая деятельность. В зависимости от того, какие нервы попали под удар иммунной системы, возникают те или иные начальные симптомы заболевания. Это может быть ощущение постоянной усталости, снижение памяти, внимания, концентрации, умственной работоспособности, повышенная утомляемость, слабость. Появляется забывчивость, рассеянность, которые сопровождаются депрессией или нарастающей апатией. Сон становится прерывистым, беспокойным, сопровождается частыми пробуждениями, ночными кошмарами, развивается бессонница. Все это можно принять за признаки астено-невротического синдрома, или синдрома хронической усталости. Назначаются психотропные препараты, ноотропные средства, которые не дают практически никакого результата. Болезнь продолжает прогрессировать.
Среди ранних симптомов может быть также нарушение зрения, слуха, нарушение координации движений, шаткость походки. Такая множественная картина зачастую приводит к тому, что человек ходит от врача к врачу, и каждый назначает ему новое лечение, консервативное или хирургическое.
Между тем достаточно сделать относительно простое обследование, чтобы установить истинную причину симптомов — рассеянный склероз. Основанием для постановки диагноза служат данные МРТ головного мозга. Магнитно-резонансная томография не только показывает очаги демиелинизации (бляшки), но и позволяет отличить новые, молодые от старых. Используя контрастное вещество, врач может увидеть свежие разрушения миелиновой оболочки нервов, а также очаги воспаления и некроза нервной ткани.
Для оценки скорости прохождения нервных сигналов используется электронейромиография. Обследование с постановкой диагноза занимает всего один день.
Еще один важный диагностический показатель — анализ крови на антитела к миелину. Рассеянный склероз — аутоиммунное заболевание. По содержанию специфических антител, агрессивных к миелиновым антигенам, можно получить достоверную информацию о стадии развития заболевания, степени его опасности. Этот же показатель помогает предвидеть скорое наступление обострения вторично прогрессирующей формы заболевания.
Общая иммунограмма позволяет оценить состояние иммунной системы в целом и степень ее изменений на фоне рассеянного склероза.
Мы вам перезвоним
Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Диагностика рассеянного склероза
Невропатолог проводит тщательный осмотр, собирает данные о времени проявления первых симптомов, проверяет рефлексы. Для постановки точного диагноза и последующего лечения рассеянного склероза нужна КТ, МРТ головного и спинного мозга, иммунограмма.
Диагноз «рассеянный склероз» в наше время перестал быть синонимом слова «безнадежность»! Эффективное и безопасное лечение существует!
Чтобы получить консультацию по лечению рассеянного склероза в Москве, позвоните по телефону оформите заявку обратный звонок
Особенности лечения
Стандартное средство лечения — препараты, которые корректируют работу иммунной системы, снижают ее агрессивность, подавляют провоспалительные факторы. Они называются ПИТРС — препараты, изменяющие течение рассеянного склероза. Эффективность такого лечения может быть высокой или низкой. Кому-то они помогают, кому-то нет или почти не помогают. В этом случае врач меняет препараты, корректирует терапию.
Эффективность медикаментозного лечения зависит от двух факторов. Первое — это сами препараты. Зачастую в нашей стране используются те же самые средства, которые назначались еще пятьдесят лет назад. В то время как в мировой неврологической практике используются намного более действенные ПИТРС. Это связано с тем, что достижения мировой фармакологии не всегда должным образом отслеживаются, препараты внедряются в практику с запозданием. Для многих пациентов это означает неблагоприятный прогноз заболевания.
Мы стараемся не допускать этой ошибки и своевременно используем все лучшие, самые последние, инновационные мировые разработки, используем европейские протоколы лечения. Медикаментозный курс назначается и корректируется индивидуально. В совместном ведении пациента участвуют неврологи, иммунологи, врачи других специальностей. Междисциплинарный подход помогает подобрать оптимальные препараты и, как следствие, достичь устойчивой, длительной ремиссии, устранить симптомы и позволить человеку продолжать нормальную, здоровую жизнь.
Второй фактор — это та принципиальная особенность, которая отличает лечение рассеянного склероза в нашей клинике. На него мало кто или почти никто не обращает внимание, а зря.
Дело в том, что назначая те или иные препараты, врачи почти никогда не придают значения важнейшему обстоятельству — в какую кровь попадает действующее вещество.
А ведь кровь при рассеянном склерозе до крайности загрязнена. Она насыщена продуктами распада миелиновой оболочки. Она содержит высокую концентрацию антител, разрушающих и уже разрушивших миелин. Это очень неблагоприятная среда, которая заведомо снижает эффективность лекарственного препарата или вовсе сводит ее к нулю.
Но достаточно убрать все эти загрязнения, очистить кровь, и эффективность препарата существенно возрастает, порой многократно. Это дает возможность получить совершенно иные результаты терапии.
Можно сравнить это с простейшим примером. Если для лечения насморка применять препарат при заложенных носовых ходах, скоплении в них слизи, его эффективность может быть невысокой. Но стоит прочистить, хорошенько промыть носовые ходы, и уже после этого применить лечение, его результаты будут совсем иными.
Поэтому прежде чем начать курс медикаментозной терапии ПИТРС, мы очищаем кровь пациента с помощью плазмафереза. Эта процедура состоит в том, что кровь разделяется на эритроцитарную массу и плазму, содержащую загрязнения — антитела и продукты распада миелина. После этого грязная плазма крови удаляется и заменяется чистой.
После этого, уже в очищенную кровь, поступает действующий препарат (ПИТРС). Практика нашей клиники показывает, что такая последовательность действий позволяет достичь устойчивой ремиссии и восстановить здоровье даже в тех случаях, когда простая медикаментозная терапия не давала практически никаких результатов.
В тяжелых случаях требуется стационарное лечение, но зачастую для достижения положительных результатов бывает достаточно амбулаторного лечения и процедур, проводимых в условиях дневного стационара нашей клиники.
Результаты
У всех 79 больных со сроком наблюдения ≥9 месяцев отмечено клиническое улучшение или стабилизация в течении заболевания. Во время проведения трансплантации не было зарегистрировано ни одного смертельного исхода и тяжелых неконтролируемых побочных эффектов. Через 6 месяцев после трансплантации распределение пациентов согласно клиническому ответу было следующим: улучшение – 42 (53%) больных, стабилизация – 37 (47%) больных. Среди больных с улучшением у 20 было вторично-прогрессирующее течение, у 7 – первично-прогрессирующее, у 4 – прогрессирующе-рецидивирующее и у 11 – рецидивирующе-ремиттирующее течение. В этой группе 25 больных проведена этапная трансплантация, 15 – ранняя и 2 – трансплантация спасения. Из 37 больных, у которых зарегистрирована стабилизация заболевания, у 19 было вторично-прогрессирующее течение, у 8 – первично-прогрессирующее, у 2 – прогрессирующе-рецидивирующее и у 8 – рецидивирующе-ремиттирующее течение. В этой группе 23 больным проведена этапная трансплантация, 9 – ранняя и 5 – трансплантация спасения.
В более длительные сроки наблюдения у 40 больных (50.6%) сохранялось улучшение, у 34 (43.1%) – стабилизация. У одного больного после 6 месяцев и двух больных после 18 месяцев стабилизации произошло повышение индекса инвалидизации. У двух пациентов прогрессирование заболевания наступило после 12 и 30 месяцев клинического улучшения. По данным МРТ у всех больных без прогрессирования заболевания после трансплантации отсутствовали активные или новые очаги поражения. В целом, 6-летняя выживаемость без прогрессии после ВДТ+АуТКСК составила 72%. Больные, у которых не было зарегистрировано признаков прогрессирования заболевания, не получали иммуномодулирующую или иммуносупрессивную терапию после трансплантации. Мониторинг качества жизни проводился у 44 пациентов, включенных в исследование. У 40 из них наблюдали улучшение показателей качества жизни через 6 месяцев после трансплантации. Улучшение параметров качества жизни установлено с помощью опросников – FACT-BMT и FAMS. Через 1 год после ВДТ+АуТКСК зарегистрировано следующее распределение пациентов в соответствии со степенью ответа, связанного с качеством жизни: у 3 больных наблюдали максимальный ответ (более чем 75% улучшение интегрального показателя качества жизни в сравнении с исходным уровнем); у 12 больных – хороший ответ (улучшение на 50-75%); у 11 больных – умеренный ответ (на 25-50%); у 13 – минимальный ответ (улучшение менее чем на 25%) и у 5 больных ответ, связанный с качеством жизни, отсутствовал. Следует отметить, что у пациентов с более длительным сроком наблюдения было отмечено дальнейшее улучшение показателей качества жизни. В статье представлена классификация типов трансплантации при рассеянном склерозе, основанная на концепции ВДТ+ТКСК при аутоиммунных заболеваниях.
Контроль состояния
Еще одна особенность нашего подхода к лечению рассеянного склероза — это контроль состояния. Регулярные анализы позволяют вовремя предвидеть и предотвратить обострение заболевания, захватить его на той стадии, когда оно еще не успело привести к необратимым последствиям.
Это значит, что человек продолжает жить здоровой, нормальной, полноценной жизнью, время от времени контролируя свое состояние. Для этого достаточно раз в три месяца делать анализ крови на наличие антител к миелину.
Казалось бы, все просто. Но удивительно, что такой эффективный метод практикуется относительно редко, лечение обычно начинается уже после появления симптомов обострения. А ведь его можно избежать. Оно никогда не возникает вдруг и мгновенно. Ему предшествует повышение показателей специфических антител в крови. Достаточно регулярного мониторинга этих показателей, чтобы полностью контролировать состояние человека.
На практике это означает, что человек прошел курс медикаментозной терапии, в результате которой была достигнута ремиссия. Симптомы исчезли, и человек продолжает жить нормальной жизнью. Время от времени он приходит в наш центр и делает анализ крови на антитела.
Длительное время они могут оставаться на низком уровне. Это значит, что здоровью ничто не угрожает. Но вдруг очередной анализ показывает существенное повышение уровня антител. Это значит, что если не принять меры, в скором времени наступит обострение.
Предупрежден — значит, вооружен. Мы принимаем превентивные меры, и обострения удается избежать. Это может быть плазмаферез или его сочетание с медикаментозной терапией, все зависит от индивидуального случая.
Записаться на прием к врачу
Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Центр трансплантации костного мозга
Что такое костный мозг и гемопоэтические стволовые клетки? Костный мозг представляет собой мягкую, губкоподобную ткань, расположенную внутри кости. Он содержит клетки, называемые гемопоэтическими или кроветворными стволовыми клетками. Гемопоэтические клетки могут делиться, чтобы образовывать больше кроветворных стволовых клеток или развиваться для создания «красных кровяных клеток – эритроцитов», «белых кровяных клеток – лейкоцитов» и «тромбоцитов». Большинство гемопоэтических стволовых клеток (ГСК) находятся в костном мозге, однако небольшое их количество также имеется в пуповинной и периферической крови. Для трансплантации могут быть использованы клетки, полученные из любого вышеупомянутого источника ГКС.
Что такое пересадка костного мозга? Пересадка костного мозга и трансплантация периферических стволовых клеток крови – это лечение с использованием высоких доз химиотерапии и/или лучевой терапии для угнетения поврежденных ГСК с дальнейшим их замещением на здоровые (донорские или собственные) ГСК.
Есть три типа пересадки: Аутотрансплантация: Пересадка собственных стволовых клеток пациента. Сингенная трансплантация: Пересадка путем получения стволовых клеток от однояйцевых близнецов Аллогенная трансплантация: Пересадка путем получения стволовых клеток от братьев и сестер или родителей. Неродственный донор также может быть использован в случае совместимости.
Как происходит пересадка костного мозга? При трансплантации собственных клеток костного мозга требуется радикальная терапия основного заболевания. Поэтому пациент получает терапию в соответствии с назначениями врача. До начала радикальной терапии проводится сбор и заморозка стволовых клеток пациента. После сбора стволовых клеток пациент получает высокодознуювысокоинтенсивную терапию. В среднем, длительность такого курса радикальной терапии составляет около недели. После окончания высокодозной терапии пациенту вводят ранее собранные здоровые стволовые клетки. Данный метод позволяет инициировать самовосстановление стволовых клеток, поврежденных во время терапии.
Существуют ли какие-либо риски, связанные с аутотрансплантацией? Процедура сбора стволовых клеток от пациента связана с риском возможного попадания патологических клеток в материал трансплантата. Другими словами, повторное введение замороженных стволовых клеток пациента может вызвать рецидив болезни из-за патологических клеток.
Существуют ли какие-либо риски, связанные с аллогенной трансплантацией? При аллогенной пересадке пациент также получает часть иммунной системы донора. Это является преимуществом метода. Однако аллогенная трансплантация связана с риском несовместимости иммунных систем. Это может привести к реакции иммунной системы донора с органами реципиента стволовых клеток. Существует риск повреждений печени, кожи, костного мозга и кишечника. Это называется реакцией «трансплантат против хозяина» (РТПХ). Такие риски при аутотрансплантации отсутствуют.
Как стволовые клетки донора совмещаются со стволовыми клетками пациента при аллогенной и сингенной трансплантации? Врачи в основном, используют трансплантационные стволовые клетки, которые как можно более схожи со стволовыми клетками пациента. Для того, чтобы свести к минимуму потенциальные побочные эффекты, анализируется совместимость донора и хозяина. На поверхности практически всех клеток человека представлены белковые нити, называемые человеческим лейкоцитарным антигеном (HLA-антиген). Эти белковые нити определяются с помощью анализа крови на HLA-антиген типирование. В большинстве случаев успех аллогенной трансплантации основан на степени совместимости HLA антигенов в стволовых клетках донора и реципиента. Шанс принятия донорских стволовых клеток организмом реципиента увеличивается по мере увеличения количества совместимых HLA-антигенов. В общих чертах, высокая степень совместимости между стволовыми клетками донора и стволовыми клетками реципиента минимизирует риск развития осложнения, известного как реакция «трансплантат против хозяина» (РТПХ). Шанс для близких родственников (особенно братьев и сестер) быть HLA-антиген-совместимыми выше, чем у не-родственников. Однако только около 25 – 35% пациентов имеет HLA-антиген-совместимого брата/сестру. Вероятность найти HLA-антиген-совместимые стволовые клетки у неродственного донора немного выше – до 50%. Совместимость HLA-антигенов среди неродственных доноров значительно повышается, когда донор и хозяин имеют одинаковое этническое и расовое происхождение. Несмотря на то, что количество доноров демонстрирует тенденцию к увеличению, некоторым людям из определенных этнических и расовых групп сложно найти подходящего донора. База универсальных добровольных доноров может помочь в поиске совместимого неродственного донора. Однояйцевые близнецы имеют одинаковые гены, следовательно, они имеют одинаковые нити HLA-антигена. В таких случаях пациент принимает пересадочный материал от своего близнеца. Однако количество таких близнецов не так уж велико, что делает сингенные трансплантации редким явлением.
Как происходит сбор костного мозга для трансплантации? Стволовые клетки, используемые для трансплантации костного мозга, получают из жидкой сердцевины, называемой «мозговое вещество». В общих чертах, процедура сбора костного мозга, обычно называемая «сбор урожая», мало различается для всех трех типов трансплантации костного мозга (аутологичных, аллогенных, сингенных). Во время процедуры донор получает седативный общий наркоз либо местную анестезию в результате чего происходит онемение ниже пояса. Иглы для экстракции вставляются в костный мозг тазовой кости. Сбор костного мозга занимает около часа. Собранный костный мозг обрабатывают, чтобы удалить следы кости и крови. В собранный костный мозг может быть добавлен консервант, затем его замораживают, чтобы сохранить стволовые клетки до востребования. Этот метод известен как криоконсервация. С помощью криоконсервации стволовые клетки могут храниться в течение нескольких лет.
Как получают стволовые клетки периферической крови? Стволовые клетки, используемые для трансплантации стволовых клеток периферической крови, получают из донорской крови. Стволовые клетки периферической крови для трансплантации получают с помощью процедуры, называемой аферез или лейкаферез. Донор принимает специальные препараты в течение 4 или 5 дней до афереза, чтобы увеличить количество стволовых клеток в кровотоке. Кровь для афереза собирают из большой вены руки или с помощью центрального венозного катетера (гибкая трубка, помещенная в широкую вену в области шеи, груди или таза). Аферез обычно занимает от 4 до 6 часов. Кровь прокачивают через прибор, который собирает стволовые клетки. Затем кровь вводят обратно донору, а собранные стволовые клетки сохраняют. Стволовые клетки замораживают до момента пересадки хозяину.
Существуют ли риски, связанные со сбором костного мозга? Вообще, сбор костного мозга у донора не вызывает проблем, поскольку количество извлеченного вещества очень мало. Большинство рисков, связанных со сбором костного мозга – это возможные осложнения, относящиеся к использованию анестетиков во время процедуры. В области сбора костного мозга в течение нескольких дней может ощущаться припухлость и затвердение. В течение этого периода донор может ощущать усталость. Организм донора восполнит утраченный костный мозг в течение нескольких недель, однако время, необходимое для полного восстановления донора, различно. В то время как некоторые люди могут вернуться к нормальной жизни в течение 2-3 дней, некоторым требуется 3-4 недели, чтобы восстановить свои силы.
Существуют ли какие-либо риски, связанные со сдачей стволовых клеток периферической крови? Аферез обычно вызывает минимальный дискомфорт. Донор может чувствовать слабость, дрожь, онемение губ и судороги рук. В отличие от сбора трансплантата костного мозга, сбор стволовых клеток периферической крови не требует анестезии. Однако препараты, используемые для высвобождения стволовых клеток из кости в кровяное русло, могут вызывать костные и мышечные боли, головные боли, усталость, тошноту, рвоту и/или проблемы со сном. Побочные эффекты, как правило, отступают через 2-3 дня после приема последней дозы препарата.
Что происходит после пересадки стволовых клеток пациенту? После попадания в кровеносную систему стволовые клетки осаждаются в костном мозге, где они начинают производить красные кровяные клетки, лейкоциты и тромбоциты. Эти клетки, как правило, начинают функционировать через 2 – 4 недели после трансплантации. Врачи будут следить за этим путем частых анализов крови. Полное восстановление иммунной системы занимает гораздо более длительное время. Этот период обычно занимает несколько месяцев для пациентов после аутотрансплантации и до 1-2 лет для аллогенной и сингенной трансплантаций.
Каковы потенциальные побочные эффекты трансплантации костного мозга? Основной риск обоих методов лечения – это повышенная восприимчивость пациента к инфекциям и кровотечениям из-за высокодозной / высокоинтенсивной терапии. Для профилактики или лечения инфекций, врачи могут назначать пациенту антибиотики. Для предотвращения кровотечений у пациента может понадобиться переливание тромбоцитов, в то время как для лечения анемии могут потребоваться красные кровяные клетки. Пациенты, подвергающиеся пересадке костного мозга и трансплантации стволовых клеток периферической крови, могут испытывать краткосрочные побочные эффекты – тошноту, рвоту, усталость, потерю аппетита, язвы в полости рта, выпадение волос и кожные реакции. Потенциальные долгосрочные побочные эффекты, как правило, связаны с дотрансплантационной химиотерапией и лучевой терапией. Они включают в себя бесплодие (биологическая неспособность человека к зачатию), катаракту (помутнение хрусталика глаза), вторичный рак, и повреждение печени, почек, легких и/или сердца. Риск осложнений и их тяжесть зависит от лечения пациента и эти риски должны быть всесторонне рассмотрены и обсуждены врачом и пациентом.
Что такое «мини – трансплантация»? Мини – трансплантация – это один из видов аллогенной трансплантации (называющейся немиелоаблятивная трансплантация или трансплантация уменьшенной интенсивности). Такой подход в настоящее время изучается с помощью клинических исследований с целью лечения различных типов рака, включая лейкемию, лимфому, множественные миеломы и другие виды рака крови. Мини – трансплантация использует химиотерапию низкой интенсивности или низкоинтенсивную лучевую терапию при подготовке пациента к аллогенной трансплантации. Использование малых доз противораковых лекарств и радиации частично уничтожает костный мозг пациента, однако не приводит к его полному разрушению. С другой стороны, это позволяет сократить количество патологических клеток и подавляет иммунную систему для предотвращения отторжения трансплантата. В отличие от традиционной трансплантации костного мозга или трансплантации стволовых клеток периферической крови, клетки донора и пациента продолжают совместно существовать в течение короткого промежутка времени после мини – трансплантации. Когда костный мозг начинает производить кровь, донорские клетки вступают в реакцию «трансплантат против опухоли» (ТПО) и уничтожают патологические клетки, сохранившиеся после курса радикальной терапии. Для усиления эффекта ТПО, пациенту могут ввести белые кровяные клетки донора. Эта процедура называется «вливание донорских лимфоцитов».