Рассеянный склероз заметно отражается на состоянии зрительной системы человека. У пациента с таким диагнозом зачастую происходит поражение оптического нерва, называемое ретробульбарным невритом. В чем особенности этой офтальмопатологии, как она влияет на зрение и какие методы лечения предлагает современная медицина, читайте в нашей статье.
В этой статье
- Рассеянный склероз: что это за болезнь?
- Какие симптомы могут указывать на РС?
- Как аутоиммунное заболевание влияет на нашу зрительную систему?
- Почему при РС страдает зрение?
- Ретробульбарный неврит зрительного нерва как симптом РС
- Специфика ретробульбарного неврита при рассеянном склерозе
- Как диагностируют ретробульбарный неврит?
- Можно ли вылечить неврит зрительного нерва при рассеянном склерозе?
- Основные направления терапии нисходящего неврита
- Лечение ретробульбарного оптического неврита при РС
- Существуют ли меры профилактики?
- Когда придумают лекарство от рассеянного склероза?
Рассеянный склероз: что это за болезнь?
Рассеянным склерозом (РС) называют аутоиммунную хроническую патологию, сопровождаемую повреждением верхнего слоя нервных волокон мозга (головного и спинного).
Человеческие нервы покрывает так называемая миелиновая оболочка, задача которой — защищать тонкие волокна от негативных воздействий. Когда структура этого поверхностного слоя разрушается, образуются бляшки — дефектные области. В результате сигнал, передаваемый от мозговых центров к органам, доходит плохо или не доходит совсем, что и ведет к нарушению многих функций организма, в том числе и зрительной.
Понятие «аутоиммунная патология», которое часто применяют при описании рассеянного склероза, означает, что к развитию патологического процесса приводят аномалии в функционировании иммунной системы собственного организма. Проще говоря, иммунитет по ошибке принимает собственные клетки за чужеродные и начинает уничтожать их. Происходит замена одних клеток другими, в результате чего на месте нервных волокон образуется рубцовая соединительная ткань.
Многие люди ошибочно связывают термин «рассеянный склероз» с нарушениями памяти у пожилых людей. На самом деле, заболевание, о котором мы говорим, предполагает другой характер нарушений и развивается зачастую в молодом возрасте. Чаще всего болезнь выявляют у пациентов в возрастном диапазоне 15-40 лет, хотя известны случаи, когда рассеянный склероз обнаруживали и у двухлетних малышей.
Статистика показывает, что уровень заболеваемости рассеянным склерозом составляет примерно 25 случаев на каждые 100 тысяч человек. И это вторая по распространенности причина, которая приводит к неврологической инвалидности в юном или молодом возрасте.
Почему возникает рассеянный склероз и есть ли эффективное лечение?
Рассеянный склероз (РС) — это хроническое (продолжающееся) и сложное заболевание, при котором иммунная система вашего организма по ошибке атакует сама себя. Это называется аутоиммунным ответом.
При РС иммунная система атакует и повреждает жировой материал (миелин), изолирующий нервы центральной нервной системы (головной, спинной и зрительные нервы). Это называется демиелинизацией. Здоровый миелин действует как покрытие электрического шнура. Он защищает нервные волокна и позволяет им быстро и эффективно передавать импульсы (сообщения).
Демиелинизация вызывает воспаление и рубцевание (рассеянный склероз означает «множество шрамов»). Образование этих шрамов, известных как бляшки или поражения, влияет на способность нервов передавать сообщения между мозгом и другими частями тела.
Симптомы заболевания
Симптомы рассеянного склероза разнообразны и непредсказуемы, в зависимости от того, какая часть центральной нервной системы поражена и в какой степени. Нет двух одинаковых случаев рассеянного склероза.
Симптомы могут варьироваться ото дня к дню, и симптомы также могут взаимодействовать друг с другом. Симптомы рассеянного склероза могут быть как видимыми, так и невидимыми для окружающих.
Некоторые из наиболее распространенных симптомов рассеянного склероза включают:
- Контроль моторики. Трудности с ходьбой, равновесием или координацией, мышечные спазмы или тремор, мышечная слабость, невнятность или замедление речи, трудности с глотанием, головокружение или головокружение.
- Усталость. Крайняя усталость, часто в сочетании с повышенной чувствительностью к жаре, которая может повлиять на ваши физические, эмоциональные и умственные способности.
- Сенсорные проблемы. Нарушения зрения (например, нечеткость или двоение в глазах или изменения восприятия глубины, частичная или полная потеря зрения), измененные ощущения, такие парестезия, онемение, неврологическая боль, чувствительность к теплу, холоду или дискомфорт.
- Дисфункция мочевого пузыря и кишечника, включая недержание мочи (истечение из мочевого пузыря или кишечника), потребность в более или менее частом мочеиспускании, позывы к мочеиспусканию, частые позывы к мочеиспусканию в ночное время, запор или диарея.
- Когнитивные симптомы, в том числе «мозговой туман», нарушение памяти и концентрации, изменения скорости и способностей обработки данных, нарушение когнитивной функции.
- Личностные и эмоциональные изменения, беспокойство, депрессия и трудности со сном.
РС — хроническое заболевание, требующее постоянной корректировки, лечения, мониторинга и устойчивости. Точно так же он влияет на окружающих по-разному в разное время.
Особенности лечения
Лекарств для лечения рассеянного склероза не существует, они используются для изменения течения болезни. Терапия, использующаяся в данный момент, используется чтобы:
- минимизировать рецидивы;
- уменьшить воспаление;
- предотвратить образование новых повреждений;
- минимизировать атрофию головного мозга;
- восстанавливать утраченные функции;
- свести к минимуму влияние симптомов на вашу повседневную жизнь.
Есть несколько вещей, которые пациент может сделать самостоятельно, чтобы сохранить свой мозг как можно более здоровым:
- держать свой вес под контролем;
- придерживаться здоровой диеты;
- отказаться от курения;
- ограничить употребления алкоголя;
- поддерживать достаточный уровень физической активности;
- изучать некоторые способыуправления стрессом.
Рассеянный склероз может вызывать стресс из-за его непредсказуемости, но стресс, в свою очередь, может увеличить риск рецидива. Поэтому последний пункт крайне актуален для снижения скорости прогрессирования заболевания.
Прогноз
Прогресс РС и прогноз человека невозможно предсказать на ранних стадиях с большой точностью. Людям с рассеянным склерозом на ранних стадиях рекомендуется стараться вести нормальный образ жизни, часто заниматься спортом и соблюдать здоровую диету. Однако не было доказано, что какая-либо конкретная диета при рассеянном склерозе отрицательно влияет на течение болезни. Если у вас рассеянный склероз, отслеживайте симптомы, которые появляются во время упражнений, чтобы приспособиться к ним и научитесь соответственно уменьшать уровень своих усилий.
Хотя лекарства от рассеянного склероза еще не существует, исследователи ежедневно делают многообещающий прогресс и делают открытия в области лечения и ведения больных.
Какие симптомы могут указывать на РС?
У разных пациентов при рассеянном склерозе симптомы могут заметно отличаться. Более того, на разных стадиях патологического процесса они могут быть различными у одного и того же человека. Это объясняется тем, что симптомы напрямую зависят от того, какие именно зоны мозга и ЦНС затронуты аномальными изменениями.
Большинство симптомов, возникающих при рассеянном склерозе, можно отнести к неврологическим и офтальмологическим.
- У пациента наблюдаются серьезные нарушения зрения (чаще односторонние).
- При движении глаза могут возникать болевые ощущения.
- Изменяется чувствительность тканей — человек может ощущать покалывание, зуд, онемение.
- Постоянное чувство усталости, быстрая утомляемость.
- Изменение мышечного тонуса.
- Нарушенная координация, утрата равновесия, неустойчивость при ходьбе.
- Нарушения в работе мочеполовой системы — недержание мочи, сниженное либидо, эректильная дисфункция.
- Эмоциональная лабильность, неврозы.
Любой из этих симптомов, а в особенности их совокупность — это веская причина для консультации со специалистом.
Рассеянный склероз (РС) — это заболевание с многоочаговым поражением центральной нервной системы (ЦНС). Как известно, классическими проявлениями РС являются признаки поражения пирамидной, сенсорной и мозжечковой систем, вовлечение краниальных нервов и также тазовые расстройства [1-3]. Эта клиническая симптоматика встречается в различном сочетании, отражая локализацию очагов демиелинизации в головном и спинном мозге. Тем не менее выделяют «типичные» и «нетипичные» для РС симптомы [3]. Если типичные симптомы помогают клиницисту диагностировать РС, то нетипичные заставляют искать другие причины их возникновения, и РС становится диагнозом «исключения». Одним из «нетипичных» проявлений РС являются экстрапирамидные двигательные расстройства. В литературе имеются редкие описания спастической кривошеи [4, 5], хореи, дистонии [6], дрожательного гиперкинеза при РС [7]. Единичные статьи посвящены миоклониям [8-12]. В своей клинической практике мы столкнулись с таким необычным проявлением РС, как спинальная миоклония. Поскольку это весьма необычное проявление РС, оно может представлять интерес для специалистов.
Больной А.
, 33 лет, работает инженером, левша. Из анамнеза жизни: наследственность пациента не отягощена. В 10-летнем возрасте отмечал развитие слабости и чувства онемения в левых конечностях, по поводу чего был госпитализирован в неврологическое отделение детской больницы с диагнозом «Острое нарушение спинномозгового кровообращения». На фоне проведенного лечения симптоматика в течение полугода полностью регрессировала, после чего больного ничего не беспокоило.
Около 3 лет назад, в возрасте 30 лет, пациент обратил внимание на периодические «подергивания» в левых кисти, предплечье и плече. Такие подергивания отмечались 2-3 раза в неделю, при целенаправленных движениях, носили спонтанный характер и учащались при волнении. Пациент не мог сдержать или уменьшить эти насильственные движения какими-либо приемами или усилием воли. Яркий свет и громкие звуки также не оказывали на подергивания никакого влияния. Поскольку выраженность насильственных движений, по оценке пациента, не была значительной, то он не обращался за медицинской помощью. С течением времени подергивания в левой руке стали возникать чаще, иногда вне зависимости от активных движений, они уже беспокоили больного в покое и сохранялись во сне. Увеличение амплитуды насильственных движений заставило пациента оставить работу и обратиться за медицинской помощью. Подергивания усиливались при эмоциональных нагрузках и уменьшались после приема алкоголя. Другие внешние факторы влияния на них не оказывали. Приступов с потерей сознания у пациентов не было.
При обследовании больного в соматическом статусе патологии обнаружено не было. При неврологическом осмотре регистрировалось легкое нарушение ассоциированных движений глазных яблок без двоения и нистагма, наблюдалась легкая сглаженность правой носогубной складки. Выявлялась гиперестезия стоп с двух сторон с уровня голеностопных суставов, гипестезия левого мизинца кисти и нижней трети внутренней поверхности левого предплечья, причем активных жалоб на изменение чувствительности пациент не предъявлял. Вибрационное и мышечно-суставное чувство было сохранно, мышечная сила — достаточной. Сухожильные рефлексы с верхних конечностей носили обычный характер, с нечетким преобладанием слева, коленные и ахилловы рефлексы были оживлены. Подошвенные рефлексы имели сгибательный тип, брюшные отсутствовали. Пальценосовую пробу слева пациент выполнял с кинетическим тремором, без интенционного компонента. Тандемная ходьба не была нарушена. Дисдиадохокинез, асинергия Бабинского и тазовые нарушения не выявлялись.
В плечевом поясе слева и левой руке фиксировались насильственные движения — толчкообразные подергивания в виде резкого попеременного сокращения мышц плеча, предплечья, разгибателей кисти и сгибателей пальцев кисти, что приводило к периодическому возникновению то умеренного (на 20-25°) разгибания в плечевом, то сгибания в локтевом (на 10-15°), то к одновременному разгибанию в лучезапястном суставах и сгибанию пальцев кисти. Особенно ярко гиперкинез проявлял себя при вытягивании рук вперед и удержании их в данном положении, с частотой до 10 в минуту. В покое выявлялись редкие гиперкинезы вышеописанного характера, но значительно меньшей амплитуды. Гиперкинез мешал пациенту совершать точные движения — он не смог написать свою фамилию. Резкий шум (хлопанье в ладоши), постукивание (по мышцам, сухожилиям) и свет не вызывали усиления миоклоний.
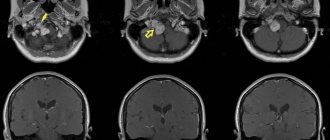
Лабораторные анализы крови и мочи были в норме. По результатам магнитно-резонансной томографии (МРТ) головного и спинного мозга были выявлены множественные очаги демиелинизации величиной 3-7 мм, гиперинтенсивные на Т2-взвешенных изображениях (Т2-ВИ) и гипоинтенсивные на Т1-взвешенных изображениях (Т1-ВИ), локализующиеся в белом веществе больших полушарий мозга, перивентрикулярных и подкорковых отделах, мозолистом теле. Аналогичный единичный очаг наблюдался в правом полушарии мозжечка (рис. 1)
.
Рисунок 1. МРТ головного мозга. Множественные очаги демиелинизации, гиперинтенсивные на Т2-ВИ. a — локализующиеся в белом веществе больших полушарий мозга, перивентрикулярных и подкорковых отделах; б — аналогичный единичный очаг регистрируется в правом полушарии мозжечка; в — очаги перивентрикулярно и в мозолистом теле; г — МРТ через 3 мес, по сравнению с предшествующими результатами выявлено появление новых очагов демиелинизации; очаг у заднего рога правого бокового желудочка накапливает контрастное вещество.
На уровне сегмента С2 определялись 2 интрамедуллярных очага без четких контуров, слабогиперинтенсивные на Т2-ВИ и изоинтенсивные на Т1-ВИ, размерами 4×6 и 4×7 мм. Не исключалось наличие аналогичного очага на уровне сегментов С4-С5 и С5-С6 шейного отдела спинного мозга (рис. 2)
.
Рисунок 2. МРТ спинного мозга. На уровне сегмента С2 определяется 2 интрамедуллярных очага без четких контуров, слабо гиперинтенсивные на Т2-ВИ; не исключается наличие аналогичных очагов на уровне сегментов С4-С5 и С5-С6 шейного отдела спинного мозга (указано стрелками).
При электроэнцефалографии патологии выявлено не было. Во время непроизвольных сокращений мышц левой руки патологических изменений на ЭЭГ не регистрировалось. Игольчатая электромиограмма (ЭМГ) выявила разряды из нескольких двигательных единиц m. extensor dig. com.
слева (сегмент С7), продолжительность разряда 70 мс и амплитуда 1400 мкВ. При проведении исследования в других мышцах, иннервируемых другими сегментами, ответы не были получены
(рис. 3)
.
Рисунок 3. Игольчатая ЭМГ. Разряд с m. extensor dig. сom.
продолжительностью 70 мс и амплитудой 1400 мкВ (в других мышцах из других сегментов ответы не были получены). При стимуляционной ЭМГ было выявлено нарушение проведения по моторным волокнам левой руки на уровне локтя (туннельный синдром), по нервам левой руки изменений обнаружено не было.
Таким образом, больной был обследован в период эпизода ухудшения неврологического статуса. Этот эпизод развился у молодого мужчины (33 года) без предшествующей или сопутствующей инфекции/лихорадки. Обнаружение 2 и более признаков многоочагового поражения ЦНС при осмотре и выявление типичных для РС очагов при нейровизуализации (субкортикально, перивентрикулярно, инфратенториально и в спинном мозге) [13] позволили остановиться на диагнозе «вероятный рассеянный склероз». Эпизод, произошедший в детстве (слабость и онемение слева), мог быть первой атакой РС (хотя его документального подтверждения нет). Если это так, то мы имеем дело с началом РС в детском возрасте. Пациент получил стандартную пульс-терапию глюкокортикостероидами и на 3-й день лечения отметил уменьшение частоты подергиваний. Объективно при этом регистрировался миоклонический гиперкинез в левой руке, который носил больше постуральный характер и появлялся с частотой 8-10 в минуту, в покое подергивания не выявлялись. Через 1 мес миоклонии купировались полностью.
Для верификации диссеминации патологического процесса во времени и установления достоверного диагноза РС пациенту было проведено повторное МРТ-исследование головного мозга через 3 мес. По сравнению с предшествующими результатами МРТ отмечалось появление новых очагов демиелинизации слева в перивентрикулярном отделе и у заднего рога правого бокового желудочка; при введении контраста последний очаг накапливал контрастное вещество (омнискан) (см. рис. 1)
. Согласно критериям Макдональда [13], пациенту был выставлен диагноз: РС, ремиттирующее течение. Через 3 мес гиперкинезов в руке выявлено не было.
Рассматривая представленное наблюдение, следует еще раз отметить, что спинальные миоклонии (СМ) — довольно редкие формы гиперкинезов. Они могут быть разделены на сегментарные и проприоспинальные [14-19]. Это разделение основывается на сегментарном строении спинного мозга и связях сегментов посредством проприоспинального пути. Спинальные сегментарные миоклонии (ССМ) представляют собой непроизвольные движения, вовлекающие в гиперкинез мышцы, которые иннервируются одним или несколькими соседними сегментами спинного мозга [17, 20-22].
В приведенном наблюдении миоклонии локализовались в одной руке. Если проанализировать всю кинетику имевшегося гиперкинеза, то движения, составлявшие гиперкинез, а именно разгибание плеча (m. deltoideus, m. supraspinatus)
; сгибание в локтевом суставе (
m. biceps brachii, m. brachialis, m. brachiradialis
); разгибание кисти (
m. extensor carpi radialis longus, m. extensor carpi radialis brevis, m. extensor dig. com.
); сгибание пальцев кисти (
m. flexor digitorum superficialis
) обеспечивались мышцами, иннервация которых осуществляется несколькими соседними сегментами С5-С7 [23]. Соответственно у пациента наблюдались ССМ.
В большинстве случаев ССМ являются симптоматическими, и в их основе лежат очаги в спинном мозге, обусловленные каким-либо первичным заболеванием — инфекцией [24-26], опухолью [27], артериовенозной мальформацией [28], сирингомиелией [16], острым рассеянным энцефаломиелитом [29], вертебральной патологией [28], ятрогенией [125] и т.д. [10, 30-35]. Напомним, что у наблюдаемого больного обнаруживались очаги демиелинизации на уровне сегментов С2, С4, С5, С6 шейного отдела спинного мозга, и именно эти очаги могли служить причиной возникновения миоклонических подергиваний сегментарного характера (см. рис. 2)
.
Клинически ССМ чаще всего нерегулярные или же могут быть ритмичными с частотой 0,2-8 Гц и интенсивностью 1-600 в минуту [10, 16, 22, 30, 32, 36]. Амплитуда также разнообразна — от едва заметных сокращений отдельных мышц или группы мышц до интенсивных движений в суставах [8]. Тема сегментарных миоклоний при РС освещена в литературе очень скудно ввиду редкости данного состояния. J. Jankovic и R. Pardo [10] приводят описание 5 больных РС, у которых обнаруживался сегментарный гиперкинез стволового происхождения в виде небной миоклонии. Миоклонический гиперкинез у пациента с РС в наблюдаемом нами случае носил периодический, неритмичный характер, с интенсивностью до 10 раз в минуту и приводил к визуальному насильственному движению в суставах левой руки.
Проприоспинальные миоклонии (ПСМ) — второй вид СМ, который отличается от ССМ вовлечением в гиперкинез большего количества мышечных групп — наряду с конечностями подергивания наблюдаются и в туловище [15-19, 32]. Происходит это ввиду распространения патологической импульсации по проприоспинальному пути, и в гиперкинез последовательно вовлекается множество сегментов спинного мозга [14, 19]. В отличие от СCМ проприоспинальные подергивания чаще не имеют определенной этиологии. Некоторые авторы [17] связывают их возникновение с травмой шеи, опухолью, вирусным миелитом и психогенными факторами. В литературе описан случай лайм-боррелиоза, проявившегося клинически в форме ПСМ [37]. При ПСМ наблюдаются ритмичные или неритмичные аксиальные сгибательные движения, вовлекающие в гиперкинез шею, тело, конечности, с частотой около 1-6 Гц. Гиперкинезы обычно возникают спонтанно, в горизонтальном положении на спине и могут провоцироваться кожной стимуляцией области живота или при вызывании сухожильных рефлексов [17, 19]. У описываемого пациента в гиперкинез была вовлечена только одна рука, туловище и нижние конечности оставались интактными, что говорит скорее о сегментарном характере поражения, без массивного вовлечения проприоспинального пути.
Имеется единичное описание ПСМ при РС [11]. У больной РС периодически, после предшествующих чувствительных ощущений на шее (покалывание), развивались спонтанные нерегулярные подергивания в правых плече и руке. Насильственные подергивания распространялись на туловище и сгибатели бедра с правой стороны. На МРТ авторами были выявлены очаги в шейных сегментах С2, С3, С4. Развитие ПСМ авторы объясняли тем, что очаги в белом веществе могли привести к расторможению спинальной активности, но допускали, что причиной могла быть и гипервозбудимость демиелинизированного аксона, который в таком поврежденном состоянии способен спонтанно или рефлекторно генерировать импульсы патологической мышечной активности.
Для обеих разновидностей СМ характерны сохранение гиперкинезов во сне и относительная устойчивость к внешним стимулам — они не усиливаются под воздействием слуховых, зрительных, тактильных раздражителей и при двигательной активности [10, 14, 16, 27, 30], хотя в литературе и имеются описания случаев ССМ с исчезновением во сне и чувствительностью к внешним раздражителям [22, 31, 32]. Считается, что по мере прогрессирования заболевания может появиться реакция на внешние воздействия [15]. Для СМ более патогномоничен постуральный компонент — усиление гиперкинеза в определенном положении, а также усугубление подергиваний при утомлении и эмоциональных нагрузках [31, 32]. ССМ, наблюдавшиеся у изучаемого пациента, сохранялись во сне, не имели зависимости от слуховых и зрительных стимулов, однако усиливались от эмоциональных нагрузок и утомления, уменьшались на фоне приема алкоголя.
Следующей важной отличительной чертой СМ является отсутствие патологической активности на ЭЭГ. Совместное выполнение ЭЭГ-ЭМГ должно исключить наличие предшествующей мышечному сокращению гипервозбудимости коры [10, 16, 30]. В рассматриваемом случае ЭЭГ не показала очагов гипервозбудимости, что позволило с большой вероятностью исключить корковый характер гиперкинезов.
Поверхностная ЭМГ при СМ позволяет выявить ритмичные или полуритмичные разряды, которые обычно синхронны, со стереотипной продолжительностью и частотой. ЭМГ-исследование при ССМ демонстрирует разряды продолжительностью более 100 мс (до 1000 мс) и ограниченные одним или двумя соседними миотомами. При ПСМ миоклонические разряды могут длиться от 50 мс до 4 с, формируются они из абдоминальных и шейных сегментов и распространяются медленно рострально и каудально, при этом краниальные мышцы остаются интактными. Для ПСМ характерны задержка между разрядами и последовательное их распространение, что обусловлено медленным проведением импульса по проприоспинальному пути [17, 30]. В описываемом нами случае продолжительность разряда составляла 70 мс, что не очень соответствует представленному в литературе описанию сегментарных миоклоний, а больше характерно для проприоспинальных. Однако ни клинически, ни нейрофизиологически мы не наблюдали распространения насильственных сокращений мышц, что с большой вероятностью исключает проприоспинальный характер миоклоний.
Описанное нами наблюдение демонстрирует яркую картину ССМ при РС. Отсутствие эпилептической активности на ЭЭГ, наличие разрядов в мышцах левой руки (сегмент С7), вовлечение в гиперкинез мышц левой верхней конечности, иннервация которых обеспечивается 3-4 соседними сегментами, и, наконец, регистрация очагов демиелинизации в спинном мозге, а именно на уровне сегментов С2, С4, С5, С6 шейного отдела, — все это подтверждает спинальный сегментарный характер миоклоний. Причиной возникновения ССМ, скорее всего, послужили очаги демиелинизации в спинном мозге. Исчезновение гиперкинеза после терапии гормонами укрепляет наше предположение о генезе насильственных движений.
Существуют различные гипотезы механизма развития СМ [8, 21, 26, 31, 32, 38-40]. Учитывая, что миоклонический гиперкинез у наблюдаемого пациента появлялся изредка в покое и ярче всего проявлял себя при удержании позы, наиболее вероятным является вариант механизма развития, в основе которого лежит разрыв межсегментарных связей очагами демиелинизации в спинном мозге [18]. Это могло привести к локальной дизрегуляции работы гамма-мотонейронной петли с последующим возникновением спонтанных нейрональных импульсов в сегментах спинного мозга и формированием миоклонического гиперкинеза. Возможно, важное значение имело расположение очагов относительно серого вещества спинного мозга.
Таким образом, основными опорными пунктами диагностики ССМ в приведенном наблюдении могут служить: 1) вовлечение в гиперкинез ограниченной группы мышц, иннервируемых несколькими соседними сегментами спинного мозга; 2) отсутствие влияния внешних раздражителей (слуховых, зрительных, тактильных) и активных движений на степень выраженности гиперкинеза; 3) сохранность гиперкинезов во сне, усиление их под влиянием утомления и эмоций, появление миоклоний в определенном положении; 4) отсутствие гипервозбудимости на ЭЭГ; 5) патологическая ЭМГ-активность мышц в ограниченных миотомах интенсивностью 70 мс.
Лечение ССМ, в частности при РС, предусматривает терапию основного заболевания — купирование обострения применением глюкокортикостероидов. В случае отсутствия эффекта препаратом выбора считается клоназепам в дозе до 6 мг в сутки [10, 17, 18, 22, 30]. Терапия баклофеном может улучшить ночные миоклонии в ногах [10]. В литературе имеется упоминание об эффективности при СМ топирамата и леветирацетама. Тетрабеназин применяется при отсутствии эффекта от других препаратов [10, 30]. Возможно комплексное применение препаратов, например тизанидина, клоназепама и баклофена [38]. В литературе имеются описания позитивного эффекта ботулинотерапии при СМ [17, 18, 30].
В заключение отметим, что приведенное наблюдение демонстрирует ССМ, как одно из редчайших проявлений РС. Основу этого «нетипичного» симптома РС составлял очаг демиелинизации, расположенный в спинном мозге шейного отдела.
Как аутоиммунное заболевание влияет на нашу зрительную систему?
При рассеянном склерозе наблюдаются симптомы со стороны зрительных органов. Более того, зачастую именно ухудшение зрения, боль в глазах и другие офтальмологические симптомы побуждают человека обратиться к врачу, где ему ставят диагноз РС.
Для этой болезни могут быть характерны разнообразные зрительные симптомы.
- Снижение зрительной остроты (от незначительного до ярко выраженного, с сохранением только светоощущения).
- Затуманенность зрения.
- Боль в движущемся глазу, может сочетаться с головной болью.
- Изменение зрительных полей: появление пятен перед глазами, концентрическое сужение.
- Повышение светочувствительности.
- Изменение цветоощущения — пациент хуже различает оттенки, видит мерцающие блики.
- Нарушения пространственного, «объемного» зрения.
Зачастую комплекс подобных симптомов указывает на болезнь, которая часто сопровождает РС, — ретробульбарный неврит зрительного нерва.
Почему при РС страдает зрение?
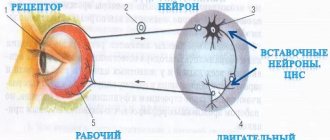
Глаза как орган зрения тесно связаны с головным мозгом, где находится зрительная кора, ответственная за обработку визуальных данных. Оптический нерв представляет собой важнейшую пару черепных нервов, передающих визуальные сигналы от сетчатой оболочки глаза к мозгу. От правильного функционирования зрительного нерва напрямую зависит качество зрения. Закономерно, что поражение оболочек тонких нитей нервного вещества мозга негативно отражается на состоянии глазной сетчатки и зрительного нерва.
Невритом называют воспалительный процесс в оптическом нерве. В общей классификации выделяют восходящий и нисходящий неврит. Первый называется папиллитом, и при нем воспаление сосредоточено внутри глазного яблока. Нисходящий неврит — ретробульбарный, и при нем воспаление может распространяться по всей протяженности нерва от глаза до области перекреста нервных волокон, так называемой хиазмы.
Диплопия
Так называют эффект двоения в глазах, который возникает по причине несогласованного функционирования мышц, ответственных за движение глазных яблок. Дискоординация глазных мышц приводит к смещению зрительной оси одного глаза, в результате чего изображение попадает не в центр сетчатой оболочки, а на другой участок, что и приводит к эффекту двоения.
Такая проблема часто развивается вследствие мышечной слабости и особенно ярко проявляет себя при большой нагрузке на глаза. Хотя такое состояние не лечат специальными методами, игнорировать его нельзя. Диплопия может указывать на развитие рассеянного склероза или других заболеваний.
Ретробульбарный неврит зрительного нерва как симптом РС
Специалисты отмечают, что зачастую ретробульбарный неврит на протяжении многих лет остается единственным симптомом РС. По статистике этот диагноз ставят примерно 15% пациентов с начальной формой заболевания. По мере развития аутоиммунной болезни ретробульбарный неврит выявляется у половины всех пациентов.
Если проявления воспалительного процесса не сильно мешают человеку, он может длительное время не посещать врачей. Это приводит к поздней диагностике болезни, когда эффективность лечения будет гораздо ниже, чем на ранней стадии.
Опытные офтальмологи, которые видят у человека признаки ретробульбарного неврита, обязательно инициируют полное диагностическое обследование и отправляют пациента на консультацию и диагностику в том числе к врачу-неврологу.
Двоение в глазах
Такое явление по-научному называется диплопия и возникает в том случае, когда парные глазные мышцы, отвечающие за движение глаз, ослаблены и не могут работать синхронно. Дискоординация приводит к тому, что изображение в глазах человека раздваивается. Проблема усугубляется при большом зрительном напряжении или долгой работе за компьютером.
Диплопия мешает водить автомобиль, вести привычный образ жизни, но обычно не требует специального лечения. Тем не менее, если Вы заметили у себя диплопию, нужно обязательно обследоваться, поскольку она может быть ранним признаком РС.
Специфика ретробульбарного неврита при рассеянном склерозе
Нисходящий неврит зрительного нерва при рассеянном склерозе может проявляться теми же симптомами, что и другие разновидности невритов. Но при этом специалисты выделяют ряд особенностей, которые характерны для воспалительного процесса, развивающегося на фоне РС.
- Ремиттирующее течение болезни. Для больных рассеянным склерозом характерно волнообразное протекание неврита, при котором периоды с острой, ярко выраженной симптоматикой сменяются полным исчезновением или значительным ослаблением симптомов болезни. После периода ремиссии зачастую снова наступает рецидив.
- Кратковременное снижение зрительной остроты. Воспаление зрительного нерва часто сопровождается резким ухудшением зрения: пациент начинает видеть менее четко или с трудом различать контуры объектов, может возникать ощущение тумана, размытости. При этом особенностью неврита зрительного нерва на фоне РС является тот факт, что подобная симптоматика может быть кратковременной, и уже через 7-20 дней острота и четкость зрения восстанавливаются полностью. Специалисты отмечают, что ни при каких других видах ретробульбарного неврита не происходит полного и настолько быстрого восстановления зрительных функций. В то же время в период дальнейших обострений восстановление зрения происходит все медленнее и уже не является полным. Подобная специфика клинических проявлений неврита часто приводит к поздней диагностике рассеянного склероза. Поскольку зрение после первого резкого падения восстанавливается довольно быстро, многие пациенты считают, что нет повода для обращения к врачу. На самом деле, именно в этот период важно обратиться к специалисту, который правильно поставит диагноз и назначит лечение. На ранней стадии есть высокие шансы сохранения зрения и замедления прогрессирования болезни.
- Суточное колебание зрительной остроты. Для зрительного неврита при РС характерно изменение зрительной остроты зрения в разное время суток. В частности пациенты с рассеянным склерозом в утренние часы видят более четко и ясно, нежели в вечерние. При этом диапазон колебаний в диоптриях может составлять 0,05-0,2 дптр. Нередко снижение зрительной остроты наблюдается после занятий спортом, физических нагрузок и употребления горячей пищи.
- Локализация слепых пятен в центре. Характерные для зрительного неврита скотомы при рассеянном склерозе обычно локализуются в области центрального зрения. Они могут выглядеть как темные круги или пятна перед глазами. Нередко скотомы при РС сопровождаются сужением зрительного поля на периферии. В периоды ремиссии, когда зрение восстанавливается, скотома из центра зрительного поля обычно исчезает.
- Неустойчивое выпадение участков зрительного поля. Неврит зрительного нерва часто приводит к выпадению отдельных участков зрительного поля. Специфика болезни, развивающейся при рассеянном склерозе, состоит в том, что выпадение зрительных полей является изменчивым и неустойчивым. Проще говоря, слепые участки могут то появляться, то исчезать, возникать то в одном, то в другом месте.
- Временные нарушения цветоощущения. Нарушенное восприятие цветов при ретробульбарном неврите на фоне РС также имеет свои особенности. Как и некоторые другие симптомы, снижение цветовой чувствительности зачастую носит временный характер. То пациент может заметить, что начал хуже различать цвета, но спустя короткое время к нему возвращается нормальное цветовое восприятие. Еще одна характерная особенность патологии состоит в том, что у пациента нарушается чувствительность сразу ко всем цветам.
- Боль в глазах. Почти всегда ретробульбарный неврит при РС сопровождается болезненными ощущениями в глазами и отечностью век. Наиболее выраженные болевые ощущения возникают, когда пациент пытается смотреть вверх или надавливает на глазные яблоки. Боль в глазах при рассеянном склерозе может продолжаться от нескольких часов до нескольких дней и объясняется раздражением оболочек оптического нерва, возникающим при натяжении мышечных сухожилий. Болевые ощущение могут возникать как параллельно с потерей зрительной функции, так и предшествовать ей.
- Поражение зрительного нерва с одной стороны. Ретробульбарный неврит зрительного нерва при РС зачастую поражает только один глаз. Случаи двустороннего неврита также встречались на практике, но они являются более редкими.
- Неспецифическое поражение глазного дна и диска нерва. При офтальмологическом осмотре на глазном дне и в диске зрительного нерва зачастую не наблюдается специфических изменений, которые могли бы со 100%-ной точностью указать на РС. Более того, на ранней стадии заболевания состояние глазного дна нередко является нормальным.
- Поражение зрительного нерва при РС сопровождается двоением. Диплопия часто возникает как признак повреждения ствола головного мозга. На то же нарушение может указывать и нистагм (он характерен для 70% случаев). Возможно развитие экзофтальма, при котором глазные яблоки выпячиваются вперед, или птоза.
- Побледнение диска зрительного нерва в височной зоне. Атрофия зрительного нерва и побледнение его диска обычно начинаются с височной половины.
- Необычная реакция зрачков на свет. Повреждение зрительного нерва внешне может проявляться в расширении зрачков под воздействием света (обычно при ярком освещении зрачок, напротив, сужается). Также признаком патологии может быть гиппус — приступообразное состояние, при котором зрачок ритмично сужается и расширяется.
Диагностика рассеянного склероза
Диагностика рассеянного склероза несколько затруднена, особенно в ранний период. Связано это с разнообразием и неспецифичностью симптомов.
Первым этапом диагностики является тщательный сбор жалоб, уточнение анамнеза. Обращает на себя внимание волнообразность течения заболевания, признаки многоочагового поражения нервной системы, непостоянство клинических проявлений.
На этапе физикального обследования оцениваются мозжечковые и пирамидные функции, исследуется глазное дно, острота зрения.
Лабораторная диагностика включает в себя проведение общего анализа крови, общего анализа мочи, биохимического анализа крови, анализ цереброспинальной жидкости (отмечается цитоз и увеличение иммуноглобулинов в ликворе).
Наиболее информативным инструментальным методом исследования для постановки диагноза является магнитно-резонансная томография, которая дает возможность выявить очаги разрушения миелиновой оболочки в центральной нервной системе.
Результаты МРТ оцениваются с учетом клинической картины. Используется также метод исследования вызванных потенциалов, который заключается в регистрации электрической реакции мозга на воздействие внешних раздражителей (зрительных, слуховых, соматосенсорных).
Обследование пациентов направлено не только на подтверждение диагноза, но и на исключение других заболеваний, имеющих схожую симптоматику.
Как диагностируют ретробульбарный неврит?
Диагностика оптического неврита предполагает тщательное обследование пациента с применением разных методов.
- Сбор анамнеза, опрос пациента. На первом приеме врач выясняет у пациента, какие симптомы и как давно его беспокоят; есть ли родственники, страдающие рассеянным склерозом; наблюдались ли раньше проблемы со зрением и какого рода.
- Офтальмологический осмотр. С учетом жалоб пациента врач обычно проводит исследование зрительной остроты по специальным офтальмологическим таблицам, оценивает качество и особенности цветовосприятия, осматривает глазное дно, изучает состояние диска зрительного нерва; проверяет зрачковую реакцию на световые раздражители, определяет зрительные поля на наличие скотом, концентрического сужения.
- Консультация невролога. При воспалении оптического нерва офтальмолог зачастую отправляет пациента на консультацию к неврологу даже при отсутствии неврологических симптомов. Осмотр врача-невролога является обязательным, если предположительной причиной развития неврита является рассеянный склероз.
- МРТ головы. Томография помогает обнаружить признаки поражения головного мозга, которые характерны для РС, либо выявить другие возможные причины нисходящего неврита — например, опухоли. Перед МРТ пациенту обычно вводят специальный раствор красящего вещества, который обеспечивает четкую визуализацию зрительного нерва на снимках.
- ОКТ. Еще одна диагностическая процедура, которая позволяет подтвердить или опровергнуть наличие ретробульбарного или другого неврита. ОКТ является безболезненным методом исследования, который проводится за считанные минуты. В процессе диагностики пациент должен смотреть на специальную метку, пока томограф сканирует сетчатую оболочку глаза, позволяет рассмотреть структуру, зрительного нерва, толщину волокон и внутреннего слоя сетчатой оболочки. При РС нейроны в головном мозге воспаляются и меняют свою структуру. Изменения мозговых нейронов влияют на изменения в сетчатке и оптическом нерве. Специалисты обнаружили, что при РС, как правило, наблюдается уменьшение толщины внутреннего слоя сетчатой оболочки. Этот симптом можно обнаружить в ходе ОКТ. Также во время оптической когерентной томографии специалист может оценить быстроту прохождения визуального сигнала от глазной сетчатки до головного мозга, что также позволяет делать определенные диагностические выводы.
- Анализы крови и другие исследования. Нисходящий неврит может быть вызван, помимо РС, воспалением в зрительных органах, общими инфекционными заболеваниями, патологиями внутренних органов, синдромом Девика. В последнем случае выяснить причину помогает исследование крови на выявление специфических антител.
Основная задача диагностики — установить, каким заболеванием или патологическим состоянием спровоцировано повреждение зрительного нерва. Ведь при ретробульбарном неврите зрительного нерва лечение будет напрямую зависеть от тех патологических процессов в организме, которые спровоцировали воспаление.
Более того, лечение любого зрительного неврита должно заключаться прежде всего в терапии основной патологии.
Глава 5. Нарушения зрения и движений глазных яблок
Потеря зрения
Может возникнуть в результате поражения зрительного пути, проходящего от сетчатки до задних отделов полушарий головного мозга. Из-за высокой чувствительности зрительной системы появление даже такого незначительного симптома, как «пелена перед глазами», может указывать на наличие состояния, угрожающего зрению и жизни больного, поэтому требуется самое серьезное отношение врача к жалобам больного.
Подход к больному
Анамнез. Наиболее важно выяснить вопрос, как быстро развивалось нарушение зрения — остро, подостро или хронически. Также важно, затронуло ли, по мнению больного, нарушение зрения один или оба глаза (больному не всегда легко это определить). Другие направления исследования включают выявление сопутствующих симптомов (боль в глазах, головная боль), предрасполагающих заболеваний (артериальная гипертензия, сахарный диабет, рассеянный склероз, СПИД), контакт с медикаментами и токсинами, а также семейный анамнез (состояние зрения у родственников).
Обследование. Важно выяснить моно- или бинокулярный характер нарушения зрения, выявить выпадения полей зрения (центральная скотома, одноименная геми-анопсия и др.). Оценка остроты зрения и полей зрения для каждого глаза имеют первостепенное значение. Далее проводят исследование роговицы, хрусталика, сосудистой оболочки, глазного дна, зрачкового рефлекса для оценки состояния сетчатки и зрительного нерва (снижение реакции зрачка на свет — показатель дисфункции зрительного нерва). Детальный неврологический осмотр для выявления патологических процессов в ретроорбитальной зоне завершает исследование.
Оценка полей зрения позволяет отличить поражение переднего отдела зрительного анализатора (оптические среды глаза, сетчатка, зрительный нерв до хиазмы) от заднего (оптический тракт, латеральное коленчатое тело, radiatio optica и представительство зрения в коре затылочной доли). Поражение переднего отдела зрительного анализатора может вести к моно- или бинокулярным нарушениям; поражение задних отделов зрительного анализатора ведет к сходным изменениям полей зрения обоих глаз. На рис. 11-1 показаны наиболее часто встречающиеся выпадения полей зрения, изображение дифференцированно в зависимости от поражения того или иного участка зрительного пути.
В табл. 11-1 представлены типичные причины нетравматического нарушения зрения. Дифференциальный диагноз, основанный на анамнезе и результатах обследования, должен быть сведен к единичной категории (например, острое монокулярное нарушение зрения). Новая информация, почерпнутая из анамнеза и обследования, может еще больше сузить диагноз, но для этого требуется дополнительное обследование.
Центральная скотома (неврит зрительного нерва, токсическая или метаболическая невропатия зрительного нерва) Дугообразная скотома (ишемия глазного нерва или реакция на повышение внутриглазного давления — глаукома) Выпадение верхней половины поля зрения (передняя ишемическая невропатия зрительного нерва; тромбоз ветви артерии сетчатки) Центроцекальная скотома (неврит зрительного нерва; токсическая, метаболическая или врожденная невропатия зрительного нерва) Сужение поля зрения (дегенерация сетчатки, сдавление зрительного нерва)
Хиазма Битемпоральная (сдавление хиазмы опухолью) гемианопсия
Задний зрительный путь Гомонимная гемианопсия (значительное одностороннее поражение заднего отрезка зрительного анализатора) Правосторонняя верхнеквадрантная гемианопсия (одностороннее выраженное поражение височной части radiatio optica) Сохранность только (двустороннее поражение центральной части зрительной зоны коры) поля зрения — «трубчатое зрение»
Рис. 11-1. Выпадение зрительных полей, вызванное поражением переднего, хиаз-малъного или заднего участков зрительного пути.
Таблица 11-1 Наиболее частые причины нарушения зрения
ОСТРЫЕ
Монокулярные
Передний зрительный путь: ишемия или сосудистая окклюзия (передняя ишемическая невропатия зрительного нерва), височный артериит, окклюзия центральных артерий или вен сетчатки; иммунологическая причина (неврит зрительного нерва, папиллит); отслойка сетчатки.
Бинокулярные
Передний зрительный путь (реже): двусторонняя передняя ишемическая невропатия зрительного нерва.
Задний зрительный путь: инфаркт или кровоизлияние в вещество головного мозга; кровоизлияние в гипофиз.
ПОДОСТРЫЕ ИЛИ ХРОНИЧЕСКИЕ
Монокулярные
Передний зрительный путь: сдавление опухолью (глиома оболочки зрительного нерва или менингиома); преимущественно одностороннее проявление бинокулярного нарушения зрения.
Бинокулярные
Передний зрительный путь (NB могут быть асимметричными и поэтому кажутся монокулярными): помутнение роговицы, хрусталика (катаракта) или стекловидного тела; дегенерация сетчатки; вазопатия сетчатки (гипертензионная, диабетическая); дефицит факторов питания (дефицит витамина В12), отравления (метанол, этамбутол, хинин); инфекционные поражения сетчатки (токсоплазмоз); врожденная невропатия зрительного нерва (болезнь Лебера); повышенное внутриглазное или внутричерепное давление (глаукома, отек диска, псевдоопухоль головного мозга).
Задний зрительный путь: первичная или метастатическая опухоль головного мозга или другой объемный процесс (абсцесс); иммунологические факторы (рассеянный склероз); инфекции (прогрессирующая многоочаговая лейкоэнцефалопатия), параселляр-ная опухоль (аденома гипофиза, краниофарингиома).
Дополнительное обследование: щелевая лампа (поражение глаза); периметрия (оценка изменений полей зрения); измерение внутриглазного давления (глаукома); МРТ головы (инфаркт или кровоизлияние в головной мозг, опухоль, демиелини-Зация, компрессионные повреждения тканей орбиты, зрительного нерва, хиазмы) электроретинография (дегенерация сетчатки); флюоресцентная ангиография (поражение сосудов сетчатки); люмбальная пункция (рассеянный склероз, псевдоопухоль мозга); зрительные, слуховые и соматосенсорные потенциалы (рассеянный склероз) СОЭ (височный артериит).
Нарушения движений глазных яблок
Диплопия
Наиболее частый симптом нарушения движений глаз. Причиной может быть поражение глазодвигательных нервов (III, IV, VI), нервно-мышечного синапса, наружных мышц глаза.
Дисфункция глазодвигательных нервов. При изолированном поражении глазодвигательных нервов выявляются следующие признаки:
III нерв — диплопия по горизонтали и вертикали; ограничение движений глазного яблока вверх и вниз; птоз верхнего века; зрачок расширен, реакция на свет отсутствует.
IV нерв — диплопия по вертикали при взгляде вниз; в покое глаз слегка поднят вверх, компенсаторный наклон головы.
VI нерв — диплопия по горизонтали; невозможность повернуть глаз кнаружи; в покое глаз повернут кнутри.
Наиболее частые причины изолированного поражения глазодвигательных нервов: диабетическая и идиопатическая вазопатии, вместе дающие около 1/2всех случаев. Другие частые причины: аневризма (особенно III нерв), опухоль (особенно IV нерв), травма (особенно VI нерв). Более редкие причины: синусит, сифилис, herpes zoster, повышенное внутричерепное давление (IV пара), ДБСТ или васкулит, менингит, саркоидоз.
Для изолированного поражения III нерва наиболее важно провести различие между инфарктом в результате вазопатии, нарушающей иннервацию зрачка, и сдав-лением задних соединительных артерий аневризмой, что почти всегда снижает зрачковый рефлекс. МРТ, МР-ангиография или церебральная ангиография могут потребоваться для дифференциации этих двух болезней.
Расстройства нервно-мышечной передачи. Myasthenia gravis более чем у 60 % больных проявляется глазными симптомами, диплопией и (или) птозом, а изолированная глазная симптоматика отмечается более чем у 90 % больных. Реакция зрачка всегда нормальна. Диагностически значима проба с Edrophonium chloride (10 мг внутривенно). [В России обычно проводится прозериновая проба. — Прим. ред.
Глазные миопатии. Диплопия в результате поражения глазодвигательных мышц может быть следствием воспалительного процесса (орбитальный миозит), инфильтрации (тиреоидная офтальмопатия), смещения тканей (травма орбиты). Диагноз подтверждают пробой с давлением на глазные яблоки, при которой оценивают механическое сопротивление анестезированного глазного яблока. Другие расстройства движений глазного яблока включают: Нистагм: ритмичные движения глаз; сам по себе нистагм не относится к патологическим симптомам, но может появиться при расстройстве взаимоотношений центральных и периферических вестибулярных функций.
Межъядерная офтальмоплегия — нарушение сочетанных движений глазных яблок при повреждении медиального продольного пучка в стволе головного мозга.
Надъядерные параличи взора — потеря произвольного контроля за движениями глаз по горизонтали или вертикали; происходит при нарушении нисходящих связей от коры головного мозга к стволу.
Можно ли вылечить неврит зрительного нерва при рассеянном склерозе?
Если к развитию неврита, поражающего зрительный нерв, привел рассеянный склероз, прогноз лечения во многом будет зависеть от ранней диагностики.
На сегодняшний день не существует специфической терапии РС, которая могла бы полностью избавить человека от этого заболевания, восстановить целостность оболочек нервных волокон. Если при РС диагностирован нисходящий неврит зрительного нерва, лечение этой патологии будет симптоматическим, а также направленным на подавление активности иммунной системы.
Полностью вылечить офтальмологическую патологию при сохранении основного аутоиммунного заболевания почти невозможно, но, если болезнь диагностирована своевременно, до необратимых изменений, есть шанс сохранить и восстановить зрение, уменьшить количество обострений и снизить выраженность симптоматики.
Лечение
Лечение рассеянного склероза направлено на решение нескольких задач:
- купирование активного иммуновоспалительного процесса,
- снижение активности иммунной системы к оболочкам нервных волокон,
- замедление процессов развития заболевания, приостановление появления новых «бляшек» ,
- борьбу с симптоматикой, существенно ухудшающей качество жизни.
Для решения проблем применяется медикаментозные препараты, физиотерапия.
Комплексная медикаментозная терапия
При лечении важен приём иммуномодуляторов и противовоспалительных препаратов. Особенно хорошо известны следующие лекарства:
- Интерфероны бета. Препараты обладают иммуномодулирующим действием на главные звенья иммунных реакций.
- Лекарства на основе глатирамера ацетата. Лекарства этой группы способны замещать антигены миелина и запускать процесс торможения Т1-лимфоцитов. Т2-лимфоциты при этом, наоборот, активизируются. За счёт этого препарат обладает нейропротекторным и противовоспалительным эффектом.
- Финголимод. Модулятор сфингозин-фосфатных рецепторов на мембранах лимфоцитов. Существенно снижает количество циркулирующих в крови «аутоагрессивных» Т-клеток.
- Натализум. Замедляет проникновение через гемато-энцефалический барьер и снижает в очагах аксонального повреждения активность Т-лимфоцитов. Существенно притормаживается воспалительный процесс.
При обострениях, когда болезнь сопровождается явными приступами, применяются адренокортикотропный гормон, кортикостероиды (метилпреднизолон). Благодаря этим препаратам удаётся достаточно быстро снизить движение иммунных клеток к спинному, головному мозгу. Но эти препараты хороши только как краткосрочная терапия. Для длительного применения они не подходят, так как способны вызвать зависимость.
Если заболевание сопровождается признаками депрессией, врачом может быть назначен амитриптилин, мелипрамин. Однако назначение этих препаратов производится крайне осторожно – только после детального обследования. Увы, у многих пациентов и так есть задержка мочи, а амитриптилин, мелипрамин способны изрядно усугубить ситуацию. Альтернативой для таких пациентов способны стать всевозможные селективные ингибиторы без холинолитических свойств, но с отличной способностью обратного захвата серотонина. Среди таких препаратов тразадон, сертралин, флуоксетин, пароксетин.
Также при наличии депрессии последние годы широко используется агомелатин. Это препарат с мелатонинэргическим механизмом действия. Он нормализует циркадианные ритмы (колебания).
При проблемах с мочеиспусканием нужна целенаправленная терапия, направленная на решение этой проблемы.
Если главная проблема – императивные позывы, применяется толтеродин оксибутинин, амитриптилин, нифедипин.
Если беспокойства связанны с опорожнением мочевого пузыря, выручает блокатор теразозин. Но важно, чтобы при приеме препарата был тщательный контроль за тем, чтобы не развилась ортостатическая гипотензия.
Некоторым пациентам также дополнительно могут назначаться препараты, направленные на снижение напряжения наружного сфинктера. Среди них – диазепам, тизанидин.
Вышеназванные препараты применяются в таблетированных и инъекционных формах.
Гипобарическая оксигинация
Большим подспорьем для пациентов с рассеянным склерозом является насыщение кислородом. Оно возможно посредством процедуры гипобарической оксигинации.
Особенно гипобарическая оксигинация актуальна для пациентов, у которых рассеянный склероз сопровождается кардиозаболеваниями, диабетом.
Гипобарическая оксигинация проводится в барокамере. Кислород подаётся под высоким давлением. В процессе гипобарической оксигинации активируются адаптационные и регенерационные механизмы.
Массаж
Отличное средство для уменьшения дискомфорта и болевых ощущений у пациентов с разными видами и стадиями склероза – это и массаж. Особенно массаж полезен для решения следующих задач:
- Расслабления мышц и снятия спастичности.
- Активизации кровообращения.
- Предотвращение пролежней. Актуально для лиц, которые вынуждены большинство времени проводить в кровати.
Диетотерапия при рассеянном склерозе
- Общим принципом для всех пациентов с рассеянным склерозом является ограничение в рационе источников быстрых углеводов. Главные из них – сахар, выпечка из рафинированной муки.
- Остальные принципы питания во многом зависят от того, какие конкретно проблемы у пациента в каждом конкретном случае.
- В случае затруднения жевания, рекомендуется употребляют пюреообразную пищу.
При наличии запоров стоит применять больше жидкой пищи (если одновременно нет проблем с мочевыделительной системой), продуктов с бифидобактериями.
Основные направления терапии нисходящего неврита
Многих пациентов волнует вопрос — если нет специфического лечения РС, какая именно терапия проводится при ретробульбарном неврите.
- Специалисты отмечают, что лечение ориентировано на достижение нескольких основных целей:
- затормозить активность иммунной системы, которая разрушает собственные клетки организма;
- изменить характер протекания рассеянного склероза;
- устранить или снизить выраженность офтальмологических симптомов; продлить периоды ремиссии, облегчить протекание периодов обострения.
Для достижения этих целей используются преимущественно медикаментозные методы.
Лечение ретробульбарного оптического неврита при РС
Правильный диагноз и установленная причина неврита позволяют назначить пациенту лечение. Если специалисты установили, что симптомы зрительного неврита вызваны рассеянным склерозом, то схема лечения может быть примерно следующей.
- Глюкокортикоидные препараты, в частности метилпреднизолон, назначают в остром периоде заболевания. Они оказывают мощное противовоспалительное действие, устраняют симптомы поражения зрительного нерва, замедляют продвижение клеток иммунной системы к мозгу, уменьшают количество антител в крови. Кортикостероиды используются преимущественно для купирования признаков неврита в период обострения. Как правило, лекарство вводят внутривенно в назначенной врачом дозе на протяжении от трех до семи дней. Впоследствии назначают оральный прием тех же глюкокортикоидов с постепенным снижением дозировки. Нужно учитывать, что повреждение зрительного нерва продолжается не только в период обострения, но и в стадии ремиссии, поэтому зачастую офтальмологи назначают курсы поддерживающей гормональной терапии и вне острой фазы заболевания.
- Противовоспалительные нестероидные средства применяются для уменьшения воспалительного процесса.
- Иммуномодуляторы или иммуносупрессоры позволяют подавить активность иммунной системы и тем самым снизить ее разрушающее действие на оболочки нервных волокон. Поскольку специфического лечения рассеянного склероза не существует, медикаментозное воздействие на иммунную систему становится одним из главных терапевтических методов.
Помимо перечисленных методов, схема лечения может включать дегидратационную терапию, назначение витамина В12, препаратов с антиоксидантным действием.
Патология глазного дна
Возрастная макулярная дегенерация
Возрастная макулярная дегенерация является одной из основных причин потери центрального зрения среди взрослого населения. Увеличение продолжительности жизни людей и повышение качества диагностики выводит это заболевание на первое место среди причин стойкого снижения зрения.
Причины возникновения и прогрессирования этого заболевания еще недостаточно хорошо изучены и в настоящее время все усилия врачей направлены лишь на стабилизацию патологического процесса и зрительных функций.
Заболевание включает в себя совокупность патологических изменений в центральной зоне сетчатки связанных с возрастом, которые можно подразделить на стадии или формы. В зависимости от формы и течения ВМД предлагаются различные способы лечения. Все методы лечения ВМД базируются на ранней и точной диагностике, поэтому на ранних стадиях заболевания адекватное лечение может остановить прогрессирование и продлить на годы активную деятельность, связанную с письмом и чтением наших пациентов.
Неэкссудативные формы ВМД являются начальным этапом заболевания, периодом предвестников. Как правило, снижения зрительных функций не происходит. На этом этапе важно динамическое наблюдение, антиоксиданты и ретинопротекторы в виде пищевых добавок.
Атрофические формы ВМД развиваются медленно, но неизбежно приводят к потери центрального зрения. Как правило, заболевание обнаруживают на обоих глазах, возможно с различной степенью выраженности. В настоящее время в качестве лечения проводят периодические курсы сосудистого и ретинопротекторного (улучшающее питание сетчатки) лечения. Пациентам рекомендуется пользоваться солнцезащитными очками на улице.
Экссудативные формы ВМД отличаются тяжелым течением и резким снижением зрения. На первых порах, до потери центрального зрения пациенты замечают искривление контуров предметов, прямых линий, текста. Все сложнее выполнять мелкую работу на близком от глаз расстоянии (шить, вязать, читать и писать). Причина кроется в быстром росте и высокой активности новообразованных сосудов, располагающихся под сетчаткой. Новообразованные сосуды имеют тонкую проницаемую стенку, что в итоге приводит к появлению отека (скопление жидкости под сетчаткой) и кровоизлияния в центральной зоне сетчатки. В конечной стадии ВМД происходит потеря центральных зрительных функций из-за развития атрофии или рубца, периферическое зрение, как правило, остается незатронутым. Все усилия в лечении экссудативной формы ВМД направлены на борьбу с новообразованными сосудами. В настоящее время широко вошло в практику применение анти-VEGF препаратов.
Эпиретинальный макулярный фиброз
Эпиретинальный макулярный фиброз может быть, как первичным заболеванием сетчатки, так и следствием (осложнением) других глазных заболеваний (воспалительных, сосудистых, травм и т.д.).
Чаще всего первичный эпиретинальный макулярный фиброз возникает после 50 лет, однако в последнее время наблюдается тенденция к «омоложению». Заболевание начинается с появления мембраны (тонкойпленки) на поверхности сетчатки, как правило в центральной зоне или около нее. Сокращаясь мембрана вызывает сморщивание и деформацию подлежащей сетчатки, а по мере уплотнения мембраны происходит выраженная деформация и даже частичная плоская отслойка сетчатки.
На начальных этапах развития эпиретинальный фиброз протекает бессимптомно. Это состояние не требует вмешательства, достаточно динамического наблюдения. По мере прогрессирования могут появиться искривление очертаний предметов и прямых линий и заметное снижение остроты зрения. В таких случаях целесообразно провести хирургическое вмешательство – отделение и удаление мембраны.
В редких случаях мембрана может самостоятельно отслоится, что приводит исчезновению всех симптомов.
Идиопатический макулярный разрыв
Идиопатический макулярный разрыв – это сквозной дефект ткани в центре сетчатки. Как правило возникает в возрасте старше 60 лет. Причина кроется в тракции фиксированной к центру сетчатки отслоенной задней гиалоидной мембраны. Заболевание развивается по стадиям, причем на ранних стадиях протекает асимптоматично. На более поздних стадиях пациент отмечает черное пятно перед глазом, часто выявляемое случайно при закрытии здорового глаза. Периферическое зрение не страдает. Для постановки диагноза часто достаточно только осмотра сетчатки, для документального подтверждения диагноза и уточнения стадии может потребоваться проведение оптической когерентной томографии. На первой стадии заболевания – угроза формирования макулярного отверстия – какое-либо лечение не проводится, так как на этой стадии может произойти спонтанное обратное развитие. На более поздних стадиях показано проведение хирургического вмешательства – задней витрэктомии с устранением тракционного фактора.
Центральная серозная хориоретинопатия
Это часто встречающаяся патология глазного дна, поражающая преимущественно молодых пациентов. Это заболевание идиопатическое и до сих пор многое в причинах и развитии этого заболевания остается неясным. Зрение обычно сильно не страдает. Пациенты часто жалуются на затуманивание зрения одного глаза, появление искривления контуров предметов и прямых линий. Диагностика не представляет каких – либо затруднений, однако для определения дальнейшей тактики лечения пациента показано проведение флюоресцентной ангиографии. Именно от результатов этого обследования зависит предложат ли Вам просто наблюдение и консервативное лечение, лазерное лечение или интравитриальное введение анти-VEGF препарата.
Диабетическая ритинопатия
Поражение органа зрения при сахарном диабете занимает особое место, так как существенно влияет на качество жизни людей. Причем из всех клинических проявлений диабетического поражения глаз наибольшую опасность представляет ретинопатия, являясь основной причиной прогрессирующего и безвозвратного снижения зрения вплоть до слепоты, которая у больных сахарным диабетом наступает в 25 раз чаще, чем в общей популяции.
Главным фактором развития и прогрессирования ДР является хроническая гипергликемия, т.е. высокий уровень сахара.
В настоящее время в большинстве европейских стран используется классификация, согласно которой выделяют три основных формы ретинопатии:
- непролиферативная ретинопатия;
- препролиферативная ретинопатия;
- пролиферативная ретинопатия.
Снижение остроты зрения при диабетическом поражении сетчатки происходит в результате трех причин. Во-первых, из-за наличия макулопатии (отек сетчатки в центральной зоне) может страдать центральное зрение. Во-вторых, на стадии пролиферативной ретинопатии кровоизлияния, которые возникают из новообразованных сосудов, вызывают резкое ухудшение зрения. В-третьих, образование, разрастание и сокращение фиброваскулярной ткани ведет к тракционной отслойке сетчатки, в результате чего происходит тяжелая и часто необратимая потеря зрения.
Своевременное выявление самых ранних проявлений диабета глаза является первоочередной задачей, так как на поздних стадиях процесса лечение уже малоперспективно.
Однако на начальных этапах диабета глаза патологические изменения в сетчатке не сопровождаются зрительными расстройствами, поэтому сами пациенты обращаются за медицинской помощью, как правило, поздно. В связи с этим большая ответственность возлагается на работу диспансерного офтальмологического наблюдения и на плечи самого пациента, серьезное отношение и ответственный подход которого будет способствовать сокращению имеющегося риска потери зрения при диабете глаза.
Существуют два основных направления в лечении диабетических поражений сетчатки:
Максимально стабильная компенсация сахарного диабета и непосредственное лечение диабетической ретинопатии.
Лазерная коагуляция сетчатки является единственно эффективным способом лечения диабетической ретинопатии. Лазеркоагуляция при диабетическом поражении сетчатки направлена на стабилизацию процесса, и повышение остроты зрения достигается далеко не всегда. При тяжёлой пролиферативной ретинопатии с развитием рецидивирующих кровоизлияний в стекловидное тело и тракционной отслойки сетчатки проведение лазерной коагуляции бесперспективно. В таких случаях может быть показано хирургическое лечение – витрэктомия.
При стойкой макулопатии разрабатываются схемы интравитриального введения анти – VEGF препарата.
Ретинит Коатса
Болезнь Коатса – это врожденное заболевание, в типичных случаях проявляющееся в детском возрасте у мальчиков и поражающее один глаз. Большинство случаев диагностируют до 20 лет с пиком выявляемости в конце первого десятилетия.
Поводом для обращения могут быть косоглазие, лейкокория или красный болящий глаз в далекозашедшей форме. Дети старшего возраста и реже взрослые могут обратиться с жалобами на снижение остроты зрения на одном глазу.
Диагноз обычно ставят на основании осмотра глазного дна – циклоскопии иногда может потребоваться проведение флуоресцентной ангиографии.
В легких случаях заболевания достаточно динамического наблюдения – осмотры раз в полгода. При прогрессирующем течении показаны многочисленные повторные сеансы лазерной коагуляции и требуется более тщательное наблюдение, так как в течении 5 лет после полной регрессии возможны рецидивы заболевания. При далекозашедшей стадии заболевания при развитии отслойки сетчатки показано оперативное лечение.
Болезнь Илза
Заболевание известно с 1880 года, когда впервые было описано возникновение повторяющихся кровоизлияний в стекловидное тело у молодых людей на фоне полного здоровья.
Болезнь Илза – это хроническое воспаление сосудов периферии сетчатки, сопровождающиеся повторными кровоизлияниями и постепенным снижением зрения. Заболевание преимущественно поражает представителей мужского пола среднего возраста и как правило двустороннее.
Пациенты жалуются на появление плавающих «мушек» или снижение остроты зрения одного глаза. В тяжелых случаях повторные кровоизлияния приводят к тракционной отслойке сетчатки и вторичной неоваскулярной глаукоме.
Медикаментозного лечения болезни Илза не существует. Гормональная терапия обычно не эффективна. Единственным эффективным методом лечения является вовремя проведенная лазерная коагуляция сетчатки, что позволяет стабилизировать патологический процесс и сохранить оставшееся зрение.
В ряде случаев при возникновении отслойки сетчатки возникает необходимость в проведении хирургического лечения.
Осмотр глазного дна – циклоскопия должна проводиться ежегодно. Описаны случай рецидива заболевания через десятки лет после кажущейся стабилизации процесса.
Тромбоз центральной вены сетчатки или её ветвей
Это состояние представляет собой острое нарушение кровообращения в центральной вене сетчатки или ее ветвях, угрожающее необратимым снижением зрения.
Заболевание обычно возникает у людей старше 50 лет на фоне артериальной гипертензии, сахарного диабета, атеросклероза, тромбофилии и других заболеваний крови.
Обычно пациенты отмечают одностороннее безболезненное резкое снижение зрения, возникшее на фоне повышенного артериального давления, после физической или эмоциональной нагрузки, после перегревания, приема алкоголя. Как правило пациенты могут четко указать, когда снизилось зрение. В зависимости от локализации процесса могут быть жалобы на появление пятна перед глазом, появление или увеличение плавающих «мушек», выпадение полей зрения, искажение контуров предметов.
Лечение следует начинать безотлагательно. Это экстренное состояние, требующее срочной госпитализации в стационар. Наилучший эффект будет наблюдаться при своевременном и комплексном лечении пациента прогноз для зрения будет во многом зависеть от остроты зрения при обращении. Для растворения тромба, окклюзирующего вену используют тромболитические препараты, которые эффективны только в первые семь дней от начала заболевания. В дальнейшем эффекта от их использования не будет.
Другим направлением комплексного лечения является максимальное снижение внутриглазного давления, рассасывающая терапия и антиоксиданты. При наличии диффузного отека в центре сетчатки решается вопрос о проведении решетчатой лазеркоагуляции. В последнее время успешно применяется интравитриальное введение анти – VEGF препарата, как метод лечения макулярного отека.
При угрозе появления новообразованных сосудов в следствии длительной ишемии сетчатки и развития неоваскулярной глаукомы, как осложнения тромбоза центральной вены сетчатки следует проводить панретинальную лазеркоагуляцию сетчатки, которая проводится в несколько сеансов. Целью лазерного лечения является не повышение зрительных функций, а предотвращение развития неоваскулярной глаукомы.
Окклюзия центральной артерии сетчатки
Заболевание представляет собой острую блокаду кровообращения в центральной артерии сетчатки тромбом. Как правило встречается у лиц старше 60 лет. В основе развития этого заболевания лежат разные причины, основные из них:
- артериальная гипертензия;
- атеросклероз;
- патология клапанов сердца;
- опухоли;
- глазной травматизм;
- системные заболевания.
Как правило пациенты отмечают острую одностороннюю и безболезненную потерю зрения, развивающуюся в течении нескольких секунд. Иногда до полной потери зрения наблюдаются эпизоды преходящей потери зрения.
Прогноз для зрения в дальнейшем как правило неблагоприятный. В большинстве случаях острота зрения остается на уровне светоощущения. Исключение составляет в случае дополнительного кровоснабжения области центральной ямки сетчатки цилиоретинальной артерии, когда острота зрения может восстановиться до исходного, но тем не менее имеются значительные потери в полях зрения.
Метода лечения с доказанной эффективностью в отношении остроты зрения не существует, однако это офтальмологическое неотложное состояние и теоретически, своевременное смещение тромба может предупредить развитие необратимых изменений зрения. Попытки сместить тромб имеют смысл в первые 48 часов от начала заболевания. Поэтому в данном случае необходимо срочно обратиться к офтальмологу за помощью, а на этапе доврачебной помощи проводить массаж глазного яблока, целью которого – вызвать сначала коллапс просвета сосуда, а потом резко его расширить. При необходимости пациент может проводить массаж глазного яблока самостоятельно по следующей технике.
- Голова пациента должна лежать низко, чтобы избежать ортостатического относительного ухудшения кровоснабжения сетчатки.
- Пальцами руки нажимают через закрытое веко на глазное яблоко.
- Глазное яблоко вдавливают в орбиту сначала слабо, затем с усилением и спустя 3-5 секунд внезапно отпускают.
- Через несколько секунд процесс повторяют.
Передняя и задняя ишемическая нейропатия
Заболевание, которое наиболее часто встречается у пожилых людей. В основе лежит частичный или полный инфаркт диска зрительного нерва или его ретроламилларной части, вызванный окклюзией сосудов, питающих зрительный нерв.
Факторами риска развития являются артериальная гипертензия, сахарный диабет, гиперхолистеринемия, коллагенозы, антифосфолипидный синдром, гипергомоцистеинемия, внезапные гипотензивные состояния и т.д.
Начало заболевания чаще всего проявляется внезапной односторонней потерей или значительным снижением зрения без каких-либо предшествующих зрительных нарушений. Снижение зрения, как правило, обнаруживается при пробуждении, что указывает на вероятную связь с ночной гипотонией.
Врачебная помощь направлена на восстановление и улучшение кровообращения в системе питающей зрительный нерв и предотвращения развития полной атрофии зрительного нерва.
Застойный диск зрительного нерва
Застойный диск зрительного нерва характеризуется отеком, развивающимся на фоне повышения внутричерепного давления. Застойный диск почти всегда двусторонний. Обычно зрительные нарушения проявляются только на стадии атрофии зрительного нерва (далекозашедшей), поэтому часто застойный диск зрительного нерва является диагностической находкой во время обследования у офтальмолога.
Клиническими проявлениями повышенного внутричерепного давления могут быть головная боль, внезапная тошнота и рвота, нарушение сознания, преходящие эпизоды помутнения зрения и двоение изображения.
Причины повышения внутричерепного давления:
- Обструкция системы желудочков (врожденная или приобретенная)
- Объемные внутричерепные образования, включая гематомы
- Менингит, субарахноидальное кровоизлияние, перенесенные травмы сопровождающиеся диффузным отеком мозга
- Тяжелая системная артериальная гипертензия
- Идиопатическая внутричерепная гипертензия
- Гиперсекреция цереброспинальной жидкости опухолью сосудистых сплетения мозга.
Все пациенты с застойными дисками должны быть обследованы невропатологом и нейрохирургом для исключения внутричерепных образований.
Неврит зрительного нерва
Неврит зрительного нерва – это поражение зрительного нерва вследствие воспалительного, инфекционного или демиелинизирующего процесса.
Демиелинизирующий неврит встречается наиболее часто при рассеянном склерозе. Начало заболевания проявляется подострым односторонним снижением зрения. Иногда снижение зрения сопровождают точечные белые или цветные вспышки или искры. Часто наблюдаются боли при движении глаза или дискомфорт, которые предшествуют снижению зрения и длятся обычно несколько дней. В большинстве случаев появляются дефекты в поле зрения.
Ухудшение зрительных функций продолжается от нескольких дней до двух недель в дальнейшем восстановление зрения происходит в течении полугода. При повторных атаках развивается атрофия зрительного нерва.
Несмотря на то, что у некоторых пациентов с невритом зрительного нерва отсутствуют признаки клинически выявляемого системного демиелинизирующего заболевания, следующий ряд наблюдений указывает на тесную связь неврита зрительного нерва с рассеянным склерозом.
У пациентов с невритом зрительного нерва и исходно нормальной картиной МРТ головного мозга риск развития рассеянного склероза в течении последующих 5 лет составляет 16%, а у пациентов с установленным рассеянным склерозом неврит зрительного нерва развивается в 70% случаев.
Учитывая все вышесказанное при постановке диагноза неврит зрительного нерва врач обязательно направит вас на МРТ головного мозга.
Предлагаемое лечение гормональными препаратами и интерфероном позволяет ускорить выздоровление до 2-3 недель. Однако лечение не влияет на конечную остроту зрения.
Неврит зрительного нерва при инфекционных заболеваниях встречается значительно реже. Причиной может служить заболевания придаточных пазух носа. Такой неврит характеризуется повторяющимися эпизодами одностороннего снижения зрения, сильными головным болями и признаками синусита. В данном случае лечение проводится совместно с отоларингологом. Терапия – местное и системное применение антибиотиков.
Основной причиной параинфекционного неврита зрительного нерва является вирусная инфекция. Кроме того он может развиться после вакцинации. У детей эта форма неврита встречается гораздо чаще, чем у взрослых. Заболевание развивается обычно через 1-3 недели после вирусной инфекции и снижение зрения сопровождается неврологической симптоматикой (головная боль, аттаксия).
Лечение, как правило, не требуется ввиду благоприятного прогноза, предполагающего быстрое восстановление зрительных функций. Однако при выраженном или двустороннем поражении показана гормональная терапия.
Хориоретинальные воспалительные заболевания (хориоретиниты)
Причины хориоретинита могут быть инфекционные и неинфекционные.
Среди инфекционных причин развития хориоретинита наиболее частой является токсоплазмоз. Возбудитель заболевания – внутриклеточный паразит, обитающий в кишечнике у кошек.
Чаще всего заболевание выявляют у молодых, здоровых взрослых людей, приходящих к врачу с жалобами на снижение зрения и плавающие помутнения перед глазом, фотофобию. При локализации очага воспаления в центральной зоне сетчатки значительно страдает центральное зрение.
Кроме токсоплазмоза инфекционной причиной хориоретинита могут быть: токсокароз, цитомегаловирус, вирус герпеса, вторичный сифилис, кандидоз, гистоплазмоз, туберкулез.
При достоверно установленном диагнозе, подтвержденным лабораторными методами исследования лечение проводит инфекционист.
Наследственные дистрофические и дегенеративные заболевания сетчатки
Пигментный ретинит -группа наследственных дистрофических заболеваний сетчатки, характеризующихся субъективно ночной слепотой и потерей периферического зрения. Почти четверть всех больных сохраняет высокую остроту зрения и способность читать на протяжении всей жизни. Однако необходимо ежегодное обследование для выявления значительного падения остроты зрения, которое может быть вызвано потенциально устранимой причиной, такой как кистозный отек макулы или катаракта.
Болезнь Штаргардта – это наиболее распространенная форма генетически – наследуемой дистрофии сетчатки, возникающей в юношеском возрасте. Начало заболевания приходится на возраст 10-20 лет. Происходит двустороннее постепенное снижение центрального зрения. У большинства пациентов сохраняется средняя острота зрения по крайней мере на одном глазу.
Болезнь Беста – редкое наследственное дистрофическое заболевание сетчатки. Заболевание обычно медленно прогрессирует, проходя пять стадий и заканчивается атрофией макулы с потерей центрального зрения. В основном прогноз достаточно хороший, так как большинство пациентов сохраняют зрение, достаточное для чтения, по крайней мере на одном глазу на протяжении всей жизни. Если имеет выраженное снижение зрения, это обычно происходит медленно и начинается после 40 лет.
Альбинизм – группа генетически – наследуемых заболеваний, в основе которых лежит нарушение синтеза пигмента меланина и которые могут характеризоваться либо изолированным глазным поражением(глазной альбинизм), либо системным поражением глаз, кожи и волос.
Важные клинические признаки это
- Низкая острота зрения
- Маятникообразный горизонтальный нистагм
- Красный оттенок радужки.
Патогенетически обоснованного лечения наследственных заболеваний сетчатки не существует. Существует мнение и несколько эксперементально-клинических работ указывающих на положительную динамику и стабилизацию дистрофического процесса сетчатки при периодическом применении препаратов — тканевых биорегуляторов.
Отслойка сетчатки
Это отделение сетчатки от подлежащего слоя пигментного эпителия. Основные типы отслойки сетчатки: регматогенная, экссудативная, тракционная.
Регматогенная отслойка сетчатки возникает вторично на фоне сквозного разрыва сетчатки, в результате чего жидкость из стекловидного тела поступает под сетчатку. Разрывы сетчатки являются распространенным состоянием, чаще возникают при миопии, артифакии и после травмы. Во многих случаях разрывы двусторонние и множественные, возникают на фоне дегенеративных аномалий, аномалий развития и травм.
Многие разрывы протекают бессимптомно, иногда разрывы проявляются плавающим помутнением перед глазом и вспышками света, не влияя на остроту зрения. Однако если развивается отслойка сетчатки, происходит прогрессирующая потеря поля зрения.
Около 60% всех разрывов возникают на фоне специфических изменений – периферических дегенераций. Это патологически тонкие участки сетчатки, в которых спонтанно формируются разрывы. Периферические дегенерации сетчатки, предрасполагающие к отслойке сетчатки (решетчатая, «след улитки», дегенеративный ретиношизис) как и разрывы подлежат лазерной коагуляции в целях профилактики регматогенной отслойки сетчатки.
Регматогенные отслойки подлежат хирургическому лечению, причем послеоперационный прогноз для зрения зависит от давности заболевания и распространенности отслойки. Если отслойка сетчатки не захватывает центральную (макулярную зону) и свежая, послеоперационные прогнозы на восстановление зрения относительно высокие.
Экссудативная отслойка сетчатки представляет собой отслоение сетчатки вследствие интраретинального или субретинального просачивания жидкости.. По определению такая отслойка не связана с ретинальным разрывом. Необходимо искать признаки основной причины экссудации(просачивания) жидкости, такие как воспаление, сосудистые изменения или опухоли. В зависимости от причин экссудации применяется этиопатогенетическое лечение.
Основными причинами тракционной отслойки сетчатки являются: пролиферативная диабетическая ретинопатия, ретинопатия недоношенных, проникающая травма заднего сегмента глаза. Это наиболее тяжелое осложнение основного заболевания, приводящее к слепоте. В таких случаях показано хирургическое лечение.
Существуют ли меры профилактики?
Если воспаление зрительного нерва связано с рассеянным склерозом, то врачи рекомендуют, помимо обязательного лечения, придерживаться и некоторых профилактических мер. Цель профилактики в данном случае — предупреждение периодов обострения.
Чтобы контролировать факторы риска при данном заболевании, важно придерживаться нескольких рекомендаций.
- избегать любых инфекций или травм;
- контролировать эмоциональное состояние, избегать стрессов;
- не допускать длительного пребывания на солнце, перегревания или переохлаждения;
- отказаться от курения и употребления других токсичных веществ.
Вылечить рассеянный склероз и сопутствующий ему неврит невозможно, но взять патологические состояния под контроль, облегчить симптомы, замедлить прогрессирование, сохранить зрение возможно при условии ранней диагностики, корректного лечения и соблюдения профилактических мер.
Лечение рассеянного склероза
Лечение рассеянного склероза направлено на предотвращение или замедление инвалидизации, улучшение качества жизни, предотвращение развития осложнений.
С момента установления диагноза всем пациентом показано назначение препаратов, изменяющих течение рассеянного склероза (ПИТРС). К этой группе препаратов относятся глатирамера ацетат, интерфероны, моноклональные антитела.
Пациентам также показана симптоматическая терапия. Назначаются глюкокортикоиды, препараты, улучшающие микроциркуляцию крови, ноотропы, миорелаксанты, антидепрессанты, слабительные, м-холинолитики.
При рассеянном склерозе рекомендовано проведение физиотерапии и ЛФК, а также соблюдение диеты (ограничение употребления животных жиров, преобладание в рационе полиненасыщенных жирных кислот, достаточное потребление витаминов и минеральных веществ).
Ранняя диагностика рассеянного склероза и адекватное лечение специализированными препаратами позволяет замедлить негативные проявления заболевания и оттянуть наступление критических поражений нервной системы. Прогноз заболевания в случае отказа от лечения крайне неблагоприятный. Так, через 15-20 лет 2/3 пациентов имеют трудности при самообслуживании, а 1/3 пациентов не способны к самостоятельному передвижению. Благодаря появлению специальных препаратов, замедляющих прогрессирование рассеянного склероза, стало возможным предупреждать обострения, снижать выраженность и распространенность симптомов, что значительно замедляет инвалидизацию.