24.11.2016
Пинчук Елена Анатольевна
Заместитель главного врача по лечебной работе, кмн, врач-невролог, врач физической и реабилитационной медицины
Белкин Владимир Андреевич
Заведующий отделением ранней медицинской реабилитации, врач физической и реабилитационной медицины, врач-невролог
Липовка Надежда Сергеевна
Заведующий отделением медицинской реабилитации, врач физической и реабилитационной медицины, врач-невролог
Соболев Аркадий Игоревич
Врач физической и реабилитационной медицины, врач-невролог
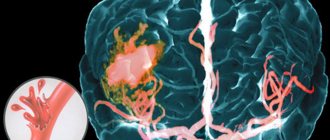
Ишемический инсульт имеет несколько стадии течения. Первая стадия – это острый период ишемического инсульта, который длится до 21-го дня. На протяжении первых 3-5 дней развивается перифокальный отек головного мозга, клетки кариоплазмы и цитоплазмы сморщиваются.
Важным моментом в острый период ишемического инсульта является правильно провести диагностику. Прежде всего, необходимо отграничить любые другие заболевания нервной системы от инсульта. Далее определяют характер самого инсульта, и чем он вызван (кровоизлияние в коре головного мозга или тромб сосуда). На последнем этапе диагностики определяют локализацию очага поражения, а также патогенез инфаркта головного мозга при инсульте.
Этапы диагностики острого периода
- 1 этап. Пострадавший срочно госпитализируется. Основную информацию врач получает со слов больного, его родственников или окружающих людей. Внешние признаки нарушения мозгового кровообращения, эмоциональный фон, физическое напряжение, уровень артериального давления позволяют достаточно быстро и точно поставить диагноз. Изучается история болезни пациента на наличие других заболеваний, которые могут провоцировать развитие ишемического инсульта (аритмия, атеросклероз, ранее перенесенный инфаркт и т.д.). Однако возможность постановки неправильного диагноза существует при эпилептическом припадке больного, опухоли головного мозга, травме головы, при гипогликемическом состоянии и др.
- 2 этап. Самым важным моментом этого этапа является быстро и точно определить характер заболевания. От этого будет зависеть тактика оказания первой помощи и дальнейшего лечения. Проводится компьютерная томография головного мозга, так как только одна клиническая картина не может дать полностью достоверную информацию.
- 3 этап. После того как быстро собран анамнез, выявлена клиническая картина и проведена КТ, врач приступает к выбору тактики лечения. Также определяется подтип инсульта (лакунарный, атеротромботический или кардиоэмболический и т.д.). Правильный выбор терапии поможет не только своевременно оказать пострадавшему помощь, включая хирургическую, но и предупредить возможное повторение инфаркта в будущем.
Поздний восстановительный период
Данный период инсульта по времени наступает позже всего – через полгода после острого – и продолжается до двух лет. Обычно на этой стадии пациенты уже могут себя обслуживать, у них восстанавливается речь и основные функции организма. Основное внимание уделяется мелкой моторике, упражнениям, которые закрепляют новые функции за теми участками мозга, которые не пострадали во время инсульта.
Через год врачи говорят о периоде отдаленных последствий. Пациенты должны раз в год обязательно проходить профилактическое обследование и при возможности – лечение.
Если пациент или окружающие вовремя обратили внимание на первые симптомы инсульта и незамедлительно обратились к врачу, шансы на восстановление важнейших функций заметно возрастают. Ведь важнее всего наладить нормальное кровоснабжение мозга в первые часы после приступа. Именно это гарантирует минимальное поражение нервной ткани и сохранность функций.
Терапия при ишемическом инсульте в острый период
В первые три недели (время протекания острого периода) предпринимаются мероприятия общего характера:
- Поддерживается необходимый уровень кислорода;
- Артериальное давление стабилизируется;
- Под наблюдением врача находится сердечная деятельность;
- Контролируются состояние мочевого пузыря, кишечника;
- Проводится пассивная гимнастика всех конечностей пострадавшего;
- Профилактика пролежней;
- Антибактериальная терапия, включающая прием противогрибковых препаратов.
В зависимости от специфики и подтипа ишемического инсульта проводится специальная терапия.
Острый ишемический инсульт может повториться, если диагноз оказался не достоверным и не все экстренные мероприятия были проведены. Большую опасность представляет в острый период вторичное кровоизлияние в поврежденную ткань коры головного мозга. Как правило, это происходит в первые 10 дней с момента наступления инсульта. Выявить это осложнение визуально практически невозможно. Только с помощью компьютерной томографии и рентгенологического исследования находят новый очаг поражения и принимают меры. Причиной такого осложнения является отсутствие необходимого контроля над артериальным давлением, а также проведение реперфузионной терапии. Некоторые пациенты имеют серьезные противопоказания для ее проведения.
Клинический институт мозга Рейтинг: 4/5 — 2 голосов
Поделиться статьей в социальных сетях
Ведение больных в раннем восстановительном периоде инсульта
Е.Ю. СУСЛОВА
,
Н.В. ВАХНИНА
, к.м.н.,
кафедра нервных болезней и нейрохирургии Первого МГМУ им. И.М. Сеченова, Москва
Представлен обзор основных факторов риска ишемического инсульта, принципов ведения больных в раннем восстановительном периоде ишемического инсульта. Особое внимание уделено вторичной профилактике повторного инсульта и применению нейропротекторных препаратов в составе комплексного лечения пациентов, перенесших инсульт.
Актуальность проблемы
Острые нарушения мозгового кровообращения (ОНМК) представляют собой одно из наиболее распространенных патологических состояний в неврологической практике [1]. По данным Всемирной федерации неврологических обществ, ежегодно в мире регистрируется не менее 15 млн инсультов [1]. При этом считается, что далеко не все ОНМК регистрируются, и реальная цифра намного больше. В РФ регистрируется более 400 000 инсультов ежегодно, при этом инсульты составляют около 19% в структуре общей смертности [2, 3]. Около 30% инсультов приводят к смерти в остром периоде заболевания [1, 4—6]. Инсульт сокращает длительность предстоящей жизни мужчин на 1,62—3,41, женщин — на 1,07—3,02 года [3].
Этиология и патогенез ишемического инсульта
Согласно общепринятой классификации TOAST (Adams H.P. et al., 1993), в настоящее время выделяют 5 патогенетических подтипов ишемического инсульта (ИИ):
— атеротромбоэмболический, — кардиоэмболический, — лакунарный (вследствие окклюзии мелкого сосуда), — инсульт другой установленной этиологии, — инсульт неустановленной этиологии. В результате многочисленных эпидемиологических исследований, проводимых в последние годы, были выявлены факторы, увеличивающие риск развития ИИ, среди которых выделяют неизменяемые и изменяемые (табл. 1
).
| Таблица 1. Неизменяемые и изменяемые факторы риска ИИ | |
| Неизменяемые факторы риска ИИ | Изменяемые факторы риска ИИ [5 ] |
|
|
Ведение больного в острейшем периоде должно осуществляться в специализированном отделении стационара (первичное сосудистое отделение). Далее, в раннем восстановительном периоде (РВП), для реабилитации больной может переводиться в специализированные стационарные или амбулаторные центры или выписываться домой. Цели лечения больного в РВП включают восстановление утраченных двигательных, речевых и других функций, вторичную профилактику инсульта у конкретного больного, социальную и психологическую помощь.
Вследствие перенесенного ИИ у 15—30% развивается стойкая инвалидность и у 40% — умеренное восстановление [4, 7]. Восстановление способности к самообслуживанию и самостоятельной жизни во многом зависит от варианта неврологического дефекта. При наличии только гемипареза зачастую пациенты могут самостоятельно передвигаться и жить без посторонней помощи. Даже если добавляются чувствительные расстройства, помощь необходима, как правило, только частично. Если же у пациента в результате ИИ развилась гемианопсия, часто может требоваться посторонняя помощь при передвижении. Прогноз значительно ухудшается при формировании выраженных когнитивных расстройств, афазии, анозогнозии, депрессии, болевого синдрома, грубых бульбарного или псевдобульбарного синдромов [5].
Восстановление неврологического дефицита включает в первую очередь активизацию больного [7]. Постоянная двигательная нагрузка приводит к уменьшению моторного дефицита: при регулярных прогулках улучшается ходьба, специализированная гимнастика помогает восстановить функции рук. Возможно использование ортезов при парезе стопы, миорелаксантов при развитии грубой спастичности. Целью двигательной реабилитации является достижение максимальной независимости пациента, для чего, прежде всего, необходимо восстановление бытовых навыков пациента (одевание, туалет, прием пищи, передвижение по дому и по улице). Для уменьшения выраженности речевых нарушений высокоэффективны логопедические занятия.
Когнитивные нарушения могут значительно ухудшать прогноз пациента в плане реабилитации, качества и продолжительности жизни, кроме того, они снижают приверженность пациента к терапии [5, 8]. В течение 1 года после перенесенного инсульта у 25—30% пациентов формируется деменция, при этом у ⅓ из них она связана с декомпенсацией сопутствующих нейродегенеративных изменений головного мозга [9]. Для улучшения памяти и других когнитивных функций у пациентов с умеренными и легкими когнитивными нарушениями рекомендуют как достаточную умственную нагрузку, тренировку памяти, так и использование лекарственных препаратов. При когнитивных расстройствах, достигающих степени деменции, применяются ацетилхолинергические (донепезил, галантамин, ривастигмин) и глутаматергические (мемантин) препараты. На фоне применения данных лекарственных средств отмечается уменьшение когнитивных и других нервно-психических расстройств. Ингибиторы ацетилхолинэстеразы уменьшают ацетилхолинергический дефицит, возникающий на фоне поражения центральных ацетилхолинергических структур, а мемантин нормализует паттерн передачи импульсов в глутаматергических синапсах. Выбор конкретного лекарственного средства определяется тяжестью и характером когнитивных нарушений, наличием сопутствующих заболеваний, переносимостью лекарственных препаратов.
Примерно у 60% пациентов в постинсультном периоде развивается депрессия, которая также является фактором риска повторных инсультов, инфаркта миокарда, ухудшения когнитивных функций [4]. Всем пациентам с постинсультной депрессией рекомендуется рациональная психотерапия и назначение антидепрессантов (трициклических или селективных ингибиторов обратного захвата серотонина) с их индивидуальным подбором в каждом конкретном случае. Адекватное лечение депрессии имеет важное значение для улучшения качества жизни пациентов и их родственников, а также для снижения летальности в течение нескольких лет после перенесенного инсульта [4].
Вторичная профилактика ИИ
Вторичная профилактика ИИ у пациентов, перенесших инсульт или транзиторную ишемическую атаку (ТИА), имеет огромное значение. Максимальный риск повторного ИИ отмечается в первые дни после ТИА или ИИ, поэтому начало профилактических мероприятий должно приходиться на острейший период и продолжаться в восстановительном периоде ОНМК. Вторичная профилактика ИИ включает в себя в первую очередь коррекцию факторов риска и осуществляется с помощью нелекарственных, лекарственных и хирургических методов.
Нелекарственные методы включают отказ от вредных привычек — курения и приема алкоголя, диету, дозированную физическую нагрузку. Отказ от курения или уменьшение числа выкуриваемых сигарет (даже у курильщиков с многолетним стажем) достоверно снижает риск повторного ИИ и инфаркта миокарда. Прекращение приема алкоголя снижает риск повторного ИИ и кровоизлияния в мозг.
Увеличение физической активности с регулярными аэробными нагрузками способствует улучшению состояния сердечно-сосудистой системы больных, перенесших инсульт. Первое место занимают пешие прогулки или лечебная гимнастика дома (при наличии неврологического дефекта, затрудняющего ходьбу). Пациенту рекомендуется постепенное достижение уровня доинсультной физической активности или ее превышение, если до инсульта наблюдалась гиподинамия. Кроме того, физические нагрузки способствуют снижению артериального давления (АД), избыточной массы тела, уровня холестеринемии [5]. Целесообразна диета с низким содержанием холестерина, при сопутствующем сахарном диабете – контроль уровня гликемии и соответствующее питание. Снижение избыточной массы тела способствует снижению АД, уровня холестерина и глюкозы в крови.
Антитромботическая терапия включает назначение антитромбоцитарных средств при некардиоэмболическом инсульте (атеротромботическом, лакунарном, инсульте неясной этиологии) и непрямых антикоагулянтов — при кардиоэмболическом.
Результатом действия антитромбоцитарных средств является снижение агрегации тромбоцитов, что препятствует их фиксации на атеросклеротической бляшке и, как следствие, формированию тромба. Доказано, что длительный прием антитромбоцитарных средств у пациентов, перенесших ИИ или ТИА, достоверно снижает риск развития повторного инсульта. Целесообразно назначение антитромбоцитарных средств с доказанной антиагрегантной активностью. К таким средствам относят ацетилсалициловую кислоту в дозе 75—325 мг/сут, клопидогрел в дозе 75 мг/сут, комбинацию 25 мг аспирина и 200 мг дипиридамола замедленного высвобождения. В нескольких крупных исследованиях показана более высокая эффективность клопидогрела и комбинации аспирина с дипиридамолом замедленного высвобождения по сравнению с аспирином [10].
В качестве вторичной профилактики ИИ у больных, перенесших кардиоэмболический инсульт (т. е. страдающих фибрилляцией предсердий, клапанными пороками) и имеющих внутрижелудочковый тромб или другие факторы риска кардиальной эмболии, применяются антикоагулянты. Золотым стандартом антикоагулянтной терапии долгое время являлся варфарин, дозу которого необходимо постепенно подбирать, а затем корректировать в зависимости от показателя международного нормализованного отношения (МНО). При приеме варфарина МНО должно измеряться 1 раз в 2 нед. и поддерживаться в диапазоне от 2 до 3 [9, 10]. В последние годы у пациентов с фибрилляцией предсердий активно разрабатывались и исследовались оральные антикоагулянты, не требующие регулярного контроля показателя МНО и не уступающие по своей эффективности варфарину: дабигатран, ривароксабан и апиксабан. Эти препараты значительно более удобны для применения пациентами, имеют сходные с варфарином эффективность и безопасность. Однако использование этих препаратов ограниченно ввиду их высокой стоимости [5, 10].
Коррекция дислипидемии требует назначения статинов на длительное время. Статины применяются как для вторичной, так и для первичной профилактики инсульта у пациентов с высоким риском развития ИИ. Эти препараты достоверно снижают вероятность развития не только ишемических ОНМК, но и инфаркта миокарда у больных, страдающих ишемической болезнью сердца, сахарным диабетом или перенесших ИИ даже при нормальном уровне холестерина в крови [5, 9, 11, 12]. Основное значение имеет снижение уровня холестерина липопротеидов низкой плотности, замедление прогрессирования атеросклероза.
Нормализация АД — одно из наиболее действенных направлений вторичной профилактики ИИ. Согласно метаанализу рандомизированных исследований при эффективной терапии артериальной гипертензии (АГ) возможно предупреждение 30—40% повторных инсультов [5]. В нескольких крупных исследованиях показано, что контроль АД не только снижает вероятность повторного инсульта, но и способствует уменьшению выраженности и темпа прогрессирования постинсультных когнитивных нарушений. Как уже упоминалось выше, регулярные физические нагрузки и диета могут способствовать снижению АД, также полезно уменьшение количества соли в пище. Лекарственная терапия АГ достоверно снижает риск развития повторного инсульта, инфаркта миокарда и смерти от сердечно-сосудистой патологии [5, 13, 14]. При этом в исследованиях показали свою эффективность ингибиторы ангиотензинпревращающего фермента (иАПФ), диуретики и их комбинация [13—15]. Выбор антигипертензивного средства также зависит от сопутствующих заболеваний пациента. Результаты исследований показывают, что даже небольшое стабильное снижение АД (на 5/2 мм рт. ст.) может значительно снижать риск повторного ИИ (на 29%) [5, 16]. Результаты исследования PROGRESS показали, что у больных, перенесших инсульт или ТИА, использование комбинации периндоприла 4 мг/сут и индапамида 2,5 мг/сут в течение четырех лет приводит к уменьшению риска развития повторного инсульта в среднем на 28% [12, 13]. На основании исследования PROGRESS пациентам, перенесшим ИИ или ТИА, рекомендовано назначение антигипертензивной терапии даже при нормальном уровне АД [5, 7]. Таким образом, пациентам, перенесшим ИИ или ТИА, рекомендуется постепенно в течение нескольких месяцев снизить АД до нормальных значений — ниже 140/90 мм рт. ст. При отсутствии гемодинамически значимых стенозов магистральных артерий головы (менее 70%) целевые цифры АД должны быть не выше 130/85 мм рт. ст.; при сопутствующих сахарном диабете и почечной недостаточности целесообразно более значительное снижение АД ниже 130/80 мм рт. ст. [5, 7]. При наличии более выраженного стеноза (70% и более) хотя бы одной магистральной артерии головы пациент должен быть консультирован ангиохирургом для решения вопроса о возможном хирургическом лечении (каротидной эндартерэктомии, в более редких случаях — стентировании). При выявлении стеноза более 70% в каротидном бассейне на стороне заинтересованного полушария у пациента, перенесшего ИИ или ТИА, хирургическое лечение в ранние сроки (в первые 2—3 нед.) имеет преимущества над консервативным ведением пациентов. При стенозе менее 70% или в поздние сроки (спустя 6 мес.) преимущества хирургического лечения сомнительны.
Нейропротекторная, ноотропная терапия в течение многих лет представляет большой интерес для врачей. Эти препараты должны уменьшать повреждающие эффекты патологических процессов, которые протекают в веществе мозга при его ишемии (активация возбуждающих аминокислот и внутриклеточных протеаз, выход кальция во внеклеточное пространство, апоптоз, повреждение клеточных мембран). В экспериментальных исследованиях на животных и in vitro были получены данные об эффективности многих лекарственных средств из группы нейропротекторов.
В качестве лекарственных средств у пациентов, перенесших инсульт и имеющих умеренные когнитивные расстройства сосудистой или смешанной природы, могут использоваться препараты гинкго билоба (по 120 мг/сут), холина альфосцерат (1 000 мг/сут), пирацетам (по 1 200—2 400 мг/сут), винпоцетин (30 мг/сут) и др.
К сожалению, пока отсутствуют результаты крупных рандомизированных плацебо-контролируемых многоцентровых исследований, которые доказали бы эффективность этих лекарственных средств у пациентов, перенесших инсульт. Заслуживает внимания новый для России лекарственный препарат Дузофарм (), действующим веществом которого является нафтидрофурил.
Механизм действия препарата Дузофарм связан с селективной блокадой серотониновых рецепторов класса 5-HT2 (5-гидрокситриптаминовых). Взаимодействие серотонина с этими рецепторами приводит к сокращению гладкой мускулатуры сосудов [17], агрегации тромбоцитов и повышению проницаемости сосудов (Kirsten et al., 1995). При этом уменьшение церебрального кровотока, индуцируемое серотонином [22], более выражено на уровне коллатеральных сосудов, состояние которых играет решающую роль в ограничении распространения зоны некроза.
Дузофарм, блокируя серотониновые рецепторы 5-НТ2, предотвращает спазм артериол, агрегацию тромбоцитов и уменьшает проницаемость сосудов, а также улучшает коллатеральный кровоток и ограничивает распространение зоны инфаркта [23].
Эффекты серотонина, реализуемые через серотониновые рецепторы класса 5-НТ2, играют исключительно важную роль в развитии главных событий в очаге сосудистой катастрофы головного мозга. Повышение агрегации тромбоцитов, разрушение гематоэнцефалического барьера, а также высвобождение серотонина из поврежденных тканей способствуют значительному повышению уровня этого медиатора в зонах «сосудистой катастрофы». Эндотелий в условиях ишемии теряет способность поглощать серотонин, и его концентрация значительно возрастает. Кроме этого, выявлена прямая зависимость между поглощением серотонина и степенью гипоксии [24]. Эти факты свидетельствуют о чрезвычайно выраженной негативной роли серотонина в усугублении ишемической картины, что способствует увеличению зоны инфаркта в остром периоде ишемии и способствует формированию «замкнутого» круга, препятствующего восстановлению кровотока в постишемическом периоде.
Не менее важно развитие реакции гиперчувствительности к серотонину, возникающей со стороны сосудов, проходящих через ишемизированные ткани, в результате чего у пациентов в постинсультном периоде наблюдается сильная реакция на серотонин, которая становилась еще более интенсивной при увеличении продолжительности восстановительного периода [25]. Этот факт свидетельствует, что гиперчувствительность серотонинергической системы сохраняется длительное время и может сыграть решающую роль при развитии повторного инсульта [25]. Среди предпосылок к развитию повышенной чувствительности к серотонину необходимо отметить атеросклероз и гипертензию.
Нафтидрофурил более двух десятилетий успешно применяется в лечении острой и хронической нейрососудистой патологии.
Дузофарм, в отличие о других сосудистых препаратов, действует только в зонах ишемии и не распространяется на интактные сосуды — это позволяет исключить синдром «обкрадывания» и влияние на системное артериальное давление, что представляется важным преимуществом в терапии пациента с нарушением церебрального кровотока. Помимо сосудистых эффектов, Дузофарм обладает ноотропным и анксиолитическим действием, что позволяет рассматривать его применение как комплексную терапию, затрагивающую ключевые патологические процессы как в остром периоде ИИ, так и в периоде реабилитации.
Нафтидрофурил имеет обширную доказательную базу в терапии сосудистой патологии: проведено более 18 рандомизированных плацебо-контролируемых исследований.
Нафтидрофурил в исследованиях in vitro приводил к прекращению агрегации тромбоцитов и повышению уровня метаболизма в поврежденной мозговой ткани [13, 18, 19].
Нафтидрофурил улучшает функциональное состояние активности нейронов у взрослых здоровых добровольцев: через 5 дней терапии на функциональной МРТ сигнал от правой лобной доли, средней и нижней лобных извилин, обеих височных долей и участков затылочных долей был более интенсивным у испытуемых, получавших нафтидрофурил, по сравнению с получавшими плацебо. На ЭЭГ при этом отмечались изменения, в частности уменьшение альфа-активности [18].
Применение нафтидрофурила сокращает пребывание больного с острым инсультом в стационаре [20]. В обзоре 4 плацебо-контролируемых исследований показана эффективность добавления нафтидрофурила к стандартной терапии в подостром периоде ИИ в отношении физической активности и ходьбы после лечения [21].
В многоцентровом рандомизированном плацебо-контролируемом исследовании, включавшем 339 пациентов в подострой стадии ишемического инсульта, соответствующих критериям сосудистой деменции в возрасте от 50 до 85 лет, сравнивалась эффективность применения нафтидрофурила (400 или 600 мг) в качестве дополнительной терапии в сравнении с плацебо. Пациенты получали антиагрегантную (аспирин и дипиридамол) терапию, физическую реабилитацию. При необходимости допускалась терапия малыми дозами бензодиазепинов и нейролептиков короткого действия. Согласно результатам исследования доля пациентов, у которых наблюдалось ухудшение, уменьшилась с 42 до 25% в группе получавших плацебо и до 27% — в группах получавших нафтидрофурил в дозировке 400 и 600 мг соответственно. Между группами, получавшими лекарственный препарат в разных дозах, существенной разницы в динамике регрессии когнитивных нарушений выявлено не было. Во время исследования неблагоприятные события, происшедшие после рандомизации, были зарегистрированы всего у 13% пациентов. Ни один из зарегистрированных симптомов, по мнению исследователей, нельзя рассматривать как возможно или вероятно связанный с изучаемым лекарственным препаратом. Ни у кого из участников в ходе исследования не было отмечено никаких клинически значимых изменений лабораторных и гематологических показателей [19]. Таким образом, препарат Дузофарм (нафтидрофурил) может эффективно использоваться у пациентов, перенесших ИИ, с целью восстановления утраченных функций головного мозга, уменьшения выраженности когнитивных нарушений.
Заключение
Ведение больного в раннем восстановительном периоде ИИ должно быть комплексным, т. е. включать нелекарственные и лекарственные методы. Пациенту и его родственникам должна быть разъяснена цель различных методов терапии и важность выполнения всех мероприятий в восстановительном и последующих периодах болезни. С учетом индивидуальных особенностей каждого конкретного пациента назначаются антигипертензивные и антитромботические средства, при необходимости статины, антидепрессанты, гипогликемические, глутаматергические, холинергические препараты. Сочетание нескольких средств вторичной профилактики ИИ (диета, физические упражнения, прием антитромбоцитарного или антикоагулянтного средства, статина и антигипертензивных препаратов) позволяет снизить риск развития повторного инсульта почти на 80%, предупредив тем самым 4 из 5 возможных инсультов. Двигательная реабилитация не только направлена на компенсацию очагового дефекта, но и способствует улучшению когнитивных функций и качества жизни пациентов. При назначении препаратов целесообразно отдавать предпочтение лекарственным средствам с доказанной безопасностью и эффективностью, длительное курсовое лечение которыми может способствовать более полному восстановлению функций центральной нервной системы после перенесенного инсульта.
Литература
1. Захаров В.В. Лечение ишемического инсульта. Русский медицинский журнал, 2006, 14, 4: 242-246. 2. Файзулин Е.Р. Реабилитация больных церебральным ишемическим инсультом в позднем восстановительном периоде на амбулаторно-поликлиническом этапе: дис. … канд. мед. наук. Иркутск, 2009. 172. 3. Гусев Е.И., Скворцова В.И., Стаховская Л.В. Эпидемиология инсульта в России. Журн. неврологии и психиатрии им. С.С. Корсакова. Инсульт: прил. к журн., 2003, 8: 4-9. 4. Парфенов В.А. Постинсультная депрессия: распространенность, патогенез, диагностика и лечение. Неврология, нейропсихиатрия, психосоматика, 2012, 4: 84-88. 5. Парфенов В.А., Хасанова Д.Р. Ишемический инсульт. М.: МИА, 2012: 288. 6. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге. Болезни нервной системы. Руководство для врачей. Под ред. Н.Н. Яхно. М.: Медицина, 2005, 1: 232–303. 7. European Stroke Orgasation (ESO) Executive Commitee; ESO Writing Committee. Guidelines for Management of ischaemic stroke and transient ischaemic attack. Cerebrovasc Dis, 2008: 457-507. 8. Парфенов В.А., Вербицкая С.В. Ведение больного, перенесшего инсульт. Неврология, нейропсихиатрия, психосоматика, 2013 (спецвыпуск 2): 23–27. 9. Яхно Н.Н., Захаров В.В., Локшина А.Б., Коберская Н.Н., Мхитарян Э.А. Деменции. М.: МЕДпресс-информ, 2010. 10. Житкова Ю.В., Сайхунов М.В., Хасанова Д.Р. Профилактика нарушений мозгового кровообращения. Consilium medicum, 2011, 9, 13: 5-8. 11. Захаров В.В. Хроническая сосудистая мозговая недостаточность. Трудный пациент, 2005, 12: 12-15. 12. Парфенов В.А. Профилактика повторного ишемического инсульта. Русский медицинский журнал, 2008, 16, 1: 1694-1699. 13. Dufouil С, Chalmers J, Coskun O. Effects of blood pressure lowering on cerebral white matter hyperintensities in patients with stroke: the PROGRESS (Perindopril Protection Against Recurrent Stroke Study) Magnetic Resonance Imaging Substudy. Circulation, 2005, 112 (1l): 1644–1650. 14. Rashid P et al. Blood pressure reduction and secondary prevention of stroke and other vascular events. Stroke, 2003, 34: 2741-2748. 15. Вахнина Н.В. Когнитивные нарушения и их лечение у больных с артериальной гипертензией. Медицинский совет, 2014, 5: 30-36. 16. PATS Collaborating Group. Post-stroke antihypertensive treatment study. A preliminary result. Chin Med J (Engl). 1995. 108(9): 710-717. 17. Oudart N. Naftidrofuryl Inhibits Contractions to Serotonin in Intact and De-endothelialized Cerebral Arteries in vitro. Journal of cardiovascular pharmacology. 1990. 16 (3): 45-48. 18. Boeijingaa PH, Nedeleca JF, Demazièresa A, Souana ML, Gamandb S, Gillesa C, Parotc P, Stanera L, Luthringera R, Machera JP. Characterization of the CNS Effects of Naftidrofuryl (Praxilène) by Quantitative EEG and Functional MRI: A Study in Healthy Elderly Subjects. Neuropsychobiology, 2003. 48. 160–168. 19. Muller HJ, Hartmann A, Kessler C,·Rainer M,·Brown T, Gamand S, Lehert P. Naftidrofuryl in the treatment of vascular dementia. European Archives of Psychiatry and Clinical Neuroscience. 2001. 251. 247–254. 20. Shteiner TJ. Naftidrofuril after acute stroke: a review and hypothesis. Journal of cardiovascular pharmacology. 1990. 16. 3: 58-61. 21. Capon A, Lehert P, Opsomer R. Natfidrofuryl in the treatment of subacute stroke. Journal of cardiovascular pharmacology. 1990. 16. 3: 62-66. 22. Welch KMA, Hashi K, Meyer JS. Cerebrovascular response to intracarotid injection of serotonin before and after middle cerebral artery occlusion. J Neurol Neurosurg Psych 1973, 36: 724-35. 23. Wiernsperger NF. Serotonin 5-HT2 Receptors and Brain Circulation. Journal of Cardiovascular Pharmacology™. New York: Raven Press, Ltd., 1990, 16 (3): 20-24. 24. Salzman SK, Hirofuji E, Llados-Eckman C, McEwen GD, Beckman AL. Monoaminergic responses to spinal trauma. J Neurosurg, 1987, 66: 431-9. 25. Ricci A. Amenta F. Autoradiographic localization of 5-HT2 receptors in rat cerebral vessels. Annual Meeting of the European Neuroscience Association. Zurich, 1988: 48.
Источник:
Медицинский совет, № 18, 2014
Программы:
Оценка реабилитационного потенциала
Реабилитация после инсульта
Восстановление когнитивных функций
Диагностика нарушений глотания и коррекция
Восстановление, коррекция нарушений речи