20.07.2018
Автор статьи — Дахно Л.А.кандидат медицинских наук, врач стоматолог-хирург, врач рентгенолог.
Посттравматическая невропатия системы тройничного нерва – это сенсорные нарушения с или без невропатической боли, часто приводящие к функциональным и психологическим последствиям.
Тройничный нерв — самый большой сенсорный нерв в организме и именно он ответственный за орофациальную область. Ятрогенные травмы тройничного нерва (trigeminalnerveinjuries -TNI) приводят к боли у 70% пациентов, что в свою очередь приводит к функциональным нарушениям речи, питания, поцелуев, бритья, нанесения макияжа, чистки зубов и т.д., а значит существует негативное влияние на самооценку, качество жизни и психологию пациента.
Нужно понимать, что после повреждения тройничного нерва полное выздоровление происходит редко, за исключением случаев незначительной травмы, поэтому очень важно сохранить доверительные отношения между стоматологом и пациентом и не давать ложных заверений о полном выздоровлении.
Повреждение нерва может возникать во время проведения любых стоматологических манипуляций: инъекций местной анестезии, удаления зуба мудрости, эндодонтического лечения, а также на всех этапах имплантации — от введения анестетика и подготовки ложа имплантата до внедрения имплантата, аугментации кости и/или отека мягких тканей после операции.
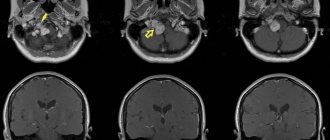
Рис. 1 Клинический случай. На изображениях компьютерной томографии КЛКТ визуализируются фрагменты силера, которые непосредственно прилежат к просвету нижнечелюстного канала в области ментального отверстия. Жалобы пациента на парестезию и болезненные ощущения от прикосновений и ветра в области подбородка и нижней губы слева, которые появились после эндодонтического лечения 34 зуба. Через 6 месяцев — парез (двигательное нарушение) левой половины нижней губы, что привело к невозможности полноценного питья и еды (пациентка удерживает губу пальцами во время приёма пищи во избежание выпадения пищи и жидкости изо рта) и, как следствие, стрессовое расстройство сопровождающееся беспокойством, страхом и приступами гнева.
Рис 2. Выведение силера в нижнечелюстной канал в результате отсутствия апикального упора
Что касается имплантации — боль во время препарирования кости пилотным сверлом может быть показателем близости нерва и, если это не учесть немедленно (принять решение о внедрении более короткого имплантата), можно получить постоянное повреждение нерва.
Повреждение нерва во время имплантации связано прежде всего с предоперационными факторами, включая плохое предоперационное планирование, что приводит к неточным измерениям и неверному выбору места имплантации и типа имплантата (диаметр и длина).
Рис 3а. Ошибка планирования.
Рис 3б. Неверный выбор длины имплантатов.
Рис 3-а,б. Изображения КЛКТ двух клинических случаев демонстрируют повреждение нерва связанное с имплантацией. Имплантаты внедрены непосредственно в канал нижнего альвеолярного нерва, что связано с ошибками предоперационного планирования.
Привычка тщательно планировать имплантацию на основе данных компьютерной томографии, проводить имплантацию под инфильтрационной анестезией с помощью хирургических шаблонов, делать интраоперационный рентгенконтроль и использовать стоперы сверла (ограничители сверления) может свести к минимуму возможную травму нерва во время имплантации.
Любые повреждения (проникновение или компрессия), а также кровоизлияния в нижнечелюстной канал приводят к острой и часто тяжелой интраоперационной боли невралгического типа и крайне важно, чтобы врач использовал соответствующий протокол инфильтрационной местной анестезии для того, чтобы пациент мог указать на близость хирургических инструментов к нижнечелюстному каналу.
Поскольку имплантация – это хирургия выбора, травму нерва, которая приводит к потенциально необратимым последствиям даже после повторного хирургического вмешательства (извлечение имплантата) можно всегда избежать.
Физиологические последствия повреждения сенсорного нерва являются немедленными и часто необратимыми. Нижний альвеолярный нерв проходит в костном канале, который может подвергнуться компрессии и повреждению ишемического типа. Сжатие периферических сенсорных нервов в течение 6 часов может вызвать атрофию нервных волокон.
Ишемия сама по себе даже без прямого повреждения нерва вызовет достаточное воспаление и повреждение нерва, которое может привести к постоянному поражению нерва.
Рис 4. Сагиттальные срезы КЛКТ демонстрируют допустимое соотношение имплантанта с просветом канала нижнего альвеолярного нерва, однако клиническая картина соответствует ишемии, которая вызвала боль и парестезию. В течении первых суток принято клиническое решение об удалении имплантата и назначении медикаментозного лечения.
Через три месяца после травмы нижнего альвеолярного нерва произойдут уже постоянные изменения нервной системы как центральные так и периферические, которые вряд ли будут поддаваться хирургическому лечению или реагировать на медикаментозное лечение и периферические вмешательства.
Когда возникает повреждение нерва, клиницист должен уметь распознавать тип и степень травмы, обеспечить наиболее подходящую послеоперационную помощь и уметь дать рекомендации.
Виды повреждений нервов:
— полная или частичная резекция нерва (перерезание),
— компрессия, разможжение, растяжение, ущемление, тепловые и ишемические повреждения.
Суммарный сенсорный дефицит может варьироваться от незначительной потери чувствительности до постоянной, тяжелой и изнурительной болевой дисфункции, но чаще всего сочетается анестезия, парестезия (безболезненное измененное ощущение), дизестезия (неудобное измененное ощущение) и невропатическая боль.
В настоящее время не существует у стоматолога стандартизированного протокола для диагностики и лечения повреждений нервов после имплантации.
Мы попробуем заполнить этот пробел.
Посттравматическое повреждение сенсорного нерва. Терминология.
Ассоциация по изучению боли стандартизировала номенклатурную систему, которая определяет наиболее часто используемые невросенсорные описательные термины Classification of Chronic Pain, Second Edition: International Association for the Study of Pain Task Force on Taxonomy, ed.: H Merskey and N. Bogduk. IASP Press IASP Council in Kyoto, November 29-30-2007.
- Парестезия — не болезненное измененное ощущение. Может описываться пациентами как мурашки, легкое ощущение жжения или покалывания. НОВЫЕ ощущения — растягивание, тянущие ощущения.
- Дизестезия — извращенные ощущения. Аномальные, иногда неприятные ощущения, испытываемые человеком с частичным повреждением чувствительных нервных волокон во время прикосновения к коже. — Неприятное ненормальное ощущение, спонтанное или спровоцированное. Примечание: дизестезия — это не боль, когда больно и не парестезия. Особые случаи дизестезии — гипералгезия и аллодиния. Дизестезия всегда должна быть неприятной, а парестезия не должна быть неприятной, хотя признается, что граница может создавать определенные трудности, когда речь идет о том, приятные или неприятные эти ощущения. Всегда следует указать, являются ли ощущения спонтанными или спровоцированными.
- Невропатическая боль (IASP) — боль, вызванная поражением или заболеванием соматосенсорной нервной системы.
- Невропатия (IASP) — нарушение функции или патологическое изменение в нерве: в одном нерве — мононейропатия; в нескольких нервах — мононейропатический мультиплекс; если диффузная и двусторонняя — полинейропатия. Примечание: Неврит является особым случаем нейропатии и в настоящее время термин предназначен для воспалительных процессов, влияющих на нервы. — чувствительный (прикосновение, тепло, боль) — двигательный (движение).
- Аллодиния — боль от непагубных стимулов (боль при лёгком прикосновении / на холоде / в жару). Появление боли в ответ на стимул, который у здоровых людей ее не вызывает. Термическая аллодиния, особенно холодовая аллодиния — особенность экстраорального дерматома у пациентов с IANIs. Некоторые пациенты сообщают о сниженной вкусовой и тепловой чувствительности. Извращение чувствительности характеризуется повышенным порогом чувствительности и увеличенной длительностью восприятия, отсутствием точной локализации ощущений имеющих неприятный характер, склонностью к иррадиации. Боль продолжается при удалении стимула.
- Гипералгезия — повышенная чувствительность к болевым раздражителям
- Анестезия — онемение
- Гиперестезия и Гипостезия — это термины, которые часто используются для описания изменений чувствительности в большую или меньшую сторону соответственно.
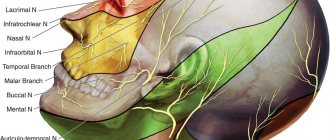
Рис. 5 Анатомия II (верхнечелюстной) и III (нижнечелюстной) веток тройничного нерва. Важно заметить, что ветви верхнего альвеолярного нерва ретроградно «вливаются» в подглазничный нерв, что объясняет симптоматику отека и боли подглазничной области при повреждении верхнего зубного сплетения.
Посттравматическая сенсорная невропатия – это боль, развивающаяся после медицинского вмешательства (операция, лечение, анестезия), минимальной продолжительностью 2 месяца при этом исключены другие причины боли (инфекция, стойкая малигнизация, неправильное диагностирование и др.), также должна быть исключена предоперационная боль от других причин.
Важно добавить, что невропатическая область не обязательно должна четко указываться пациентом, однако около 80% пациентов могут локализовать и указать на невропатический участок.
ЗДЕСЬ можно больше прочитать о частоте «фантомной зубной боли» (атипичная одонтальгия) после эндодонтического лечения, которая классифицируется как стойкая дентоальвеолярная боль (persistent dentoalveolar pain PDAP тип 2) и встречается до 3% случаев.
Факторы, влияющие на неврологический ответ при травме нерва
— Необходимо проводить предоперационный скрининг невропатической боли. Предшествующая невропатическая зубная боль (PDAP тип 1), которая существует до операции, может быть вызвана множеством различных системных состояний, принимаемыми медикаментами и другими поражениями. Крайне важно, чтобы хирурги признавали предхиругические невропатические состояния, поскольку невропатическая боль не реагирует на хирургическое вмешательство, а часто может привести и к ухудшению боли. Кроме того, плохо контролируемая предоперационная боль и повреждение нерва могут вызвать хроническую послеоперационную боль.
— Основными показателями прогнозирования хронической постхирургической боли являются психологические факторы, в том числе уровень беспокойства, невротизм (фундаментальная черта личности в психологии, характеризуется тревожностью, страхом, быстрой сменой настроения, фрустрацией и чувством одиночества. Считается, что невротические люди хуже справляются со стрессом, склонны преувеличивать отрицательную сторону той или иной ситуаций.), катастрофизация и интроверсия. Таким образом, у врача есть возможность не проводить хирургию выбора (имплантацию) у таких пациентов, а принять решение в пользу альтернативого плана лечения.
— Концентрация используемого анестетика — до 2% лидокаин — принятый стандарт, т.к. более высокая концентрация обладает бо́льшым нейротоксичным эффектом, что может стать причиной постоянной нейропатии. Избегайте использования нескольких (повторных) анестезирующих блокад в одной области по той же причине.
— Предоперационный медицинский осмотр должен исключить следующие заболевания: Болезнь Рейно, Эритромелалгию (болезнь Митчелла), Синдром раздраженного кишечника (IBS), Мигрени, Фибромиалгию.
— Локализация хирургии — это еще один фактор, связанный с неврологическим ответом. Травма в дистальном отделе челюсти более значительна (например, область угла и ветви челюсти) чем в области ментального отверстия, т. к. чем ближе проксимальный участок повреждения нерва, тем выше риск повреждения клеток ганглия тройничного нерва и инициирование ретроградных эффектов дифференцировки в центральную нервную систему.
Таким образом, тщательное собеседование и обследование пациента, детальное предварительное планирование имплантации на основе данных КЛКТ, соответствующая визуализация плана имплантации и использование хирургических шаблонов, выбор оптимальных размеров имплантатов с расширенными зонами безопасности, использование ограничителей свёрления и, конечно, опытная команда врачей, которые проведут имплантацию с последующим ранним послеоперационным наблюдением — все эти факторы будут способствовать более безопасной практике и оптимизации результатов для пациента.
Причины
Обычно при неврите тройничного нерва происходит его сдавливание, что провоцирует демиелинизацию, то есть нарушение проводимости сигналов.
Причинами заболевания могут стать:
- Рассеянный склероз, при котором нерв подвергается компрессии, вызванной холестериновыми бляшками или опухолью.
- Травматическое повреждение самого нерва.
- Патологии развития челюсти.
- Инфекционные заболевания.
А также воспалительные процессы, затрагивающие область расположения ветвей нерва.
Различают два вида тригеминальной невралгии – первичную и симптоматичную, которая формируется на фоне иных заболеваний, например, инфекций, опухолей, склеротических изменений.
Неврит тройничного нерва протекает типично и в атипичной форме. Во втором случае боль присутствует постоянно и затрагивает значительную область лица, что не характерно для клинической картины.
Можно выделить несколько основных причин возникновения воспаления:
- Переохлаждение. Достаточно попасть под сквозняк или подольше находиться на холодном воздухе, как тройничный нерв отреагирует сильной болью и другими характерными симптомами.
- Стресс. Сильные эмоциональные переживания, потрясения или длительное психологическое перенапряжение могут вызвать тригеминальную невралгию.
- Ишемия – недостаточное кровоснабжение.
А также иные провоцирующие факторы.
Особенности проявлений ятрогенного повреждения тройничного нерва
- Болевой дискомфорт, изменение ощущений, онемение (анестезия).
- Функциональные последствия — пациенты, испытывающие боль от прикосновения или холода, часто испытывают трудности с ежедневными функциями: поцелуи, общение, речь, еда и питье и т. д. https://www.ncbi.nlm.nih.gov/pubmed/22677874
- Психологические последствия — у пациентов развиваются различные беспокойства, страх, гнев, посттравматическое стрессовое расстройство. Психологические расстройства могут усугубляться в тех случаях, если до медицинского вмешательстване не было подписано информированное осознанное согласие на имплантацию, эндодонтическое лечение, ортогнатическую хирургию и т. д., где конкретно указано о возможном повреждении нерва.
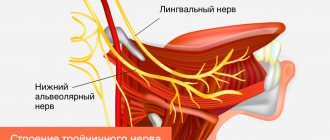
Рис. 6. Схематическое изображение соотношения веток нижнего альвеолярного нерва с формируемым ложе имплантата. Боль во время сверления — важный диагностический критерий близости нерва.
Клинический алгоритм определения посттравматической нейропатии
Анкета оценки нейропатии тройничного нерва
Важно! Сильная боль, испытываемая во время лечебных манипуляций — может быть подтверждением вероятной травмы нерва.
- История первичного возникновения боли.
- Развитие боли.
- Продолжительность боли.
- История регулярной боли SOCRATES (Site, Onset, Character, Radiation, Associated signs, Timing, Exacerbating and relieving factors, Severity) — Локализация, Возникновение (частота возникновения приступов), Характер, Иррадиация, Связанные симптомы, Продолжительность, Факторы обострения и облегчения (что усиливает и купирует боль), Тяжесть боли.
- Психологический скрининг.
- Функциональный скрининг (влияние на повседневную жизнь).
Механосенсорные тесты (картирование области поражения)
Протокол обследования дерматомы с целью оценки экстра-оральной механосенсорной функции альвеолярной ветки тройничного нерва.
Дерматомы — сегменты кожи, на которые подразделяется вся поверхность человеческого тела в связи с иннервацией ее различными корешками спинного мозга, в данном случае — тройничного нерва.
Рис 7. Дерматомы веток тройничного нерва
1. Протоколирование области поражения.
Используя хирургический пинцет, пройти от нормальной к невропатической (измененной) области, предупреждая пациента, что может быть повышенная чувствительность и/или пониженная чувствительность. Выделите область на лице пациента маркерными метками и сделайте фотографию. Оцените % или область экстра-оральный дерматомы, на который влияет нейропатия.
2. Протоколирование оценки субъективного ощущения.
Плотно (но не больно) прижмите хирургический пинцет или зонд к руке пациента несколько раз с интервалами (5 раз в минуту) объясняя, что это «нормальная» субъективная оценка функций по шкале 10 из 10. Нажмите с тем же давлением на не пораженную сторону лица или языка и повторите стимуляцию, объясняя, что это должно быть 10 из 10. Затем уберите пинцет или зонд и объясните, что отсутствующая стимуляция равна 0 из 10. Только после этого повторите такие же действия в области нейропатии, которую вы уже подтвердили и отметили маркерными метками, и попросите пациента сообщить уровень раздражителя из возможных 10 (если > 10 = гиперестезия и <10 = гипостезия). Этот тест нужно повторить в разных областях нейропатии (кайма губ, кожа губ, подбородок, язык и т. д.)
3. Протоколирование оценки легкого прикосновения
Для оценки порогов легкого прикосновения рекомендуется использовать разлохмаченный ватный тампон, повторяя прикосновения с интервалом 5 раз в мин. Сначала с здоровой стороны, а затем повторяя на пораженной стороне попросите пациента сообщить о различиях. Если пациент испытывает онемение, то при стимуляции будет снижен порог обнаружения легкого касания, однако, если пациент страдает от гиперестезии и возможной аллодинии (боль при прикосновении), то этот тест может быть очень не комфортным и раздражающим.
Интерпретация карты вовлечения дерматомы и оценка нейропатии— Соответствует ли область нейропатии области дерматомы, в котором была проведена операция? — Динамика площади вовлеченной внеротовой и внутриротовой области при картировании невропатических участков (надежность критерия низкая)
Важно! Локальная сенсорная нейропатия не всегда присутствует у пациентов, однако почти всегда есть область аномального ощущения, а максимальная боль у пациента связана с областью сенсорного дефицита, то есть страдает от сочетания боли, онемения и измененного ощущения. Это важное диагностическое отличие сенсорной нейропатии.
Субъективная функция
- Нейропатия является гиперестезией или гипостезией?
- Тест на термическую аллодинию — возникновение боли при воздействии тепла или холода. Термическая аллодиния, особенно холодовая аллодиния — особенность для пациентов с повреждением тройничного нерва.
- Тест на термическую гипералгезию. Повышенная боль, возникающая на слабое воздействие раздражителя.
- Тест «Направление движения». Пациент закрывает глаза, доктор при помощи мягкой кисточки определяет способность пациента обнаруживать как ощущение, так и направление движения кисточки.
- Тест на чувствительность к температурным раздражителям. ватный тампон со спрей для холодового теста и нагретая ручка стоматологического зеркала до 43 — 45 ° C — используются для определения способности пациента чувствовать холод и тепло. Альтернативно, можно заполнить пробирки горячей (43 -45 ° C) водой и холодной водой.
Существуют рекомендации ВОЗ относительно того, какие параметры периферических сенсорных последствий нужно учитывать для прогноза результатов микрохирургического восстановления поврежденного сенсорного нерва. Zuniga JR и Yates DM адаптировали рекомендации к поражениям тройничного нерва. Подробнее здесь: Zuniga JR и Yates DM Factors Determining Outcome After Trigeminal Nerve Surgery for Neuropathic Pain. J Oral Maxillofac Surg 2021 Jul;74(7):1323-9.
Сегодня уже принят гайдлайн обязательного рентгенконтроля после эндодонтического лечения и операции дентальной имплантации с целью индикации соотношения корня и корневой пломбы, а также близости ложе имплантата и/или самого имплантата к каналу нижнеальвеолярного нерва. Считается, что достаточно интраоральной дентальной рентгенографии для выявления ятрогении, хотя посттравматическая нейропатия является прежде всего клиническим диагнозом.
Renton T, Yilmaz Z. Managing iatrogenic trigeminal nerve injury: a case series and review of the literature. Int J Oral Maxillofac Surg 2012 May;41(5):629-637.
Ятрогенная нейропатия тройничного нерва.
Эта нозологическая единица возникла в связи с тем, что лечение невралгии тройничного нерва в большинстве случаев начинали с проведения нейродеструктивных операций (спиртово-лидокаиновые блокады, нейроэкзерез, деструкция узла тройничного нерва). Вследствие этого у значительного числа больных наблюдались ятрогенные травматические или токсико-травматические нейропатии тройничного нерва. Чаще всего поражались верхне- и нижнечелюстной нервы.
Во многих пособиях по неврологии предлагается в случае невралгии тройничного нерва проводить спиртово-новокаиновые и спиртово-лидокаиновые блокады периферических его ветвей или узла — так называемая алкоголизация. Обезболивающий эффект в этом случае достигается в среднем после второй-третьей процедуры, но объясняется он тем, что наступает онемение вследствие развития деструктивных изменений в стволе нерва. С течением времени развивается токсико-травматическая нейропатия, практически резистентная к лечению, поэтому больному необходимо проводить и дальше блокады, эффективность которых уменьшается пропорционально к их количеству.
Таким образом, нейродеструктивные операции, которые проводятся при лечении невралгии, приводят к развитию токсико-травматической нейропатии. Этим и обусловлен характер болевого синдрома.
Клиника.
Клиническая картина представлена, как правило, наличием постоянной ноющей, жгучей или тупой нейропатической боли в участке иннервации пораженного нерва, на фоне которой возникают невралгические пароксизмы с иррадиацией боли соответственно в сегментарные зоны лица (сегменты Зельдера). У больных наблюдаются разнообразные виды парестезии (онемение, «ползание мурашек», жжение) и расстройства чувствительности (гипестезия с явлениями гиперпатии или гиперестезии), которые иногда распространяются за пределы иннервации одной из ветвей тройничного нерва.
Во многих случаях в процесс втягиваются вегетативные волокна, что приводит к трофическим изменениям слизистой оболочки полости рта (гингивит), зубочелюстной системы (прогрессирующий пародонтит) и кожи лица (пигментация или депигментация, сухость, шелушение, атрофия мягких тканей). В таких случаях боль становится невыносимо жгучей, разрывной, сверлящей, сопровождается вегетативными реакциями (покраснением и отеком кожи лица, местным повышением температуры тела, слезоте чением, слюнотечением).
Во время проведения нейродеструктивных манипуляций на нижнечелюстном нерве может возникать болевое сведение зубов (больные вынуждены принимать пищу через соломинку, не могут разговаривать и открывать рот). С каждой последующей алкоголизацией характер болевого синдрома изменяется: невралгические пароксизмы становятся более длительными, частыми, может формироваться невралгический статус, на коже лица возникают незначительно выраженные триггерные участки. Боль провоцируют погодные условия (холод или жара), обострение соматической патологии, употребление пищи, физические нагрузки. Точки выхода тройничного не рва болезненны во время пальпации приблизительно у 2/3 больных.
Приведенные данные убедительно свидетельствуют о том, что про ведение нейродеструктивных манипуляций не является методом выбора лечения невралгии тройничного нерва, поскольку в большинстве случаев достигается непродолжительный эффект. Вместе с тем такая терапия приводит к развитию токсической нейропатии, прогрессированию заболевания и развитию резистентности к консервативным методам лечения. Лишь в том случае, когда все использованные методы лечения невралгии являются не эффективными, а интенсивность болевого синдрома остается выраженной, можно использовать нейродеструктивные операции, разработанные в последнее время нейрохирургами.
Что происходит после повреждения нерва?
Взаимодействие между периферическими сенсорными нервами и центральной нервной системой необычайно сложное. Доказано, что незначительная травма такая как компрессия, сотрясение, контузия (ушиб) или «защип» может привести только к онемению, однако более серьезная травма (химический ожог, анатомический перерыв частичный или полный) может привести к дизестезии и/или невропатической боли, что вызывает постоянный дискомфорт у пациентов (особенно ночью) и влияет на качество их жизни.
- После повреждения волокон нижнего альвеолярного нерва в течение всего нескольких минут развивается дегенерация со всего места повреждения: ретроградная по направлению к ЦНС и валлерианова по направлению к периферии.
- При острой компрессии немедленно нарушается аксоплазматический ток, что приведёт к снижению мембранной возбудимости. Если компрессию не убрать = хроническая компрессия, стартует развитие аксолизиса и валлериановой дегенерации, что в свою очередь приведет к развитию фиброза, образованию невромы и прогрессированию невропатии.
- Даже если нервные волокна частично прерваны, сохраняется возможность спонтанной регенерации нерва за счет врастания аксонов концевых отделов его центрального отрезка в периферический участок при условии немедленного удаления имплантата. Между прерванными нервными волокнами сохраняется линейный массив шванновских клеток, которые значительно увеличивают фактор роста нервов. Кроме того, значительно активизируется работа гена, кодирующего рецепторную мРНК и активируется регенерация нерва. Эти защитные механизмы и реакции репарации могут быть завершены в течение 2 — 3 недель. Таким образом, нерв вновь может подключаться достаточно быстро, за исключением случаев тяжелой нейропатии или полного разрыва.
Несмотря на то, что гистологически будет наблюдаться регенеративная репарация и подключение нерва, тем не менее функция полностью не восстанавливается. Повторное подключение (соединение) нерва не означает заживление, а при определенных условиях может стать причиной боли у пациентов.
Нижний альвеолярный нерв является смешанным и отвечает за болевую чувствительность, чувствительность к прикосновению, теплу, холоду и давлению, хотя механизм каждого вида чувствительности отличается. Можно провести аналогию с подземной сетью труб в большом городе, где транспортируются газ, электричество, телефон, вода и канализация, но каждая труба по отдельности и по своему маршруту. Если нервные сети повреждены, изолированность структуры скомпрометирована, и когда происходит регенерация, соседние нервные волокна могут быть случайно подключены друг к другу. Это значит, что импульсы от периферических нервов могут передаваться в неправильное место назначения, а оттуда — к ЦНС. Если принять аналогию с трубопроводом, то это как если бы подземные воды и электрические кабеля, разорванные в результате землетрясения, были бы перекрестно связаны.
Рис. 8. Нижний альвеолярный нерв. Смешанная чувствительность. Каждое волокно отвечает за свой вид чувствительности.
Такая ненадлежащая связь называется «эфапсией» и была доказана на лабораторных животных ещё в 70-е годы прошлого столетия. https://www.ncbi.nlm.nih.gov/pubmed/224343
Таким образом, после травмы функция нерва никогда полностью не восстанавливается, даже если регенерация нерва гистологический завершается путем активной его репарации.
Рассмотрим случай, когда нервные волокна, предназначенные для передачи чувства холода случайно связываются с тепловыми, что может поставить под угрозу способность пациента реагировать на изменения температуры. Существует бесчисленное количество нервных волокон, поэтому травма любого конкретного нерва может привести к соединению с любым количеством других нервов в зависимости от тяжести травмы. Большое количество неправильных подключений нервных волокон и приводит к образованию невромы.
Невромы часто генерируют спонтанный разряд. Этот электрический импульс и вызывает дизестезию, а такие пациенты жалуются, как правило, на онемение, покалывания или мурашки на коже. https://www.joms.org/article/0278-2391(90)90385-F/pdf
Таким образом заживление поврежденного нерва невероятно сложный процесс, который не ограничивается только участком травмы, а вовлекается в процесс вся система от периферии к ЦНС, в отличие от процессов заживления слизистой или кости. Регрессивные изменения в аксонах и миелиновой оболочке, а также регенерация нерва влияет на все нейроны не только гистологически, но и молекулярно и электрофизиологически. Формирующийся эфапс
создаёт участок соприкосновения, в котором возбуждение с одной клетки на другую передается посредством электрического тока без участия медиаторов.
Рис. 9. Перекрестное возбуждение соседних волокон холодной и горячей чувствительности за счет эфаптической передачи электрического импульса. Возможно взаимодействие волокон разного диаметра (например волокон холодовой и болевой чувствительности), при этом сигнал распространяется в обоих направлениях, что лежит в основе стимулозависимых симптомов боли и объясняет ненормальное восприятие непагубной стимуляции при аллодинии и гиперпатии.
Невралгия тройничного нерва
Тригеминальная невралгия (ТН) — (синонимы: tic douloureux, или болезнь Фотергилла) является одной из самых распространенных лицевых болей (прозопалгий — (греч. prosopon (лицо) + algos (боль)) и относится к числу наиболее устойчивых болевых синдромов в клинической неврологии. ТН является типичным примером нейропатической боли и считается самым мучительным видом прозопалгии. ТН чаще всего имеет хроническое или рецидивирующее течение, гораздо труднее поддается лечению, чем многие другие типы хронической боли. Высокая интенсивность и стойкость тригеминальной невралгии, ее особый, часто мучительный характер, резистентность к традиционным методам обезболивания придают этой проблеме исключительную актуальность. По данным ВОЗ распространенность ТН составляет до 30–50 больных на 100 000 населения, а заболеваемость — 2–4 человека на 100 000 населения. ТН чаще встречается у женщин, чем у мужчин, дебютирует на пятом десятилетии жизни и в 60% случаев имеет правостороннюю локализацию. Причины ТН Наиболее частой причиной возникновения ТН является компрессия проксимальной части тригеминального корешка в пределах нескольких миллиметров от входа корешка в мост мозга (т. н. «входная зона корешка»). Примерно в 80% случаев происходит компрессия артериальным сосудом (чаще всего патологически извитой петлей верхней мозжечковой артерии). В остальных случаях таковая компрессия вызвана аневризмой базилярной артерии, объемными процессами в задней черепной ямке, опухолями мостомозжечкового угла и бляшками рассеянного склероза На экстракраниальном уровне основными факторами, приводящими к возникновению ТН, являются: туннельный синдром — компрессия в костном канале, по которому проходит нерв (чаще в подглазничном отверстии и нижней челюсти), связанная с его врожденной узостью, присоединением сосудистых заболеваний в пожилом возрасте, а также в результате хронического воспалительного процесса в смежных зонах (кариес, синуситы); местный одонтогенный или риногенный воспалительные процессы. Развитие ТН может провоцироваться инфекционными процессами, нейроэндокринными и аллергическими заболеваниями, демиелинизацией корешка тройничного нерва при рассеянном склерозе.
Клинические проявления ТН
Заболевание, в большинстве случаев, развивается на одной стороне, двусторонний процесс бывает крайне редко. Сначала болевые ощущения возникают в месте иннервации какой-либо из трех ветвей, в дальнейшем при прогрессировании болезни боль может постепенно охватывать участки лица, иннервируемые соседними ветвями. Локализация боли зависит от того какие ветви вовлечены в процесс:
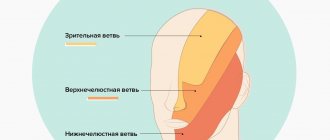
- при поражении первой ветви болевые ощущения локализуются в области надбровной дуги, лба, виска, иногда боль возникает в веках и глазном яблоке;
- при возникновении патологического процесса во второй ветви болевые ощущения возникают в верхней губе, крыле носа, в проекции скуловой кости, верхней части щеки, верхней челюсти и небе;
- при поражении третьей ветви болевая зона локализируется в нижней губе, подбородке, щеке, нижней челюсти, половине языка и мягкого неба.
Систематика тригеминальных прозопалгий
С точки зрения топической диагностики, развитие любой формы тригеминальной прозопалгии связано с поражением периферического тригеминального нейрона — периферических тригеминальных ветвей, сенсорного тригеминального ганглия (расположенного на основании черепа), следующего за ним в направлении ствола мозга сенсорного корешка тройничного нерва, а также входящих в ствол мозга сенсорных тригеминальных волокон и сенсорных ядер тройничного нерва. В зависимости от воздействия патологического процесса на соответствующий отдел тригеминальной системы выделяют ТН преимущественно центрального и периферического генеза. В возникновении ТН центрального генеза большую роль играют нейроэндокринные, иммунологические и сосудистые факторы, которые приводят к нарушению реактивности корково-подкорковых структур и формированию очага патологической активности в ЦНС. В патогенезе ТН периферического уровня большую роль играют компрессионный фактор, инфекции, травмы, аллергические реакции, одонтогенные процессы. Несмотря на различие симптоматологии клинических форм тригеминальных прозопалгий, основное значение для их дифференциации имеют особенности лицевой боли, в одних случаях — проявляющейся продолжительной (постоянной) болью, а в других — в виде пароксизмов боли. Пароксизмальные формы тригеминальной боли традиционно обозначаются невралгией, а непароксизмальные формы — невропатией тройничного нерва. Указанные формы лицевой боли — невралгия и невропатия тройничного нерва — принципиально различаются между собой по подходам к лечению. Деафферентационная тригеминальная невропатия (прозопалгия)
Деафферентационная лицевая боль (прозопалгия) — наиболее тяжелая форма тригеминального поражения, проявляющаяся высокоинтенсивной, нередко резистентной к консервативной терапии лицевой болью и выраженной сенсорной недостаточностью. Развивается в результате значительного повреждения (разрушения) периферических или центральных структур тригеминальной системы. Понятие «деафферентационные тригеминальные прозопалгии», в качестве обобщающего синдромологического определения, было предложено Ю. В. Грачевым и Ю. А. Григоряном (1995) для обозначения особой формы лицевых болей, развивающихся в результате деафферентации в сенсорной системе тройничного нерва. Патофизиологический термин «деафферентация» (де- + лат. afferentis приносящий), в буквальном смысле означает разобщение рецепторных зон периферических нервов с центральными сенсорными структурами, вследствие нарушения целостности или проводимости нервных волокон. Типичными периферическими формами деафферентационных тригеминальных прозопалгий являются постгерпетические, опухолевые и ятрогенно обусловленные лицевые боли (вызванные деструкцией ганглия и корешка тройничного нерва), а центральными — две достаточно редкие формы, обусловленные сирингобульбией и инфарктом продолговатого мозга.
Диагностика ТН
План клинического опроса при обследовании больных с лицевой болью. Описание болевых ощущений:
- Локализация боли
- Временная характеристика боли (приступообразная/неприступообразная, продолжительная)
- Частота болевых приступов
- Интенсивность боли
- Сенсорный характер боли
- Другие ощущения, сопровождающие лицевую боль (ассациированные признаки)
- Условия и время возникновения боли
- Лекарственные средства (другие факторы), уменьшающие или устраняющие боль
Анамнестические данные:
- Длительность заболевания
- Условия развития первого обострения
- Характер течения прозопалгии (острое, рецидивирующее, непрерывное)
- Частота обострений прозопалгии
- Предшествующее лечение
- Нарушения (неврологические, соматические), сопутствующие развитию заболевания.
При проведении пальпаторного исследования лицевой области необходимо различать «невралгический» и «миофасциальный триггер» (англ. trigger — курок). Невралгические триггерные точки или зоны (у больных с тригеминальной невралгией) представляют собой сверхвозбудимые участки кожи и слизистой оболочки, при механическом раздражении которых, включая легкое касание, возникает болевой приступ. В то же время сильное давление, обычно осуществляемое самим же больным, не только не вызывает боль, но в ряде случаев приводит к уменьшению или исчезновению боли. Миофасциальные триггерные точки (по сути — болевые точки) расположены в мягких тканях лица в проекции жевательных мышц. «Надавливание» на них сопровождается локализованной или иррадиирующей болезненностью.
Лечение ТН Основными направлениями медикаментозной терапии являются:
- устранение причины ТН, если она известна (лечение больных зубов, воспалительных процессов смежных зон и др.),
- проведение симптоматического лечения (купирование болевого синдрома).
- Препаратами выбора для лечения ТН являются антиконвульсанты, а карбамазепин стал одним из первых препаратов, официально зарегистрированных для лечения этого состояния.
В начале 90-х годов прошлого столетия появилась новая генерация противоэпилептических препаратов, и теперь антиконвульсанты обычно делят на препараты первого и второго поколения. Препараты первого поколения практически не рассматриваются в качестве первой линии терапии НБ (за исключением карбамазепина при ТН). К антиконвульсантам второго поколения относятся прегабалин (Лирика), габапентин (Нейронтин, Габагамма, Тебантин), ламотриджин (Ламиктал), окскарбазепин (Трилептал), топирамат (Топамакс), леветирацетам (Кеппра), тиагабин (Габитрил), зонисамид (Зонегран), вигабатрин (Сабрил), фелбамат (Талокса). Эти препараты имеют более благоприятные фармакокинетические характеристики и профили безопасности, а также низкий риск лекарственных взаимодействий по сравнению с антиконвульсантами первого поколения. Согласно рекомендациям Европейской федерации неврологических сообществ (2009) фармакотерапия ТН основана, прежде всего, на использовании предложенного С. Блюмом в 1962 году карбамазепина (Финлепсина, Тегретола) (200–1200 мг/сутки), который является препаратом первого выбора (уровень доказательности A). Противоболевое действие этого препарата обусловлено, главным образом, его способностью уменьшать проницаемость для натрия мембран нейронов, участвующих в ноцицептивных реакциях. Обычно назначается следующая схема лечения карбамазепином:в первые два дня суточная доза составляет 200 мг (по 1/2 таблетки утром и вечером), затем в течение двух дней суточная доза увеличивается до 400 мг (утром и вечером), а после этого — до 600 мг (по 1 таблетке утром, в обед и вечером). Габапентин (Нейронтин) — первый в мире препарат, который был зарегистрирован для лечения всех видов нейропатической боли. Во многих исследованиях была показана эффективность габапентина у больных с ТН, не отвечающих на лечение другими средствами (карбамазепин, фенитоин, вальпроаты, амитриптилин); при этом в большинстве случаев наблюдалось полное купирование болевого синдрома. Терапевтическая доза составляет от 1800 до 3600 мг/сутки. Препарат принимают 3 раза в сутки по следующей схеме: 1-я неделя — 900 мг/сутки, 2-я неделя — 1800 мг/сутки, 3-я неделя — 2400 мг/сутки, 4-я неделя — 3600 мг/сутки. Недавно были опубликованы результаты открытого проспективного 12-месячного исследования 53 пациентов с ТН, в котором оценивалась эффективность прегабалина (Лирики) в дозе 150–600 мг/сутки. Лечение прегабалином привело к обезболиванию или, по крайней мере, к 50%-му снижению интенсивности боли у 25% и 49% пациентов соответственно. Впервые об использовании леветирацетама (Кеппра) при лечении ТН сообщили в 2004 году K. R. Edwards et al. Свойства этого препарата особенно подходят для лечения пациентов с ТН с тяжелой болью, нуждающихся в быстром ответе на терапию. В отличие от других антиконвульсантов, особенно карбамазепина, в метаболизм леветирацетама не вовлечена система печеночного цитохрома Р450 и препарат экскретируется через почки. Кроме того, данный препарат характеризуется благоприятным терапевтическим индексом и имеет незначительное число неблагоприятных побочных эффектов (что является основной проблемой при использовании препаратов для лечения ТН). В 10-недельном проспективном открытом исследовании показано, что для лечения ТН по сравнению с терапией эпилепсии были необходимы более высокие дозы леветирацетама, составляющих 3000–5000 мг/день (50–60 мг/кг/день), которые, тем не менее, не вызвали значительных побочных эффектов. Это обстоятельство свидетельствует о перспективе использования этого лекарственного средства для лечения ТН. С 1970-х годов прошлого столетия для лечения ТН стали использовать антидепрессанты. В настоящее время доказана эффективность использования трициклических антидепрессантов (ТЦА) при лечении ТН. Патогенетическое лечение больных с ТН включает применение препаратов нейрометаболического, нейротрофического, антиоксидантного, антигипоксантного действия. В последние годы обнаружена высокая эффективность использования метаболических препаратов. При лечении пациентов с ТН показана высокая эффективность препарата метаболического действия Актовегина — депротеинизированного деривата из крови молодых телят. Основное действие этого препарата заключается в стабилизации энергетического потенциала клеток. Актовегин обладает также антигипоксическим эффектом, являясь непрямым антиоксидантом. Кроме того, действие Актовегина проявляется непрямым вазоактивным и реологическим эффектами за счет повышения капиллярного кровотока, снижения периферического сосудистого сопротивления и улучшения перфузии органов и тканей. В период приступа целесообразно применение Актовегина внутривенно медленно струйно или капельно в течение 10 дней в дозе 400–600 мг/сутки. В межприступном периоде препарат назначается внутрь в дозе 200 мг 3 раза в сутки на протяжении 1–3 месяцев. К патогенетическому лечению больных с ТН можно отнести применение высоких доз витаминов группы B в составе поликомпонентных препаратов, что обусловлено их полимодальным нейротропным действием (влиянием на обмен веществ, метаболизм медиаторов, передачу возбуждения в нервной системе), а также способностью существенно улучшать регенерацию нервов. Кроме того, витамины группы B обладают анальгезирующей активностью. К таким препаратам, в частности, относятся Мильгамма, Нейромультивит, Нейробион. До настоящего времени подбор анальгезирующей терапии НБ является скорее искусством, чем наукой, поскольку выбор препаратов осуществляется в основном эмпирически. Нередки ситуации, когда применение одного препарата оказывается недостаточно эффективным и возникает потребность в комбинации лекарственных средств. Назначение «рациональной полифармакотерапии» (одновременное применение препаратов, обладающих нейротропным, нейрометаболическим и анальгезирующим механизмами действия) позволяет повысить эффективность лечения при меньших дозировках препаратов и меньшем количестве побочных эффектов.
Дифференцированные лечебные подходы при пароксизмальных и непароксизмальных тригеминальных прозопалгиях.
Дифференцированные лечебные подходы при пароксизмальных и непароксизмальных тригеминальных прозопалгиях
| Пароксизмальная приступообразная лицевая боль Длительность болевых приступов: от нескольких секунд (мгновенная боль») до нескольких минут | Непароксизмальная (продолжительная) лицевая боль |
| Клинические формы Неврлалгия тройничного нерва — типичная тригеминальная невралгия — тригеминальная невралгия с невропатическими проявлениями (после проведения «лечебных блокад») — тригеминальная невралгия при рассеянном склерозе — симптоматическая тригеминальная невралгия при опухолях основания черепа и мозга | Клинические формы Невропатия тройничного нерва — одонтогенная — травматическая — герпетическая(включая постгерпетическую невралгию) — аутоиммунная (при системных ревматических заболеваниях) Деафферентационная тригеминальная прозопалгия (высокоинтенсиная постоянная боль) — ятрогенная («деструкционная») — постгерпетическая — опухолевая |
| Основные лечебные подходы — карбамазепин – базисный препарат, способствующий подавлению болевых приступов — Мильгамма, Мильгамма-композитум Физиотерапия, рефлексотерапия — При неэффективности конскервативного лечения типичной тригеминальной невралгии – нейрохирургическая декомпрессия корешка тройничного нерва | Основные лечебные подходы — НПВП (диклофенак, ибупрофен, мелоксикам) — габапентин (Габамма) – при герпетической и травматической невропатии, деафферентационной прозопалгии — амитриптилин – при герпетической невропатии (постгерпетической невралгии) — Мильгамма, Мильгамма композитум — Физиотерапия, рефлексотерапия |
Пациентам, длительно страдающим от непереносимой боли, и при неэффективности консервативной терапии в случае классической ТН рекомендуется хирургическое лечение. В настоящее время используются следующие подходы:
- хирургическая микроваскулярная декомпрессия;
- стереотаксическая лучевая терапия, гамма-нож;
- чрескожная баллонная микрокомпрессия;
- чрескожный глицериновый ризолизис ;
- чрескожное радиочастотное лечение Гассерова узла.
В заключение заметим, что лечение ТН должно носить мультидисциплинарный характер, при этом c пациентом должны быть обсуждены выбор различных методов лечения и риски возможных осложнений.
Прогноз посттравматической нейропатии
Важно! Невозможно классифицировать степень и прогноз повреждения сенсорного нерва, основываясь на клинических данных раннего периода после травмы. Таким образом, чтобы оценить реальный результат повреждения нерва, необходимо провести повторный опрос, осмотр и тестирование пациента через 2 — 3 недели медикаментозного лечения.
Прогноз восстановления после повреждения нижнего альвеолярного нерва во время имплантации:
Полное восстановление– 50%
Частичное восстановление – 44%
Без признаков восстановления – 6%