Нарушение, приобретённое в результате постепенного прогрессирующего разрушения у больного нервных клеток, которые отвечают за координационные функции известно, как болезнь Паркинсона. Начальная симптоматика болезни – тремор (дрожь) мышечных тканей, неустойчивость некоторых частей тела в состоянии покоя (кисти, пальцы, голова). Такие симптомы наиболее распространены среди граждан возрастом 55-60 лет, но также зафиксированы случаи, когда болезнь начинала проявляться у граждан до 40 лет. По мере развития заболевания человек полностью теряет какую-либо физическую активность и интеллектуальные способности, всё это ведёт к угасанию жизнедеятельности и смерти. Это заболевание является одним из самых тяжёлых в лечении. Как много времени может прожить человек с таким диагнозом при современной медицине? Проживание и уход в специализированных пансионатах для пожилых существенно увеличивают продолжительность жизни с данным недугом.
Возникновение болезни Паркинсона
Вся система координации движений человека контролируется его ЦНС, которая включает в себя головной, а также спинной мозг. Едва больной подумает сделать какое-либо движение, отдел коры его мозга производит активизацию всех частей нервной системы, отвечающих за физическую активность. Базальные ганглии – это одна из таких частей. Это вспомогательный двигательный механизм, ответственный за быстроту движения, качество и точность исполнения.
Сигналы об активности идут от коры человеческого мозга в отделение базальных ганглиев. Ганглии отвечают за определение конкретных, участвующих в процессе движения, мышц, за работу каждой из них и степень их напряжения. Всё это происходит, чтобы точность и целенаправленность движений соответствовала намерениям.
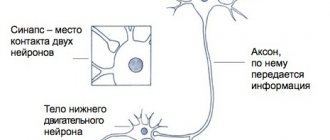
Импульсы от базальных ганглий передаются при помощи нейромедиаторов (особых химических веществ). От количества таких веществ и процесса их воздействия зависит работа мышц.
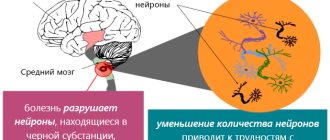
Один из важнейших нейромедиаторов – это дофамин, он способствует торможению нервных сигналов, контролируя точность и силу сокращения каждой из мышц. В сложнейшей координации движений часть работы делает «Чёрная субстанция», доставляя дофамин в полосатое тело, тем самым от базальных ганглиев идут сигналы к остальным отделам головного мозга. “Чёрная субстанция” имеет такое название из-за окраса этой структуры мозга в тёмный оттенок, так как побочный продукт биосинтеза дофамина – меланин, находится там в большом количестве. Так вот, к болезни Паркинсона приводит недостаточное содержание в чёрной субстанции дофамина.
Причины болезни, есть ли повод беспокоиться
Четко выявленных причин развития заболевания до сих пор не установлено. Один из основных факторов, приводящих к болезни Паркинсона – генетическая предрасположенность. По статистике у 15 больных из 100 в роду встречалось это заболевание.
Статьи по теме
- Формы аутизма у взрослых людей 25.09.2021
- Необходимая помощь подросткам с аутизмом 21.09.2021
- Стадии алкоголизма у женщин: главные признаки 24.06.2021
- Раздвоение личности: симптомы и признаки заболевания у женщин 24.06.2021
В 20% случаев паркинсонизм является осложнением течения других заболеваний. В остальных случаях, что именно служит толчком, не может быть определено.
Считается, что на развитие болезни влияет общая экологическая обстановка и среда проживания:
- качество потребляемой воды и пищи;
- чистота воздуха;
- имевшее место отравление токсическими газами и другие обстоятельства.
Чем раньше будут замечены симптомы болезни Паркинсона у женщин и начато лечение, тем лучше можно стабилизировать состояние и затормозить развитие заболевания.
Что такое болезнь Паркинсона
Заболевание Паркинсона – это нейродегенеративная болезнь мозга, медленно развивающаяся в большинстве случаев. В течение многих лет симптомы этой патологии могут незаметно прогрессировать. Из-за смерти значительного количества нейронных клеток в участках базальных ганглий и деградации нервных волокон и возникает эта болезнь. Симптоматика болезни Паркинсона начинает активно проявляться при нарушениях функций 80% нейронных связей. В подобных случаях заболевание Паркинсона неизлечимо и развивается с течением времени, несмотря на всю предпринимаемую терапию.
Нейродегенеративные болезни – это группа заболеваний, которые медленно развиваются, и характерны наследственными или приобретёнными поражениями ЦНС.
Ещё одна специфическая особенность болезни Паркинсона – это резко сниженное количество дофамина. Его количество перестаёт быть достаточным для необходимого торможения нервных импульсов, истекающих от коры мозга головы. Благодаря этому нервные импульсы идут прямиком к мышечной ткани, стимулируя её напряжение. Это характерно для самых ярких проявлений болезни Паркинсона: сокращения мышц (дрожь и тремор), скованность мышечной активности, обусловленная чрезмерно высоким тонусом, проявления ненамеренных движений тела.
Опасность болезни Паркинсона
Главная опасность болезни Паркинсона состоит в том, что больной может стать полностью недееспособным, прикованным к кровати.
Что касается инвалидности, то первая группа присваивается пациентам, у которых ярко выражены нарушения работоспособности, утрачена способность к самообслуживанию. Вторая группа инвалидности дается больным, у которых возникают серьезные трудности в процессе передвижения. Третья группа присваивается в случае умеренных трудностей самообслуживания и передвижения, когда ограничения трудоспособности минимальны.
Продолжительность жизни при болезни Паркинсона
Болезнь Паркинсона – это хроническое заболевание. Она не подлежит полному излечению. Продолжительность жизни людей, у которых диагностирована патология, зависит от своевременной постановки диагноза. Если болезнь обнаруживается на ранних стадиях и медицинское лечение подобрано грамотно, продолжительность жизни почти не изменяется. При этом больной должен делать гимнастику, массаж, соблюдать диету, выполнять все врачебные рекомендации.
При отсутствии адекватной лечебной терапии и быстром прогрессировании заболевания летальный исход может наступить через 5-7 лет.
Болезнь Паркинсона и Паркинсонизм
Существует два вида:
- «Первичный паркинсонизм» или болезнь Паркинсона. Это необратимый, довольно часто встречающийся случай.
- «Вторичный паркинсонизм». Характерен поражениями мозга в результате инфекционных или травматических случаев. Как правило, поддаётся лечению и восстановлению. Может возникать в любом возрасте под влиянием внешних факторов.
Привести к вторичному паркинсонизму может:
- Различные травмы мозга.
- Различные токсические отравления.
- Энцефалит.
- Поражения сосудов в головном мозге (ишемическая болезнь, инсульт или атеросклероз и пр.).
Диагностика болезни Паркинсона
Клиническая диагностика заболевания проходит в три этапа.
I этап
Осуществляется распознавание синдрома паркинсонизма и сопоставление его симптомов с другими психопатическими и неврологическими патологиями, проявляющимися аналогичным образом. Главным признаком болезни является гипокинезия, совмещенная с мышечной ригидностью, тремором покоя либо постуральной неустойчивостью. При этом она не связана со зрительными, мозжечковыми и вестибулярными нарушениями.
II этап
Предусматривает исключение наличия других заболеваний, проявляющихся синдромом паркинсонизма. Врач обращает внимание на ряд критериев:
- продолжительная ремиссия;
- окулогирные кризы (судороги взора);
- использование нейролептиков перед проявлением первых симптомов заболевания;
- яркое проявление деменции;
- рефлекс Бабинского;
- проявление вегетативной недостаточности;
- мозжечковые симптомы;
- одностороннее проявление патологии на протяжении более чем 3 лет;
- надъядерный паралич взора;
- отсутствие эффекта от приема Леводопы;
- выявленную открытую гидроцефалию/опухоль головного мозга;
- наличие в анамнезе инсультов с прогрессированием симптомов болезни Паркинсона;
- повторные черепно-мозговые травмы.
III этап
Выявляются симптомы, которые позволяют точно поставить диагноз. Для этого необходимо наличие как минимум трех критериев из списка:
- наличие тремора покоя;
- большая выраженность симптомов на той стороне тела, с которой болезнь дебютировала;
- наличие реакции на прием Леводопы;
- эффективность Леводопы на протяжении не менее 5 лет;
- продолжительность болезни от 10 лет;
- прогрессирующее течение заболевания.
При обследовании пациентов с симптомами болезни Паркинсона используются:
- Электроэнцефалография (ЭЭГ). Осуществляется регистрация биологических сигналов, идущих от клеток мозга. Оценивается функциональная активность головного мозга, диагностируются имеющиеся в ней патологические нарушения.
- МРТ головного мозга. Дает возможность увидеть мозговые структуры и визуализировать имеющиеся в них патологические образования, оценить параметры пульсового кровотока в капиллярных артериях, выявить функциональные зоны мозга.
- КТ головного мозга. В ходе обследования изучают структуру мозговой ткани, строение ликворной системы. Методика позволяет распознать аномальные процессы, протекающие в головном мозге, и осуществить динамическое наблюдение за течением заболевания, эффективностью проводимого лечения.
- Реоэнцефалография. Метод направлен на исследование кровенаполнения вен шеи и головы. Дает возможность изучить параметры пульсового кровотока в артериях мозга, венозный отток из полости черепа.
Дифференциация диагноза
Очень важно в ходе диагностических мероприятий дифференцировать болезнь Паркинсона от других патологий, проявляющихся синдромом паркинсонизма. Имеются в виду:
- паркинсонизм плюс;
- вторичный паркинсонизм;
- псевдопарксинсонизм.
Признаки и симптоматика
Как заметить болезнь Паркинсона?
Проявление болезни характеризуется стойкой утратой контролирования собственной физической активности:
- Тремор в состоянии покоя.
- Недостаточная подвижность и скованность мышц (ригидность).
- Сниженная скорость и недостаточный объём движений.
- Недостаточная способность удержания равновесия (неустойчивость).
Тремор покоя – это непроизвольные небольшие движения, которые проявляются в отсутствии двигательной активности. Наиболее распространёнными являются резкие подрагивания рук и наклонные движения головы.
Признаки, не связанные с движениями и координацией:
- Излишняя утомляемость.
- Проявления депрессии.
- Нарушения в обонянии.
- Излишнее выделение слюны.
- Повышенная потливость.
- Нарушения в метаболизме.
- Негативные изменения работы желудка и кишечника.
- Психозы и другие психологические отклонения.
- Дегенерация когнитивных функций.
Самыми заметными отклонениями в когнитивных функциях при паркинсонизме считаются:
- Проблемы с памятью.
- Заторможенность мыслительных процессов.
- Проблемы с ориентацией в пространстве.
Клиническая картина
Моторные симптомы
Гипокинезия
Включает в себя:
- брадикинезию – замедленность движений, истощаемость повторяющихся движений;
- олигокинезию – обеднение рисунка движений (отсутствие содружественных движений рук при ходьбе, ахейрокинез, гипомимия, микробазия, гипофония, микрография);
- акинезию — затруднение начала движений, застывания, затруднения при вставании со стула.
Ригидность
Повышение мышечного тонуса по пластическому типу, определяемое как сопротивление при пассивных движениях.
Тремор
Ритмичное дрожание с частотой 3–6 Гц, вовлекающее дистальные отделы конечностей, уменьшающееся или исчезающее при движении.
Постуральная неустойчивость
Нарушение рефлекторных реакций на смещение центра тяжести тела, приводящее к неспособности удерживать равновесие при изменении позы.
Нарушения ходьбы
Замедленная, «шаркающая» походка с укорочением длины шага, на поздних стадиях — с «застываниями» и непроизвольными пробежками вперёд — пропульсиями.
Немоторные симптомы
Запоры
Формирование телец Леви в структурах периферического отдела вегетативной нервной системы при БП также захватывает межмышечное нервное сплетение кишечника с развитием симпатической денервации ободочной кишки. Это проявляется клинически большей продолжительностью времени транзита пищи и развитием запоров.
Запоры, являясь одним из наиболее распространённых немоторных симптомов, встречаются у пациентов с БП значительно чаще чем в общей популяции — в 50–80% случаев. У четверти пациентов запоры возникают до появления двигательных нарушений, пациенты нередко не жалуются на них, не связывая с заболеванием. О наличии запоров необходимо опрашивать активно.
Показана статистическая связь наличия запоров со степенью тяжести болезни по шкале Хен-Яра, депрессией, тревогой и вегетативными нарушениями.
Запоры оказывают существенное влияние на качество жизни больных БП.
В исследованиях для определения запора при БП используются Римские критерии IV*:
Римские критерии запора IV
- Необходимо соблюдение 2-х и более условий**
- натуживание во время более чем в ¼ случаев (25%) дефекаций;
- стул в виде комочков или твёрдый (Бристольская шкала формы кала 1–2) более чем в ¼ случаев (25%) дефекаций;
- ощущение закупорки/нарушения проходимости заднего прохода более чем в ¼ случаев (25%) дефекаций;
- ручное пособие для облегчения дефекации используется более чем в ¼ случаев (25%) дефекаций (например, пальцевая эвакуация, поддержка тазового дна);
- менее 3-х спонтанных опорожнений кишечника в неделю.
- Дефекации без использования слабительных происходят редко.
- Недостаточно данных для установления диагноза синдрома «раздражённого кишечника».
* Соответствие критериям отмечается не более 3-х месяцев, развитие симптомов до установления диагноза отмечается не более 6 месяцев.
** При проведении клинических исследований, пациенты в состоянии соответствующем диагностическим критериям опиоидиндуцированного запора не должны получать диагноз функционального запора, поскольку сложно отличить побочные эффекты опиоидов от других причин запоров. Однако, клиницистами признаётся возможность сочетания этих состояний у одного и того же пациента.
Схема 2. Бристольская шкала формы кала
Нарушения мочеиспускания (недержание, неудержание мочи, ощущение неполного опорожнения мочевого пузыря)
Нарушения мочеиспускания встречаются при БП значительно чаще чем в сходной по возрасту контрольной группе. Нарушения удержания мочи отмечаются у 57–83%, нарушения эвакуаторной функции — у 17–27%. Это соотношение отличает больных БП от больных с мультисистемной атрофией, у которых значительно чаще встречается задержка мочи.
Наиболее частым симптомом при БП является никтурия (ночное мочеиспускание), о котором сообщают > 60% пациентов.
Императивные позывы на мочеиспускание отмечаются у 33–54%, учащённое мочеиспускание — у 16–36%.
Нарушения половых функций
Нарушения половых функций при БП могут быть как первичными, вследствие прогрессирующего поражения вегетативных ганглиев, так и вторичными, из-за двигательных и когнитивных нарушений, а также — депрессии и апатии.
Снижение интереса к сексу отмечает у себя 57%, затруднения при половом акте — 66% (Santos-García и de la Fuente-Fernández 2013). Эректильную дисфункцию и другие связанные с эрекцией проблемы отмечают у себя 79% пациентов. Проблемы пациенток связаны с непроизвольным мочеиспусканием во время полового акта, снижением любрикации и вагинизмом.
У ряда пациентов может возникать гиперсексуальность, как нежелательный эффект дофаминергической терапии (значительно чаще, при приёме ДА, чем леводопы).
Нарушения половых функций оказывают существенное влияние на общее качество жизни больных БП. Важной проблемой является низкое внимание клиницистов к этим нарушениям.
Ортостатическая гипотензия
Ортостатическая гипотензия (ОГ) — это снижение артериального давления более чем на 20 мм рт. ст. при переходе из положения лёжа в положение стоя.
ОГ может протекать без симптомов, а также иметь клинические проявления: повышенную утомляемость, головокружение/ощущение лёгкости в голове, боль в шейном отделе позвоночника (иногда, с иррадиацией в затылочную область или плечи), синкопальные состояния.
Состояние с функционально значимыми нарушениями развивается у 20–30% больных БП. К этому времени заболевание, как правило протекает в течение 10 и более лет, в отличии от мультисистемной атрофии (МСА), когда ОГ встречается у большинства пациентов и развивается через 2–3 года с начала заболевания.
Механизмы развития ортостатической гипотензии при БП и МСА могут отличаться: при МСА в основе нарушения лежит поражение вегетативных структур центральной нервной системы, при БП основную роль играет денервация периферических симпатических структур на поздних стадиях, что подтверждается многочисленными исследованиями с проведением сцинтиграфии миокарда с использованием МЙБГ (метайодбензилгуанидин) при обоих заболеваниях.
Вегетативные нарушения, в том числе ОГ, чаще встречаются у больных БП с деменцией и больных деменцией с тельцами Леви, что может указывать на связь с формированием телец Леви в структурах неокортекса и лимбической системы, а также в отделах периферической вегетативной нервной системы.
В клинических условиях ОГ выявляется при помощи ортостатической пробы. Более детальное изучение состояния возможно при проведении длительной пассивной ортостатической пробы (тилт-тест) на специальном поворотном (ортостатическом) столе. Получив положительный результат, необходимо исключить причины отличные от вегетативной дисфункции на фоне заболевания:
- приём препаратов, снижающих артериальное давление;
- гиповолемия (рвота, диарея, лихорадка, ограниченное поступление жидкости);
- сопутствующие заболевания (сахарный диабет и надпочечниковая недостаточность, алкоголизм, сердечная недостаточность).
Гипотензия и тахикардия после еды
Постпрандиальная гипотензия развивается через 15–90 минут после приёма пищи.
Природа постпрандиальной гипотензии окончательно не установлена. У пациентов не происходит адекватной симпатической компенсации при оттоке крови в органы пищеварительного тракта после приёма, что приводит к снижению сердечного выброса и периферического сосудистого сопротивления. Ещё одним механизмом может быть расширение сосудов в ответ на выброс инсулина и вазоактивного гастроинтестинального пептида.
Ортостатическая и постпрандиальная гипотензия часто развиваются у пожилых людей, не страдающих БП.
Умеренные когнитивные нарушения и деменция
Когнитивные расстройства у больных БП встречаются чаще, чем в общей популяции. С течением времени деменция развивается у 75% больных БП (маркер поздней стадии заболевания), распространённость лёгких и умеренных когнитивных нарушений (mild neurocognitive disorder по DSM-5) у больных БП оценивается в 27% (большая доля пациентов с начальными стадиями в структуре больных объясняет относительно небольшую распространённость когнитивных расстройств).
Умеренные когнитивные нарушения могут предшествовать деменции или, чаще, протекать без существенного ухудшения до конца жизни пациента.
Развитие деменции оказывает значительное влияние на течение БП: сочетается с более быстрым прогрессированием функциональных нарушений, повышенным риском необходимости помещения в больницу сестринского ухода, увеличением смертности.
Лежащие в основе патологические изменения, могут включать изменения альцгеймеровского типа и хроническое сосудистое поражение подкорковых структур, дегенеративное поражение коры с формированием телец Леви, последнее рассматривается как основной движущий фактор. На нейрохимическом уровне, развитие деменции принято связывать прежде всего с дефицитом ацетилхолина, а не дофамина.
Клинический профиль деменции при БП включает замедленность психомоторных процессов, апатию и брадифрению, нарушения процесса извлечения информации из памяти, затруднения при переключении, нарушения способности к решению проблем, зрительно-пространственные нарушения, флуктуации нарушений внимания и когнитивных нарушений, а также выраженные расстройства личности и настроения, галлюцинации и психотические нарушения, при сравнительной сохранности речевых функций и праксиса.
Для скрининга деменции при болезни Паркинсона используется Монреальская шкала оценки когнитивных функций (MoCA-тест).
Диагностические критерии когнитивных расстройств при БП
А. Соответствие критериям лёгкого/умеренного когнитивного расстройства и деменции.
B. Развитие нарушений у пациентов с установленным ранее диагнозом «болезнь Паркинсона».
C. Постепенное начало и медленное прогрессирование нарушений.
D. Нейрокогнитивное расстройство не связано с другим заболеванием и не имеет лучшего объяснения диагнозом психического заболевания.
Диагноз вероятного когнитивного расстройства устанавливается при соответствии случая всем критериям, диагноз возможного когнитивного расстройства — при несоответствии одному из критериев B или D.
Деменция при БП имеет следующие основные признаки:
- нарушения более чем в одной из когнитивных сфер (внимание, регуляторные функции, зрительно пространственные функции, память);
- более низкий уровень функционирования по сравнению с состоянием до болезни;
- нарушения выражены настолько сильно, что вызывают затруднения в повседневной жизни (утрачиваются социальные, профессиональные навыки и навыки самообслуживания), вне связи с моторными и вегетативными симптомами.
Поведенческие, нарушения, такие как апатия, изменения личности или аффективной сферы, галлюцинации, бред и повышенная сонливость в дневное время подтверждают диагноз, но не являются обязательными для его постановки.
Апатия
Апатия отмечается у 17 — 80% больных БП, значительно чаще, чем в общей популяции. В большинстве случаев, апатия сочетается с другими нейрокогнитивными нарушениями — депрессией и деменцией.
Диагностические критерии апатии Starkstein с соавт. (2009)
A. Снижение мотивации по сравнению с предыдущим уровнем функционирования пациента или привычным уровнем для его возраста или культуры.
B. Наряду со снижением мотивации, наличие хотя бы одного из симптомов, принадлежащих к каждой из трех следующих групп.
Уменьшение активности целенаправленного поведения:
- Снижение усилий или энергичности при выполнении повседневных дел.
- Зависимость от напоминаний третьих лиц при планировании ежедневных дел.
Уменьшение активности целенаправленной рассудочной деятельности:
- Снижение интереса к изучению новых вещей, получению нового опыта.
- Снижение озабоченности своими личными проблемами.
Уменьшение эмоций, сопутствующих целенаправленному поведению:
- Стойкий или уплощённый аффект.
- Снижение эмоционального ответа на положительные или отрицательные стимулы.
- Симптомы апатии вызывают клинически значимые страдания или нарушения общественной, поведенческой или других важных областях функционирования.
- Симптомы не связаны с угнетением сознания или действием психотропных веществ.
Депрессия
Клинически значимые депрессивные симптомы встречаются у больных БП с частотой 40–50%. Из них, менее чем у половины достигают достигает уровня «большой депрессии». По данным обзора Slaughter J. R. Slaughter K. A. (2001), дистимия (постоянное невротическое расстройство по определению DSM-5), малая депрессия и большая депрессия распределяются по частоте 22,5 %, 36,6 %, и 24.8 %, соответственно.
В обзоре Williams JR, Hirsch ES (2012) указывается на превосходство Гериатрической шкалы депрессии из 30 вопросов над другими инструментами при использовании у пациентов с БП.
«Золотым стандартом» выявления депрессии является клинической интервью с активным выявлением критериев этого состояния.
Для уменьшения затрат времени, используются клинические шкалы. Наибольшая точность в исследовании Goodarzi Z, Mrklas K, 2021 была показана при использовании гериатрической шкалы депрессии из 15 вопросов.
Тревога
Тревожность является одной из характерных черт личности больных БП. Распространённость тревоги и панических атак у больных БП составляет около 40%. Спектр тревожных расстройств включает в себя социофобию, паническое расстройство и неуточнённые формы тревожного расстройства. На поздних стадиях БП, развитие панических атак сочетается с периодом выключения.
Психоз
Психотические нарушения развиваются у больных БП развиваются с более высокой частотой чем в общей популяции. Их наиболее распространённое проявление — зрительные галлюцинации — в какой-либо момент времени могут испытывать 25–50% пациентов. Психоз при БП сопровождается зрительными галлюцинациями в 90% случаев. Слуховые галлюцинации встречаются редко (8–13% от числа пациентов со зрительными галлюцинациями), ещё реже бывают изолированными. Галлюцинации, как правило, кратковременные, могут возникать несколько раз в день, чаще когда на пациента не действуют раздражители — вечером, при слабом освещении, в тишине, в одиночестве.
Общепризнанных критериев диагностики психоза при болезни Паркинсона не существует, на практике удобно использование критериев предварительного диагноза психоза при болезни Паркинсона Национального института по изучению неврологических заболеваний и Национального института Психического здоровья (2007).
Критерии предварительного диагноза психоза при БП
A. Характерные симптомы. У пациента отмечается хотя бы один из нижеперечисленных симптомов:
- галлюцинации;
- иллюзии;
- ощущение, что в помещении находится кто-то посторонний (»малые» галлюцинации);
- бредовые идеи.
B. Диагноз основного заболевания. Симптомы развиваются у пациентов с диагнозом БП, установленным в соответствии с критериями Банка головного мозга Великобритании.
C. Последовательность развития симптомов психоза. Симптомы из группы А возникают у пациентов после развития БП.
D. Продолжительность симптомов. Симптомы из пункта А возникают повторно или сохраняются в течение ≥1 месяца.
E. Исключение других причин. Симптомы из пункта не имеют более вероятного объяснения диагнозом, альтернативным БП: деменция с тельцами Леви, психическими заболеваниями, такими как шизофрения, шизоаффективное расстройство, бредовое расстройство, аффективные расстройства с психотическими симптомами или общесоматические заболевания, включая осложнённые делирием.
Дополнительные характеристики психоза (укажите):
- с сохранением/без сохранения критики;
- с деменцией/без деменции;
- на фоне лечения/без лечения БП (укажите медикаментозное, хирургическое, иное лечение).
Факторами риска развития психозов при БП являются пожилой возраст возраст, сопутствующие нарушения (депрессия, нарушения поведения во сне с быстрым движением глаз, зрительные нарушения), приём дофаминергических препаратов, высокая тяжесть симптомов и длительность заболевания > 10 лет, госпитализация.
Психозы у больных БП с деменцией развиваются с частотой до 70%, а при отсутствии деменции — лишь 10%. У недементных пациентов с психозами в анамнезе отмечаются худшие оценки немедленного воспроизведения слов и речевой активности, чем у недементных пациентов без психоза. Эти факты объясняются патогистологистолоческими данными о большей распространённости телец Леви в парагиппокампальной и нижневисочной областях коры у пациентов психозами при БП.
Расстройства контроля импульсивного поведения
Расстройства включают в себя игроманию, склонность к азартным играм, непреодолимое желание есть, делать покупки; пандинг — бессмысленная сортировка или раскладывание предметов.
Нарушения сна
Нарушения сна один из наиболее распространённых немоторных симптомов БП, встречается с частотой от 41,1% у первичных пациентов до 78,3% у пациентов на распространённых стадиях заболевания.
Нарушения вызываются как симптомами БП (гипокинезия, ригидность, боли), так и первичным дегенеративным поражением структур, участвующих в поддержании сна (нарушения поведения во сне с быстрым движением глаз, синдром «беспокойных ног»). Они включают в себя как ночные (нарушение удовлетворённости ночным сном, частые пробуждения ночью), так и дневные (повышенная сонливость в дневное время).
Варианты заболевания молодых людей.
Бывают случая, когда болезнью Паркинсона заболевают молодые люди от 20 до 40 лет возрастом – это так называемый «ранний паркинсонизм». Но таких больных не много, по статистике от 10% до 20%. Люди с таким диагнозом имеют те же симптомы болезни, но они менее выражены и развиваются значительно медленнее, чем у престарелых.
Как проявляется у молодых:
- У многих пациентов заболевание проявляется как болезненные спазмы мышц конечностей тела (стопы, пальцы, плечи). Такой признак может осложнять диагностику болезни, так как очень похож на симптоматику артрита.
- Нежелательная двигательная активность тела и конечностей, зачастую возникающая из-за терапии дофаминовыми лекарствами.
Далее развиваются симптомы характерные для обычного прогрессирования заболевания.
Диагностика.
В данное время нет объективных анализов, результаты которых могут говорить о наличии болезни Паркинсона.
Основываясь на проявлениях болезни, на заключениях о физическом осмотре и результатам некоторых анализов ставится диагноз. Лечащий врач может направить на определённую диагностику (включая анализы), которая поможет распознать и исключить другие болезни, вызывающие подобные проявления.
Основным признаком наличия болезни Паркинсона является позитивные изменения, и заметное снижение симптомов болезни после назначения и приёма противопаркинсонических лекарств.
Также в современном мире есть ещё одна методика диагностирования – это «Позитронно-эмиссионная томография» (ПЭТ). В ряде обстоятельств при использовании ПЭТ получается выявить недостаточное содержание дофамина в отдельных участках мозга, что и является первопричиной болезни Паркинсона. Но такая методика очень редко используется для диагностического обследования болезни Паркинсона, так как является довольно дорогой и не многие медицинские учреждения обеспечены таким оборудованием.
Симптомы и признаки болезни Паркинсона у женщин
Основной признак болезни – замедленность движений и скованность. С развитием заболевания нарушается походка — она становится шаркающей, а шаги – мелкими.
Но первые признаки Паркинсона у взрослых женщин обычно другие:
- появление тремора одной из рук, даже в состоянии покоя;
- снижение выразительности лица;
- ухудшение ловкости;
- затрудненное выполнение многих простых действий, например, вставание со стула или переворачивание в кровати.
Дрожание верхних конечностей может увеличиваться при необходимости выполнять какие-либо действия:
- писать;
- чистить зубы;
- набирать текст на компьютере и так далее.
Болезнь Паркинсона симптомы и признаки у женщин имеет сначала неяркие, которые долго могут быть незаметными для окружающих. Особенно когда нарушение координации чередуется со всплесками физической активности. У женщин старшей возрастной категории такие проявления спада в ловкости могут списываться на возрастные изменения, что откладывает начало лечения.
Нарушения в работе мышц затрагивают также гортань. При этом может происходить даже непроизвольное слюнотечение.
Паркинсон у молодых женщин диагностируется очень редко, так как в преимущественном большинстве случаев болезнь поражает людей старше 55-60 лет.
В молодом трудоспособном возрасте проявления симптоматики быстрее будет замечено. Но диагноз может быть поставлен лишь после обследования, которое включает прохождение электромиографии.
Поставить точный диагноз больному может только врач, так как симптоматика заболевания может быть смазанной, и свойственной, кроме болезни Паркинсона, другим патологическим состояниям.
Стадии развития болезни Паркинсона
«1я стадия»
Некоторые нарушения движений одной из рук. Также имеют место неспецифичные проявления: понижение чувствительности обоняния, хроническая усталость, нарушения режима сна и отклонения в настроении. При волнении проявляются подрагивания в пальцах рук. При прогрессировании дрожь усиливается и появляется тремор в состоянии покоя.
«Полуторная» или «промежуточная стадия»
Сильные проявления признаков болезни в одной из частей тела или руке. Постоянная дрожь, исчезающая исключительно во сне. Портится качество мелкой моторики рук, проявляющаяся в изменении почерка. Становится заметной скованность шеи и части верхней спины, ограничиваются размахивающие движения обеих рук при процессе ходьбы.
«2я стадия»
Симптомы отклонения в регулировании движений имеют место в обоих сторонах туловища. Также возможна дрожь нижней челюсти и языка. Нарушения в движении суставов, заметное изменение мимики и заторможенность речи. Изменения в потоотделении: слишком жирная кожа или, наоборот, слишком сухая. Иногда больной имеет способность контролировать непроизвольные движения. Больной может выполнять простые дела и действия, но скорость их исполнения значительно замедляется.
«Зя стадия»
Значительно заметнее становится скованность мышц (ригидность) и гипокинезия. Заметно изменяется походка, которая имеет вид «марионетки», выражаясь в параллельно ставящихся стопах и мелких шагах. Выражение лица принимает вид «маски». Возможно появление дрожания головы, как покачивающихся движений (вертикально либо горизонтально). Заметно меняется, часто проявляющаяся поза: полусогнутые ноги, положение таза полуприсядь, сутулая спина с прижатой и опущенной вперёд головой, при этом при этом руки немного согнуты в локтях и прижимаются к туловищу (поза «попрошайки»). Характерные движения в суставах рывками. Развиваются отклонения в речи – человек начинает зацикливаться на одних и тех же словах. Человек всё ещё в состоянии сам себя обслуживать, но испытывает при этом огромные затруднения. Сложно даётся застёгивание пуговиц и попадания рук в рукава. На простые процедуры гигиены тратиться значительно больше времени.
«4 стадия»
Начинает быть заметна постуральная неустойчивость – человеку сложно балансировать при выполнении посадки либо вставания с кровати (есть большая вероятность завалиться вперёд). Если чуть-чуть толкнуть больного, находящегося стоя в состоянии покоя, то он будет двигаться по инерции в направлении толчка, пока не упрётся в препятствие. Бывают падения, которые заканчиваются переломами конечностей. Во время сна особо тяжело даётся изменение положения туловища. Деградирует речь больного – она становится тише и имеет «смазанный» характер. Возможны острые проявления депрессии, выраженные в попытках суицида. Есть вероятность прогрессирования деменции. Без посторонней помощи человек больше не может справляться с повседневными заботами и делами самообслуживания.
«5 стадия»
Это последняя степень развития заболевания Паркинсона, и она характерна развитием и усилением всех нарушений в движениях. Человек больше неспособен самостоятельно ходить, сидеть и вставать. Не имеет возможности питаться самостоятельно – это происходит не только из-за дрожи в конечностях и скованности в мышцах, но и из-за невозможности глотать пищу самостоятельно. Теряется контролирование мочеиспускания. Его речь становиться крайне непонятной и человек начинает нуждаться в постоянной заботе и помощи окружающих. Зачастую к этим проявлениям прибавляются тяжёлые приступы депрессии и деменция.
Деменция – это заболевание, характерное поражением когнитивных функций в значительно большей степени, чем это происходит при старении. Проявляется в утрате способности обучения и познавания новой информации при потере ранее полученных знаний.
Симптомы болезни Паркинсона
Симптомы болезни Паркинсона на ранней стадии могут быть малозаметными. Сначала больной замечает у себя дрожание либо неловкость в одной руке или ноге. Возникает общая скованность, походка затрудняется. Амплитуда движений тремора в начале болезни может менять степень выраженности – усиливаться после эмоциональных переживаний, уменьшаться после отдыха. Со временем наблюдается ограничение подвижности при шевелении пораженной ноги/руки. Спина становится более сутулой. Длина шага укорачивается.
К первым признакам болезни Паркинсона у женщин и мужчин также относятся:
- боль в конечностях, спине;
- чувство сжатия в области икроножной мышцы/плеча;
- мышечные судороги;
- бессонница;
- повышенная утомляемость;
- депрессия.
Помимо этого, могут возникать некоторые вегетативные расстройства: импотенция, запоры, нарушения мочеиспускания и потоотделения, ортостатическая гипотензия, себорейный дерматит.
Основными признаками болезни Паркинсона при уже развившейся клинической картине являются:
- Ригидность. Тонус мышц повышается, появляется повышенное сопротивление пассивным движениям. Оно может быть прерывистым либо монотонным (в первом случае говорят о феномене «зубчатого колеса», во втором – о феномене «восковой куклы»).
- Гипокинезия. Инициация произвольных движений становится затруднительной, больной становится медлительным. Он не может генерировать адекватное по темпу и силе мышечное усилие. К симптомам данного состояния относят:
— тихую речь (гипофония);
— бедность реакций лицевой мимики (гипомимия);
— очень редкое мигание;
— мелкий почерк (микрография);
— укорочение длины шага (брахибазия);
— затруднения при поднятии со стула, ходьбе, поворотах в стороны;
— уменьшение размахивания руками во время передвижения (ахейрокинез).
- Постуральная неустойчивость. В норме постуральные рефлексы помогают поддерживать равновесие во время ходьбы, стояния на месте. Если они ослабевают, человек не может удержаться, когда встает, ходит, совершает повороты. Из-за этого он часто падает. Стремясь встать и пойти, он изменяет направление своего движения. Со стороны это выглядит как топтание на одном месте.
- Тремор покоя. Начинают дрожать конечности, голова. Движения рук напоминают «счет монет». Патология может быть односторонней или ассиметричной. Она наблюдается в 80-85% случаев.
Помимо названных симптомов, при болезни Паркинсона могут возникать:
- слюнотечение;
- деменция;
- синдром беспокойства ног;
- дисфагия (затрудненное глотание);
- дизартрия (нарушение произношения).
Если Вы обнаружили у себя схожие симптомы, незамедлительно обратитесь к врачу
. Легче предупредить болезнь, чем бороться с последствиями.
Причины болезни Паркинсона
Докторам и учёным не удаётся распознать и выявить конкретные первопричины, развития болезни Паркинсона, однако, есть несколько фактов, возможно, провоцирующих прогрессирование этой болезни:
- Одной из причин может стать старение. Так как при старении резко уменьшается количество нервных связей и клеток, что, в свою очередь, приводит к уменьшению необходимого количества дофамина в частях мозга (в базальных ганглиях).
- Наследственный фактор. Генетическая расположенность пока что не доказана, но у 20% людей, имеющих эту болезнь есть родственники с проявлениями паркинсонизма.
- Окружающая среда. Может привести к токсическим отравлениям мозга, из-за наличия в воздухе, воде или пище токсических соединений, ядовитых веществ, пестицидов и тяжёлых металлов, которые могут повлечь за собой гибель смерть большого числа нервных клеток и подтолкнуть к болезни.
- Использование медикаментозных препаратов. Антидепрессанты и другие нейролептические лекарства, изменяющие метаболизм и выработку дофамина в ЦНС, могут вызывать побочные действия, очень похожие на симптомы паркинсонизма.
- Заболевания и травмирование головного мозга. Сотрясения мозга, разнообразные ушибы головы, вирусный или бактериальный энцефалит – всё это может привести к повреждению отделов базальных ганглий и спровоцировать прогрессирование болезни Паркинсона.
- Образ жизни. Неправильные режим сна (недосыпание), регулярные стрессы, вредное питание, нехватка витаминов в организме и прочие факторы могут вызывать некоторые патологии.
- Прочие болезни. Например, атеросклероз, разнообразные злокачественные опухоли в головном мозге, нарушения в работе эндокринной железы тоже могут спровоцировать осложнения, ведущие к заболеванию Паркинсона.
Паркинсонизм и его основные нозологические формы
Болезнь Паркинсона (БП) – хроническое, неуклонно прогрессирующее заболевание центральной нервной системы с дегенерацией нигростриарных нейронов и нарушением функции базальных ганглиев. Она относится к одним из наиболее частых нейродегенеративных заболеваний, которые стоят на третьем месте среди причин смертности после сердечно-сосудистых и онкологических заболеваний.
Паркинсонизм известен давно, первые сообщения о лечении похожих расстройств были сделаны 1000-2500 лет до н.э.
Первое клиническое описание принадлежит английскому врачу Джеймсу Паркинсону, который опубликовал в 1817 году «Эссе о дрожательном параличе».
Подробный клинический анализ комплекса патологии был сделан в 1879 г. знаменитым французским неврологом Жаном Мартеном Шарко.
В настоящее время в классификации паркинсонизма выделяют: I. Болезнь Паркинсона (она составляет около 70-80% всех регистрируемых случаев). II. Вторичный (симптоматический) паркинсонизм (около 15%) включает следующие варианты: лекарственный, токсический, постгипоксический, энцефалитический, травматический, при объемных процессах, при гидроцефалии, сосудистый. III. Паркинсонизм при различных дегенеративных заболеваниях с поражением экстрапирамидной системы («паркинсонизм-плюс», около 10%): мультисистемные атрофии (стриатонигральная дегенерация, оливопонтоцеребеллярная дегенерация), прогрессирующий надъядерный паралич (болезнь Стила-Ричардсона-Ольшевского), кортикобазальная дегенерация, деменция с тельцами Леви, паркинсонизм-БАС-деменция, болезнь Вильсона-Коновалова, болезнь Гентингтона (ювенильный вариант Вестфаля), болезнь Фара (идиопатическая кальцификация базальных ганглиев), болезнь Альцгеймера, другие.
Основной нозологической формой паркинсонизма является болезнь Паркинсона.
Распространенность БП во всем мире составляет приблизительно 1% .
Этиология БП неизвестна. В основе ее патогенеза лежит дегенерация так называемых дофаминергических нейронов. БП носит преимущественно спорадический характер, однако при наличии БП у ближайших родственников риск ее развития возрастает.
Клинические проявления БП возникают при уменьшении количества дофамина в хвостатом ядре и скорлупе не менее чем на 70%. Симптомы БП развиваются постепенно, вовлекая сперва конечности на одной стороне. Для клинической картины БП характерно сочетание гипокинезии, ригидности, тремора покоя, и постуральных нарушений.
Гипокинезия проявляется снижением двигательной активности, замедленностью движений, уменьшением амплитуды действий.
Тремор покоя в классических случаях начинается с дистальных отделов верхней или нижней конечности и напоминает движения рук «при счете монет или скатывании пилюль». В дальнейшем в тремор вовлекается гомолатеральная конечность, нижняя челюсть, противоположные конечности. Иногда отмечается постуральное дрожание рук.
Ригидность при БП проявляется пластическим повышением мышечного тонуса, часто — с феноменом «зубчатого колеса», нарастающим в процессе исследования. Постуральная неустойчивость, возникающая на развернутых стадиях БП, характеризуется неустойчивостью при поворотах, пошатыванием при ходьбе, падениями. В дальнейшем больные вынуждены использовать опорные приспособления.
Кроме двигательных нарушений, при БП части развиваются недвигательные проявления: нервно-психические расстройства; нарушения сна; вегетативные нарушения; чувствительные нарушения.
В зависимости от преобладания того или иного симптома в клинической картине БП принято выделять следующие клинические формы заболевания: дрожательную, акинетическую, а также смешанные формы — акинетико-ригидную и ригидно-дрожательную.
Выделяют пять степеней тяжести БП (стадии болезни по Хен и Яру): 1-я стадия — односторонние симптомы паркинсонизма; 2-я стадия — двусторонние симптомы паркинсонизма без постуральных нарушений; 3-я стадия — присоединяется умеренная постуральная неустойчивость; 4-я стадия — значительное ограничение двигательной активности, падения, но при этом еще сохраняется возможность самостоятельно передвигаться; 5-я стадия — больной прикован к постели или инвалидному креслу.
На поздних стадиях БП клиническая картина видоизменяется, появляются дополнительные моторные (двигательные флуктуации, лекарственные дискинезии, нарушения ходьбы, падения, застывания и акинетические кризы) и немоторные (вегетативные, когнитивные, нейропсихические) синдромы.
У больных могут возникать длительные периоды декомпенсаций — от нескольких дней до нескольких недель, а также акинетические кризы — тяжелые эпизоды акинезии, сопровождающиеся дисфагией, вегетативными нарушениями, гипертермией, олигурией, спутанностью сознания. Причинами этого могут являться: нарушение схемы приема противопаркинсонических средств, их полная о); прием препаратов, блокирующих ДА-рецепторы (прежде всего нейролептики); обострение сопутствующих соматических заболеваний, стресс; операции, травмы, дегидратация организма.
Диагностировать БП с уверенностью можно только с помощью аутопсии. Клиническая диагностика синдрома паркинсонизма требует обязательного наличия гипокинезии и не менее одного из трех основных симптомов паркинсонизма: тремора покоя, ригидности и постуральной неустойчивости.
Проведение МРТ головного мозга является обязательным при наличии у больного синдрома паркинсонизма. Данное исследование прежде всего необходимо для дифференцирования идиопатической болезни Паркинсона и вторичного паркинсонизма, а также «паркинсонизма-плюс».
Основными направлениями лечения БП являются: 1. Фармакотерапия. 2. Медико-социальная реабилитация. 3. Лечебная физическая культура (ЛФК). 4. Нейрохирургическое лечение.
Фармакотерапия при БП направлена на нормализацию биохимического дисбаланса и требует постоянного приема лекарственных средств, так как при прекращении лечения симптомы БП возвращаются к исходному уровню.
На ранней стадии лечение БП заключается в назначении монотерапии с последующим переходом на комбинированное лечение.
На ранних стадиях заболевания общепринятым является назначение больным в возрасте до 70 лет агонистов ДА-рецепторов и ингибиторов МАО-В в виде монотерапии или сочетания.
У пациентов старше 70 лет, когда ожидаемая продолжительность жизни больного меньше, а также имеются когнитивные нарушения, терапию можно сразу начинать с ДОФА-содержащих препаратов в минимальной эффективной дозе, которую подбирают постепенно.
Холинолитики (Циклодол, Акинетон) назначаются преимущественно на ранней стадии БП — в виде монотерапии или в комбинации с другими противопаркинсоническими средствами; они преимущественно влияют на тремор покоя.
В настоящее время их назначают лишь молодым пациентам, с выраженным тремором покоя и сохранными когнитивными функциями. Высокая частота побочных эффектов и низкая эффективность по сравнению с другими группами существенно ограничивают их применение. Препараты амантадина (Мидантан, ПК-Мерц).
Амантадины могут назначаться как при начальной стадии в виде монотерапии, так и в комбинации с другими противопаркинсоническими средствами на поздних стадиях БП. Препараты эффективны и для уменьшении степени выраженности дискинезий, вызванных приемом леводопы. Инфузионная форма амантадина сульфата (ПК-Мерц) применяется при лечении декомпенсаций и акинетических кризов при БП.
Агонисты дофаминовых рецепторов обладают способностью непосредственно стимулировать ДА рецепторы в головном мозге. Неэрголиновые агонисты ДА-рецепторов (Проноран, Мирапекс, Реквип Модутаб, Ньюпро) широко применяются на всех стадиях БП. Помимо контроля двигательных нарушений, у них выявлен антидепрессивный эффект, что очень важно, так как частота депрессивного синдрома при БП достаточно высока.
Монотерапия АДАР на ранних стадиях заболевания позволяет отсрочить назначение препаратов леводопы, а также развитие моторных флюктуаций и лекарственных дискинезий.
Ингибиторы МАО типа В (Разагилин). Назначение препаратов этой группы приводит к увеличению количества дофамина в нейронах. Также предполагается наличие у них нейропротекторного действия. Могут назначаться на ранних стадиях в виде монотерапии, а также в комбинации с леводопой.
Ингибиторы КОМТ. Ингибиторы КОМТ увеличивают биодоступность леводопы, уменьшая уровень ее неактивных метаболитов.
Ингибиторы КОМТ периферического действия не проходят ГЭБ и препятствуют метилированию леводопы в желудочно-кишечном тракте и кровеносном русле. Благодаря этому они сохраняют концентрацию леводопы на определенном уровне. К таким препаратам относится энтакапон.
Комбинация энтакапона с препаратами леводопы позволяет снизить суточную дозу ДОФА-содержащего препарата на 15–30%.
Он назначается только в комбинации с препаратами леводопы (Сталево), так как при назначении в виде монотерапии самостоятельным противопаркинсоническим эффектом не обладает.
Препараты леводопы (Мадопар, Наком, Тремонорм, Тидомет-форте, Дуэллин, Синдопа). Дофамин не проходит ГЭБ, поэтому в качестве лекарственного препарата был предложен метаболический предшественник дофамина — леводопа, которая проходит через ГЭБ и в головном мозге метаболизируется в дофамин. На сегодняшний день препараты леводопы являются наиболее эффективными лекарственными средствами, «золотым стандартом», применяющимися для лечения БП. Однако они не останавливают прогрессирование БП. Более того, в среднем после 5 лет применения ДОФА-содержащих средств у больных БП снижается их эффект, появляются двигательные флюктуации и лекарственные дискинезии.
Сроки назначения терапии препаратами леводопы зависят от степени выраженности и темпа прогрессирования заболевания, профессиональной деятельности больного, семейно-бытового статуса. В целом назначать препараты этой группы необходимо, когда имеются выраженные двигательные нарушения, которые не удается купировать другими противопаркинсоническими средствами.
Нейрохирургическое лечение.
Снижение эффективности фармакотерапии, появление моторных флюктуаций и лекарственных дискинезий являются показанием к применению нейрохирургического лечения, которое в течение последних двух десятилетий прочно заняло свое место в алгоритме ведения пациентов с БП. В настоящее время используются три типа нейрохирургических вмешательств при БП: стереотаксические деструктивные методы (вентролатеральная таламотомия, паллидотомия, субталамотомия и их комбинация), стимуляционные методы (имплантация электродов в подкорковые структуры с последующей их хронической электростимуляцией) и внутримозговая трансплантация дофаминергических нейронов мезенцефалона эмбриона человека, эффективность которой продолжает изучаться.
Наиболее современный метод хирургического лечения БП – глубокая электростимуляция головного мозга. Процедура ГСМ состоит в имплантации электродов с 4 контактами в зоны-мишени в пределах подкорковых образований головного мозга; электроды соединяются с имплантируемым под кожу стимулятором, подающим высокочастотные электрические импульсы в стимулируемое ядро.
Медико-социальная реабилитация.
Высокая степень инвалидизации при неуклонно прогрессирующей БП, социально-экономические потери, которые несет общество обусловливают необходимость создания системы медико-социальной реабилитации, которая должна включать в себя диспансерное наблюдение больных; создание школ для пациентов и их родственников ведение обучающих программ и психотерапевтических занятий, создание общественных организаций, групп поддержки. Большое значение имеет ЛФК, которая может подбираться индивидуально в зависимости от степени тяжести болезни у конкретного больного, занятия ЛФК в группах, танцевальная терапия, а также трудотерапия, физиотерапия.
Литература: 1. Шток В. Н., Диагностика и лечение экстрапирамидных расстройств. — М., 2000. — С. 138. 2.Шток В. Н., Федорова Н. В. Лечение паркинсонизма. — М., 1997. — 194 с. 3.Яхно Н. Н. Современные подходы к лекарственному лечению болезни Паркинсона // Клиническая фармакология и терапия. — 1994. — № 3-4. — С. 92 — 97. 4.Левин О.С., Федорова Н.В., Болезнь Паркинсона.- М., — 2012. 5. Н.В. Федорова, И.П. Чигирь, Болезнь Паркинсона – Лечащий врач.- 2005г. -№8.- с.26-28.
Как лечат болезнь Паркинсона.
- На первых этапах болезни Паркинсона её лечат с применением медикаментозных средств, вводя в организм вещества, которых не хватает. Основной целью медикаментозной (химической) терапии является «чёрная субстанция». При использовании такого метода лечения, почти у всех больных заметно снижается проявления симптомов и у них появляется утерянная возможность нормально жить.
- Но бывают случаи, когда у больных не происходит улучшений, даже на протяжении длительного времени приёма препаратов и увеличения их дозировок. В таких случаях применяется операция на головном мозге, посредством которой в мозг вживляется стимулятор.
Такая операция имеет вид высокочастотных стимулирований базальных ганглиев электрическим током посредством электрода, имеющего соединение с электростимулятором:
- При использовании местного наркоза в мозг больного вводятся последовательно два электрода (по определённому заранее компьютером пути), производящих глубокую стимуляцию отделов головного мозга.
- Под анестезией вживляется в грудную область под кожу электростимулятор, соединяющийся с электродами.
Использующиеся для лечения препараты:
«Амантадин» или «Мидантан». Это лекарственные вещества, которыми начинается терапия болезни Паркинсона. Этот медикаментозный препарат стимулирует выделение дофамина, способствует уменьшению его обратного захвата, блокируя глутаматные рецепторы, оказывает защиту «чёрной субстанции», а также имеет и другие положительные свойства. «Амантадин» значительно уменьшает проявления гипокинезии и ригидности (скованности и ограниченности в движениях), однако, почти не уменьшает тремор и дрожь. Эти лекарственные препараты хорошо переносятся и почти не имеют побочных эффектов.
«Ротиготин» или «Ньюпро». Это агонист группы дофаминовых рецепторов. Выпускается в виде пластыря, который накладывается на кожный покров. Такой пластырь – это трансдермальная терапевтическая система, имеющая размеры 10-40 cм², применяемая один раз за сутки. Такие медикаментозные препараты продаются исключительно по рецептам и используются для самостоятельной (без комбинирования с другими препаратами) терапии болезни Паркинсона на первых стадиях.
Применение этой формы препаратов имеет значительные преимущества: дозировка меньше, но эффективнее, а побочные действия имеют менее выраженный характер.
«Левопада». Уже давно считается одним из лучших медициских лекарств для лечения Паркинсонизма. Это соединение является химическим предвестником дофамина. Но стоит помнить, что это вещество имеет значительное количество побочных действий, таких как психологические отклонения. Назначается, как правило, в связке «карбидопой» или «бенсеразидом». Они приводят лучшему усвоению «леводопы» и достижения ей участков головного мозга и содействуют снижению проявлений побочных действий.
«Модопар». Является комбинированным лекарственным средством, содержащим в себе как «леовдопу», так и «бенсеразид». Производится в различных формах. «Мадопар ГСС» выпускается в специальных капсулах, плотность оболочки которых значительно меньше, чем у желудочного сока. Это содействует тому, что вещество медленно и равномерно поступает в организм, потому что такая капсула растворяется в желудке от 5 до 12 часов. Также выпускается «Диспергируемый Мадопар», который имеет жидкую форму, благодаря которой действует значительно быстрее. Этот вариант более приемлем для больных с ограниченной функцией глотания.
«Миралекс». Это лекарственное средство производится как таблетки, которые применяют как самостоятельное лекарство на первых стадиях болезни, так и как комбинированную с «леводопой» терапию на более позднем развитии болезни Паркинсона. «Миралекс» обладает меньшим количеством проявления побочных эффектов, чем у неселективных агонистов, но в то же время большим, чем у «амантадина». Такие побочные действия могут проявляться как тошнота, скачки давления, излишняя сонливость, изменение баланса выделяемых печенью ферментов, отёки нижних конечностей. А также возможны галлюцинации у больных, имеющих диагноз деменция.
«Ингибиторы МАО». Они значительно замедляют окисление дофамина, находящегося в «полосатом теле» отдела головного мозга, за счёт этого растёт его концентрация в синапсах. Наиболее частым применением в лечении болезни отличается «Селегилин». На первых стадиях болезни Паркинсона «Селегилин» применяется как самостоятельная терапия (без применения других комбинационных средств). Многие пациенты отмечают серьёзные улучшения при использовании этих средств. Нежелательные эффекты от применения «Селегилина» имеют редкое и слабовыраженное проявление.
Лечение «Селегилином» может отсрочить на время от 9 до 12 месяцев назначение «леподопы». На последних стадиях заболевания «Селегилин» используют как дополнение к «Леводопе», что позволяет последней увеличить свою эффективность на треть.
«Мидокалм». Этот препарат сильно снижает ненормально большой тонус тканей мышц. Это его свойство применяется при болезни Паркинсона как вспомогательное. «Мидокалм» выпускается в таблетках, для перорального применения и ампулах, для внутривенного и внутримышечного использования.
«Витамины группы В». Эта группа витаминов часто применяется для лечения заболеваний ЦНС. Чтобы L-Доф благополучно преобразовался в дофамин необходимы никотиновая кислота и витамин «В6». Также для повышения содержания дофамина в отделах мозга применяется «Тиамин» (витамин «В1»).
Диета при болезни Паркинсона
При болезни Паркинсона необходимо есть дробными порциями 5-6 раз в день. Основная часть сытных блюд должна употребляться до обеда. На вечер желательно оставлять легкоусваиваемую пищу.
Если мучают постоянные приступы тошноты, рекомендуется есть очень медленно. Пить только через полчаса после окончания трапезы.
Важно, чтобы питание при болезни Паркинсона было хорошо сбалансированным. При отсутствии аппетита необходимо все равно принимать пищу.
Чтобы исключить запоры, нужно обогатить рацион клетчаткой, зерновыми и молочными продуктами.