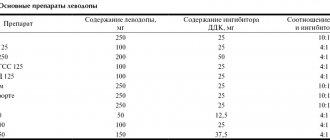
Болезнью Паркинсона страдают преимущественно лица пожилого возраста. Развивается заболевание вследствие недостатка нейромедиатора дофамина. Оно встречается у 120 – 180 человек на 100 тысяч населения. Болезнь неуклонно прогрессирует и приводит к инвалидности. Неврологи Юсуповской больницы применяют современные методики лечения болезни Паркинсона, позволяющие уменьшить выраженность симптомов и улучшить качество жизни пациентов.
Начальные проявления заболевания
От 5 до 10 % всех случаев болезни Паркинсона имеют прямую моногенную основу. В настоящее время идентифицировано более пятнадцати генов наследственных форм первичного паркинсонизма.
Остальные случаи представлены спорадической формой и их возникают под воздействием нескольких факторов. Спорадическая форма заболевания развивается в результате влияния генетических и средовых факторов. Это определяет особенности клеточной детоксикации и обмена ксенобиотиков, процессинга ряда нейрональных белков, антиоксидантной защиты, характера дофаминового обмена
Облигатным признаком заболевания является гипокинезия, т.е. замедленность, неловкость движений, обеднение двигательного рисунка, при этом мышечная сила остаётся сохранной на всем протяжении болезни. Больной испытывает некоторые трудности при выполнении таких элементарных бытовых действий:
- завязывание шнурков;
- застёгивание пуговиц
- бритьё
- пользование столовыми приборами
- просовывание руки в рукав
- затруднения письма: почерк становится мелким (микрография)
- ахейрокинез: теряется содружественноедвижение поражённой руки при ходьбе
Нередко врачи сталкиваются на практике с далеко зашедшими этапами болезни, потому что у большинства обывателей болезнь Паркинсона ассоциируется с тремором, который вовсе не обязателен при болезни Паркинсона, в то время как другие симптомы болезни пациенты игнорируют или списывают на болезни суставов или мышц.
Неврологи выделяют четыре компонента акинезии:
- нарушение моторной инициативы;
- нарушение стратегии двигательного обучения;
- нарушение кинетической «мелодии»;
- при выполнении повторных заданий происходит постепенное затухание амплитуды движений.
Если же в дебюте болезни тремор присутствует, то он обязательно односторонний как и другие признаки болезни, классический тремор при болезни Паркинсона наблюдается в покоящейся конечности, усиливается при ходьбе, но при выполнении движений поражённой конечностью тремор исчезает. Этот вид тремор является не единственным при болезни Паркинсона, но его наличие практически всегда указывает на болезнь Паркинсона. Следует отметить, что болезнь Паркинсона никогда не начинается с дрожания головы.
Для болезни Паркинсона характерны следующие симптомы:
- гипокинезия;
- тремор покоя;
- пластическая мышечная ригидность;
- постуральная неустойчивость.
Постуральная неустойчивость присоединяется на более продвинутой стадии заболевания.
Гипокинезия выявляется клинически при целом ряде произвольных движений:
- пациент застывает в различных позах, иногда напоминая манекен (не путать с истинными «застываниями», как осложнениями терапии леводопой);
- у него возникают затруднения при перемене положения тела и инициации движения;
- на лице отсутствует эмоциональная окраска (гипомимия), больной редко моргает;
- речь становится монотонной, тихой, маломодулированной, постепенно затухающей, приобретает «тремолирующий» характер;
- развивается гипофония (снижение громкости речи); брадилалия (замедленность речи), диспросодия (потеря мелодичности речи).
Для раннего выявления гипокинезии врачи Юсуповской больницы применяют следующие тесты:
- тест Фурнье. Больному предлагают максимально быстро совершать серию движений: встать, сесть, наклониться, повернуться, наклониться. Замедленность движений можно на начальной стадии гипокинезии;
- тест постукивания большим и указательным пальцами. Пациент поочерёдно обеими руками выполняет постукивания по столу указательным и большим пальцами в максимально возможном темпе и с максимальной амплитудой. При формировании гемипаркинсонизма одна рука отстаёт от темпа и амплитуды не вовлеченной пока в болезнь другой руки;
- тест сжимания и разжимания кисти: врач предлагает пациенту максимально быстро сжимать и разжимать кисть (на стороне формирующейся гипокинезии кисть отстаёт).
- Тест постукивания носком ноги
- Тест с постукиванием пяткой по полу, в обоих случаях видна асимметричность симптоматики.
Мышечная ригидность, или пластический гиперитонус, представляет собой пластическое повышение мышечного тонуса. Он повышается в начальной фазе движения и сохраняется до конца движения. Врачи во время неврологического обследования часто находят феномен Негро (симптом «зубчатого колеса»): на фоне пластического гипертонуса появляется ощущение прерывистости, ступенчатости сопротивления мышц и по мере пассивных альтернирующих движениях тонус нарастает.
Из-за повышенного мышечного тонуса, который преобладает в мышцах-сгибателях туловища, у пациента формируется своеобразная поза «просителя»: его голова опущена, ноги и руки подогнуты в коленных и локтевых суставах, стопы принимают параллельное положение друг другу. Кстати наклон туловища вперёд, наряду с тремором покоя и ахейрокинезом значительно облегчают клиническую диагностику болезни Паркинсона. После поднятия головы больного над подушкой она на некоторое время остаётся в этом положении. При выполнении теста маятникообразного качания ног движения конечностей прекращаются сразу же после выполнения теста.
Комбинированные тесты и опросники
В медицине разработаны тесты, позволяющие выявить сразу несколько нарушенных психических функций. Они состоят из множества заданий, каждое из которых отвечает за память, внимание или мышление. Широкое распространение в клинической практике получил тест на болезнь Паркинсона «Mini-Cog». В начале тестируемому называют 3 слова, не связанных между собой по смыслу. Затем пациент должен нарисовать циферблат часов, расставить на нем цифры и расположить стрелки так, чтобы они показывали определенное время (например, без двадцати четыре). После этого тестируемого просят воспроизвести слова из первого задания.
В клинической практике используется еще один комплексный тест – Монреальский опросник оценки когнитивных функций. Он применяется врачами-психиатрами для выявления деменции на фоне болезни Паркинсона. Тест считается сложным и требует 30-60 минут для прохождения. Он состоит из нескольких блоков и оценивает все высшие мозговые функции человека:
- абстрактное и пространственное мышление;
- скорость реакции;
- способность к запоминанию и воспроизведению информации;
- общий уровень интеллекта;
- внимание, его подвижность и переключаемость;
- оптико-пространственная деятельность (способность определять расположение, величину, и удаленность предмета).
Важно! Самым простым и информативным методом для выявления деменции при болезни Паркинсона является тест «Mini-Cog».
Тест на болезнь Паркинсона заключается в рисовании ломанной линии, объемного предмета (куб, параллелепипед), циферблата часов с заданным временем. В опроснике также присутствуют арифметические действия, воспроизведение названных слов, называние чисел в обратном порядке, простые логические задачи.
Недвигательные проявления болезни Паркинсона
Болезнь Паркинсона имеет целый спектр недвигательных проявлений, которые встречаются у всех пациентов независимо от стадии болезни и возраста дебюта:
- нервно-психические нарушения (эмоциональные, когнитивные, поведенческие, психотические);
- нарушения сна и бодрствования;
- сенсорные нарушения (покалывания, мурашки) и боль;
- вегетативные нарушения (очень широкий спектр нарушений среди которых наиболее дезадаптирующими являются учащённые позывы к мочеиспусканию и ортостатическая гипотезия, а самым частым симптом является запоры);
- повышенная утомляемость.
До начала появления классических моторных нарушений при болезни Паркинсона могут появляться немоторные проявления:
- запоры;
- нарушение обоняния;
- расстройства сна;
- болевые синдромы.
В связи с этим в настоящее время неврологи различают доклиническую, премоторную стадию болезни Паркинсона.
Болезнь Паркинсона: обзор всех свежих новостей
Болезнь Альцгеймера и болезнь Паркинсона — пожалуй, самые известные и самые распространенные заболевания центральной нервной системы. И распространенность их неуклонно растет: ведь мы стали жить дольше, а главный фактор риска в обоих случаях — возраст. Борьба с этими заболеваниями идет с переменным успехом. Тем не менее чаша весов склоняется — медленно, но верно — в сторону ученых.
Сегодня я расскажу вам, какие есть медицинские новости с научных фронтов борьбы с болезнью Паркинсона. Все эти «сводки» можно разделить на три группы: изучение болезни Паркинсона, ее ранняя диагностика и лечение. И чтобы стало понятно, насколько активно изучается эта болезнь, отмечу: все эти новости случились за последние три (!) месяца.
Новости про изучение болезни Паркинсона
1. Симптомы Паркинсона теперь изучают на приматах.
Японские исследователи из Университета Кэйо в Токио наконец-то смогли получить крупных модельных животных с болезнью Паркинсона. Обычно она изучается на мышах, но для того, чтобы разработать лекарства для человека, требуется проверить его действие на животных, которые по своей физиологии больше похожи на Homo sapiens.
Ученые провели генную модификацию обезьян из семейства игрунковых, вставив им в геном дефектную копию гена SNCA, связанного с болезнью Паркинсона. В итоге с самого раннего возраста обезьянки проявляли симптомы болезни: на первом году жизни они страдали расстройством сна, на втором наблюдались отложения телец Леви (патологические белковые образования) в нейронах ствола мозга, а на третьем уже вовсю отмечались двигательные нарушения.
При этом, когда несчастным животным назначили противопаркинсонический препарат леводопу, их состояние значительно улучшилось.
2. Структура альфа-синуклеина стала понятнее.
Биохимики из Университета штата Иллинойс совместно с коллегами из Университета Пенсильвании, Университета Вандербильда и Лондонского университета королевы Марии впервые сумели получить детальную структуру фибрилл альфа-синуклеина, ключевого белка болезни Паркинсона.
При этом недуге молекулы альфа-синуклеина образуют длинные фибриллы, которые нарушают работу мозга. Это чем-то похоже на амилоидные бляшки при болезни Альцгеймера, однако структура синуклеиновых фибрилл до последнего времени оставалась неясной в силу ее сложности. Теперь нейробиологам стало понятнее, как формируются эти объекты, вызывающие гибель нейронов, и как с ними можно бороться.
Новости про диагностику болезни
1. Обнаружены психологические особенности пациентов.
Команда неврологов Университета Калифорнии в Лос-Анджелесе установила, что для диагностики болезни Паркинсона на очень ранней стадии может использоваться процесс принятия решений.
Они обнаружили, что люди с ранней стадией болезни Паркинсона испытывают трудности с перцептивным (основанным на информации, получаемой от органов чувств) принятием решений в случаях, когда сенсорная информация слаба и нужно опираться на более ранний опыт.
На основании этих данных неврологи планируют выделить особую «метку», которая могла бы лечь в основу диагностического теста.
2. Выявлены биомаркеры в крови.
Ученые из Германского центра нейродегенеративных заболеваний, а также из Института клинического исследования мозга Херти и Университета Тюбингена открыли белки (если быть точным — небольшие белковые волоконца, так называемые нейрофиламенты), наличие которых в крови и ликворе (спинномозговой жидкости) отражает степень деградации нервных клеток. По крайней мере, в опытах на мышах с моделями болезней Паркинсона и Альцгеймера по концентрации этих филаментов удавалось диагностировать степень прогресса заболевания.
Такой анализ потребуется не столько для диагностики самого заболевания, сколько для того, чтобы отслеживать эффективность лечения тем или иным препаратом.
3. Найдены возможные причины поздней постановки диагноза.
Ученые из Школы медицины в Университете центра наук о здоровье Техаса установили: человек может на протяжении почти двух десятков лет жить, ходить и не знать, что в его мозге уже развивается болезнь Паркинсона. В результате первые симптомы проявляются только тогда, когда болезнь активно развивается и время может быть упущено.
Впрочем, это доказано только для мышей и экстраполировано на людей. У мышек от начала проблем с нейронами черной субстанции до симптомов прошло 14 недель. С другой стороны — не будешь же нарезать частями мозг здорового человека только для того, чтобы узнать такие новости?
Новости про терапию
1. При Паркинсоне помогает пение.
Врачи из трех больниц — Гая, Святого Томаса, Святого Хелиера — в Лондоне провели систематический обзор опубликованных данных о благотворном влиянии пения на людей с болезнью Паркинсона. Обзор преследует две основные цели — стимуляцию дальнейших исследований высокого качества в этой области и привлечение внимания клиницистов к терапевтическим возможностям, которые открывает такой простой вид досуга, как пение.
Положительная динамика в обзоре присутствует, однако авторы предлагают провести более тщательные исследования того, как пение улучшает деятельность речевого аппарата больных.
2. Создан первый препарат от галлюцинаций.
Болезнь Паркинсона требует лечения не только основной проблемы, но и сопутствующих эффектов. Например, часто бывающих при этом заболевании галлюцинаций и иллюзий. И вот в этом году FDA зарегистрировало первое в истории лекарство от подобных симптомов болезни Паркинсона. Препарат получил название Нуплазид (пимавансерин) и выпускается в таблетках.
3. Донорские нейроны заменят собственными клетками.
Хорошо известно, что при болезни Паркинсона обычно страдает так называемое черное вещество, или черная субстанция, в которой находятся нейроны, вырабатывающие дофамин.
Уже давно делались попытки трансплантации нейронов в черное вещество вместо погибших. Не так давно был опубликован удивительный результат: пересаженные нервные клетки жили и снабжали черное вещество дофамином четверть века.
Но все это — пересадка донорских нейронов. Теперь же ученые пошли дальше: новые нейроны для трансплантации решили выращивать из собственных клеток пациента. В ряде стран, в том числе и в России, уже ведутся подобные работы. У больного берут клетки кожи, затем их превращают в стволовые клетки, которые в свою очередь дифференцируют в дофаминергические нейроны. Эксперименты по пересадке таких нейронов состоятся уже очень скоро.
Алексей Паевский
Фото istockphoto.com
3.Диагностика болезни Паркинсона
Для постановки диагноза болезнь Паркинсона Ваш врач задаст вопросы о появившихся симптомах, имеющихся проблемах со здоровьем, а также проведет неврологическое обследование. Неврологическое обследование включает в себя специальные вопросы и тесты, которые покажут, насколько хорошо функционируют Ваши нервы. Например, врач будет смотреть, как Вы двигаетесь, проверит силу мышц и рефлексы, зрение. В некоторых случаях может быть рекомендован прием специальных лекарств. И результат того, как работает лекарство, поможет точно диагностировать заболевание.
Лабораторные тесты и анализы
не помогут в диагностике болезни Паркинсона, но они позволят исключить другие заболевания, которые могут вызывать схожие с болезнью Паркинсона симптомы. Процедура МРТ назначается для того, чтобы обнаружить признаки инсульта или опухоли мозга.
О нашей клинике м. Чистые пруды Страница Мединтерком!
Лечение патологии
Стратегии лечения болезни Паркинсона зависят от стадии, на которой пациент начал получать необходимую терапию. По этой причине неврологи предпочитают разделять терапевтические подходы, направленные на купировании ранней и поздней симптоматики.
Лечение на ранних стадиях предполагает применение медикаментов, стимулирующих синтез дофамина в головном мозге. Терапевтический эффект достигается за счет стимуляции дофаминовых выбросов и блокировании из обратного поглощения. Благодаря этому удается добиться снижения скорости гибели нейронов. Базовые препараты могут применяться в составе комплексного лечения или в качестве монотерапии. Сочетание необходимых веществ подбирается неврологом на основании клинической картины паркинсонизма и индивидуальных характеристик пациентов.
Лечение болезни Паркинсона на поздних стадиях остается неизбежным этапом, поскольку медикаментозная терапия позволяет лишь замедлить деструктивные процессы. Прогрессирующая патология дополняется новыми симптомами, которые с трудом купируются. В определенный момент привычная эффективность лекарственных средств снижается. Пациент сталкивается с гиперчувствительностью дофаминовых рецепторов и своеобразным синдромом отмены из-за резистентности организма к принимаемым длительное время веществам.
На фоне этого врачи вынуждены назначать пациентам постоянно растущие дозы медикаментов за счет сокращения интервалов между приемами. Альтернативным решением становится переход на комбинированную схему лечения, при которой используются препараты нескольких групп. В отдельных случаях допустимо хирургическое вмешательство для имплантации пациенту электрода, обеспечивающего глубокую стимуляцию мозга. Этот метод позволяет купировать тремор покоя и восстановить двигательную активность лиц, страдающих от болезни Паркинсона.
Подробное описание исследования
Болезнь Паркинсона — медленно развивающееся заболевание головного мозга, связанное с разрушением структур, ответственных за выработку дофамина. Это провоцирует развитие различных двигательных расстройств, среди которых:
- Тремор покоя — дрожание некоторых частей тела в спокойном состоянии;
- Скованность мышц;
- Замедление движений;
- Нарушение походки;
- Возникновение патологических поз.
Как правило, заболевание проявляет себя после 60 лет. Мужчины по сравнению с женщинами болеют несколько чаще.
Различают первичный, или идиопатический, и вторичный, или симптоматический, паркинсонизм, который может возникать из-за приема некоторых лекарственных препаратов, в результате травм, а также как последствие перенесенного энцефалита.
Специфичным для паркинсонических нарушений является сниженная активность дофаминергической системы. В норме в структурах этой системы осуществляется синтез дофамина — одного из основных тормозных медиаторов центральной нервной системы (ЦНС). Этот важный нейромедиатор образуется путем последовательных ферментативных превращений: фенилаланин → тирозин → L-ДОФА → дофамин, который сохраняется в нейронах головного мозга и по мере необходимости транспортируется к синапсам — местам связывания нейронов — для передачи нервного импульса.
После высвобождения дофамина из нейронов в синапсы примерно 80% его возвращается назад, а оставшаяся небольшая часть теряет свои биологические свойства с помощью ферментов моноаминооксидазы-В (МАО-В) и катехол-О-метилтрансферазы (КОМТ).
Недостаточное образование дофамина приводит к дисбалансу остальных нейромедиаторов ЦНС (глутамата, ацетилхолина и др.), что и провоцирует специфические двигательные нарушения. Активность дофаминергической системы ЦНС снижается с возрастом практически у всех людей, но в ряде случаев она доходит до стадии клинически выраженных расстройств, и у человека развивается паркинсонизм.
Известно, что ЦНС хорошо адаптируется к небольшому дофаминодефициту, и клинические признаки паркинсонизма проявляются только при потере не менее чем 70% дофамина, т.е. при серьезных изменениях.
Примерно в 20% случаев болезнь Паркинсона имеет семейный характер — отмечаются наследственные формы заболевания. Как правило, развитие наследственных форм паркинсонизма связано с мутациями генов SNCA, LRRK2, PRKN. Генетические мутации провоцируют разрушение клеток черной субстанции головного мозга. Эти клетки ответственны за продукцию дофамина.
Ген SNCA кодирует белок а-синуклеин, который выступает основным компонентом телец Леви (патологические белковые образования в нейронах). Мутация гена провоцирует накопление в клетке нерастворимых белковых образований и последующую гибель нейронов.
Ген LRRK2 кодирует белок дардарин, который находится в ядре клетки, а также в тельцах Леви. При мутации гена уровень дардарина значительно увеличивается, что также провоцирует гибель нейронов.
Ген PRKN кодирует белок паркин, который находится в ядрах клеток головного мозга. Паркин разрушает патологические белки в клетках головного мозга. Из-за мутации его функции нарушаются, что приводит к накоплению аномальных белков и гибели нейронов.
Диагноз ставится при наличии характерных клинических проявлений болезни Паркинсона, а также если патология диагностирована у кровных родственников. Генетическое исследование позволяет подтвердить предварительно поставленный диагноз.